第93页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
1. 选试剂 实验室制取二氧化碳所用的试剂是()
A. 纯净的碳酸钙粉末与稀盐酸
B. 大理石与稀硫酸
C. 碳酸钠粉末与浓盐酸
D. 大理石块与稀盐酸
A. 纯净的碳酸钙粉末与稀盐酸
B. 大理石与稀硫酸
C. 碳酸钠粉末与浓盐酸
D. 大理石块与稀盐酸
答案:
1. D
2. 选条件 为探究实验室制取二氧化碳的适宜条件,进行如下实验:
|实验编号试剂|甲|乙|丙|丁|
|----|----|----|----|----|
|1g大理石|块状|块状|粉末状|粉末状|
|10g盐酸(过量)|10%盐酸|30%盐酸|10%盐酸|30%盐酸|
(1)实验甲与实验____对比,是为了探究固体反应物颗粒大小对反应速率的影响。
(2)上述实验中,另一个影响反应速率的因素是____。
|实验编号试剂|甲|乙|丙|丁|
|----|----|----|----|----|
|1g大理石|块状|块状|粉末状|粉末状|
|10g盐酸(过量)|10%盐酸|30%盐酸|10%盐酸|30%盐酸|
(1)实验甲与实验____对比,是为了探究固体反应物颗粒大小对反应速率的影响。
(2)上述实验中,另一个影响反应速率的因素是____。
答案:
【解析】:
(1)要探究固体反应物颗粒大小对反应速率的影响,需要控制盐酸的浓度相同,而固体的颗粒大小不同,实验甲是块状大理石和10%盐酸,实验丙是粉末状大理石和10%盐酸,所以实验甲与实验丙对比,是为了探究固体反应物颗粒大小对反应速率的影响。
(2)从表格中可以看出,除了固体反应物颗粒大小不同外,盐酸的浓度也不同,所以另一个影响反应速率的因素是盐酸的浓度。
【答案】:
(1)丙
(2)盐酸的浓度
(1)要探究固体反应物颗粒大小对反应速率的影响,需要控制盐酸的浓度相同,而固体的颗粒大小不同,实验甲是块状大理石和10%盐酸,实验丙是粉末状大理石和10%盐酸,所以实验甲与实验丙对比,是为了探究固体反应物颗粒大小对反应速率的影响。
(2)从表格中可以看出,除了固体反应物颗粒大小不同外,盐酸的浓度也不同,所以另一个影响反应速率的因素是盐酸的浓度。
【答案】:
(1)丙
(2)盐酸的浓度
3. 选装置:常见的气体发生装置和收集装置如下。

(1)制取二氧化碳所选的发生装置可以是____(填字母,下同),其中装置比较简单的是____,可以随时添加液体的是____,可以控制反应速率的是____,可以随时控制反应的发生与停止的是____。
(2)制取二氧化碳所选的收集装置为____(填字母),依据是____。

(1)制取二氧化碳所选的发生装置可以是____(填字母,下同),其中装置比较简单的是____,可以随时添加液体的是____,可以控制反应速率的是____,可以随时控制反应的发生与停止的是____。
(2)制取二氧化碳所选的收集装置为____(填字母),依据是____。
答案:
【解析】:
(1) 实验室制取二氧化碳用大理石(或石灰石)与稀盐酸反应,该反应是固液不加热型。
发生装置可以是$C$、$D$、$E$、$F$。$C$装置比较简单;$D$装置中的长颈漏斗可以随时添加液体;$E$装置中的分液漏斗可以通过控制液体滴加速度来控制反应速率;$F$装置可以通过关闭或打开止水夹,使试管内压强变化,从而随时控制反应的发生与停止。
(2) 二氧化碳能溶于水,不能用排水法收集;二氧化碳密度比空气大,所以用向上排空气法收集,收集装置为$I$。
【答案】:
(1)$C$、$D$、$E$、$F$;$C$;$D$;$E$;$F$
(2)$I$;二氧化碳密度比空气大
(1) 实验室制取二氧化碳用大理石(或石灰石)与稀盐酸反应,该反应是固液不加热型。
发生装置可以是$C$、$D$、$E$、$F$。$C$装置比较简单;$D$装置中的长颈漏斗可以随时添加液体;$E$装置中的分液漏斗可以通过控制液体滴加速度来控制反应速率;$F$装置可以通过关闭或打开止水夹,使试管内压强变化,从而随时控制反应的发生与停止。
(2) 二氧化碳能溶于水,不能用排水法收集;二氧化碳密度比空气大,所以用向上排空气法收集,收集装置为$I$。
【答案】:
(1)$C$、$D$、$E$、$F$;$C$;$D$;$E$;$F$
(2)$I$;二氧化碳密度比空气大
4. 制取二氧化碳的步骤:①向锥形瓶中放入石灰石,②检查装置气密性,③收集气体,④连接仪器,⑤向长颈漏斗中注入稀盐酸。正确的顺序为____。
答案:
【解析】:制取二氧化碳时,首先要连接仪器,然后检查装置气密性,确保装置不漏气后,向锥形瓶中放入石灰石,接着向长颈漏斗中注入稀盐酸,使石灰石与稀盐酸反应产生二氧化碳,最后收集气体。所以正确的顺序为④②①⑤③。
【答案】:④②①⑤③
【答案】:④②①⑤③
5. 检验、验满二氧化碳。
(1)检验集气瓶内气体是二氧化碳的方法是____。
(2)证明二氧化碳收集满的方法是____。
(1)检验集气瓶内气体是二氧化碳的方法是____。
(2)证明二氧化碳收集满的方法是____。
答案:
【解析】:
(1)二氧化碳能使澄清石灰水变浑浊,这是二氧化碳的特性,所以检验集气瓶内气体是二氧化碳的方法是将澄清石灰水倒入集气瓶中,振荡,若澄清石灰水变浑浊,则该气体是二氧化碳。
(2)二氧化碳不燃烧也不支持燃烧,所以证明二氧化碳收集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,则证明二氧化碳已收集满。
【答案】:
(1)将澄清石灰水倒入集气瓶中,振荡,若澄清石灰水变浑浊,则该气体是二氧化碳
(2)将燃着的木条放在集气瓶口,若木条熄灭,则证明二氧化碳已收集满
(1)二氧化碳能使澄清石灰水变浑浊,这是二氧化碳的特性,所以检验集气瓶内气体是二氧化碳的方法是将澄清石灰水倒入集气瓶中,振荡,若澄清石灰水变浑浊,则该气体是二氧化碳。
(2)二氧化碳不燃烧也不支持燃烧,所以证明二氧化碳收集满的方法是将燃着的木条放在集气瓶口,若木条熄灭,则证明二氧化碳已收集满。
【答案】:
(1)将澄清石灰水倒入集气瓶中,振荡,若澄清石灰水变浑浊,则该气体是二氧化碳
(2)将燃着的木条放在集气瓶口,若木条熄灭,则证明二氧化碳已收集满
6. 某小组以“探究二氧化碳的奥秘”为主题开展如下的项目式学习。
任务一:认识实验室制取二氧化碳的试剂
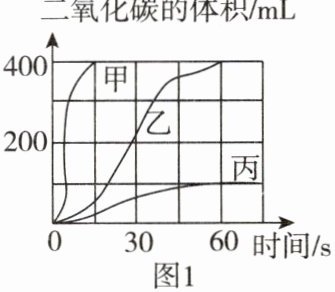
该小组的同学们按下表进行实验,取等质量的大理石加入足量且等量的酸中(杂质不与酸反应),产生的二氧化碳的体积随时间变化曲线如图 1 所示。

(1)上表中实验③对应图 1 中曲线____(填“甲”“乙”或“丙”)。实验室制取二氧化碳不选择实验①中试剂的原因是____;实验③比实验②反应速率快的原因是____。
(2)实验②中反应的化学方程式为____。
任务二:探究是否可用排水集气法收集到$CO_{2}$
已知:实验室通常采用向上排空气法收集二氧化碳。二氧化碳能不能用排水法收集?
小组同学在老师指导下,利用传感器对是否可用排水集气法收集到$CO_{2}$展开探究,实验装置如图 2 所示:
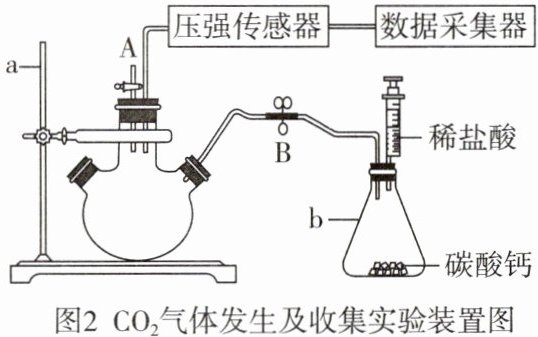
(3)实验步骤如下:
①按实验装置图 2 组装仪器。
②用压强传感器自带的注射器通过活塞 A 迅速向三颈烧瓶注入 50 mL 空气,并一直压住注射器,若压强传感器的读数____,证明装置气密性良好。
③打开活塞 A,将注射器中的稀盐酸迅速注入仪器 b 中,发生反应的化学方程式为____。反应一段时间后,常用____放在 A 处进行验满,收集满后迅速关闭活塞 A,并用弹簧夹夹住导气管 B 处。
④用压强传感器自带的注射器通过活塞 A 向三颈烧瓶中注入 15 mLH_2O,观察两分钟之内体系的压强变化如图 2 所示。
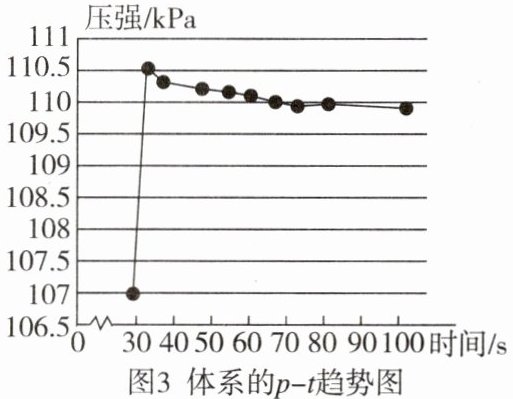
【总结与拓展】
(4)图 3 中 30 s 时体系的压强瞬间增大,后又逐渐减小的原因是____。
(5)经过测算,消耗$CO_{2}的量约为收集到的CO_{2}$总量的 0.53%,因此排水集气法____。
任务三:二氧化碳的性质及用途
将干燥的$CO_{2}$气体通入如图 4 所示装置中一段时间后:
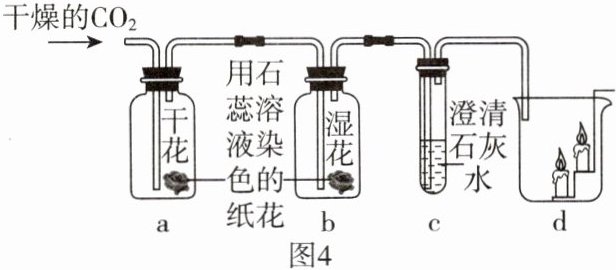
(6)b 处观察到的现象是____,通过 a 和 b 实验____(填“能”或“不能”)说明二氧化碳与水发生了化学反应,原因是____。
(7)实验过程中 d 处发生的现象是____,由此得到启示,二氧化碳可用于____。
任务四:实践操作
小组的同学们设计并制作了喷气船,气体从罐底小孔喷出使船前进,如图 5 所示。
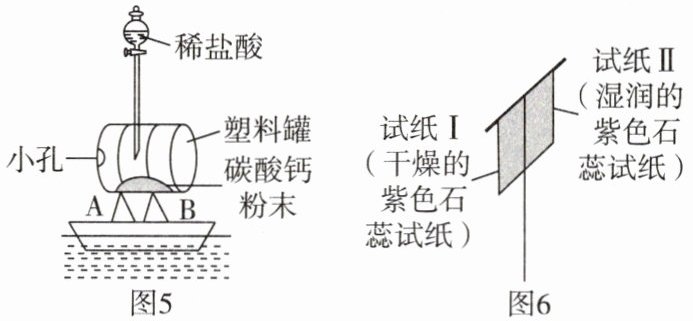
(8)随着小船的前行船身会不断上浮,请解释原因:____。
(9)为便于改变航行方向,小组的同学们又在船身 A 处安上帆杆,如图 6 所示。一段时间后,可观察到____。
任务一:认识实验室制取二氧化碳的试剂
该小组的同学们按下表进行实验,取等质量的大理石加入足量且等量的酸中(杂质不与酸反应),产生的二氧化碳的体积随时间变化曲线如图 1 所示。

(1)上表中实验③对应图 1 中曲线____(填“甲”“乙”或“丙”)。实验室制取二氧化碳不选择实验①中试剂的原因是____;实验③比实验②反应速率快的原因是____。
(2)实验②中反应的化学方程式为____。
任务二:探究是否可用排水集气法收集到$CO_{2}$
已知:实验室通常采用向上排空气法收集二氧化碳。二氧化碳能不能用排水法收集?
小组同学在老师指导下,利用传感器对是否可用排水集气法收集到$CO_{2}$展开探究,实验装置如图 2 所示:

(3)实验步骤如下:
①按实验装置图 2 组装仪器。
②用压强传感器自带的注射器通过活塞 A 迅速向三颈烧瓶注入 50 mL 空气,并一直压住注射器,若压强传感器的读数____,证明装置气密性良好。
③打开活塞 A,将注射器中的稀盐酸迅速注入仪器 b 中,发生反应的化学方程式为____。反应一段时间后,常用____放在 A 处进行验满,收集满后迅速关闭活塞 A,并用弹簧夹夹住导气管 B 处。
④用压强传感器自带的注射器通过活塞 A 向三颈烧瓶中注入 15 mLH_2O,观察两分钟之内体系的压强变化如图 2 所示。

【总结与拓展】
(4)图 3 中 30 s 时体系的压强瞬间增大,后又逐渐减小的原因是____。
(5)经过测算,消耗$CO_{2}的量约为收集到的CO_{2}$总量的 0.53%,因此排水集气法____。
任务三:二氧化碳的性质及用途
将干燥的$CO_{2}$气体通入如图 4 所示装置中一段时间后:

(6)b 处观察到的现象是____,通过 a 和 b 实验____(填“能”或“不能”)说明二氧化碳与水发生了化学反应,原因是____。
(7)实验过程中 d 处发生的现象是____,由此得到启示,二氧化碳可用于____。
任务四:实践操作
小组的同学们设计并制作了喷气船,气体从罐底小孔喷出使船前进,如图 5 所示。

(8)随着小船的前行船身会不断上浮,请解释原因:____。
(9)为便于改变航行方向,小组的同学们又在船身 A 处安上帆杆,如图 6 所示。一段时间后,可观察到____。

答案:
(1)甲;碳酸钙和稀硫酸反应生成的微溶物硫酸钙会覆盖在大理石表面,阻止反应的进一步进行,不能持续产生二氧化碳气体;大理石是粉末状的,与稀盐酸接触面积更大
(2)$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow$
(3)②突然增大后,维持一段时间不变
③$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow$;燃着的木条
(4)加入水,气体被压缩,压强增大,后二氧化碳和水反应,压强又逐渐减小
(5)可以收集$CO_{2}$
(6)纸花变红色;能;通入$CO_{2}$前b中湿花为紫色,说明水不能使石蕊变色,通入$CO_{2}$后a中干花不变色,说明$CO_{2}$不能使石蕊变色,而b中湿花变红,说明是水和二氧化碳反应的产物使石蕊变色,所以对比a、b两实验能说明二氧化碳与水发生了反应
(7)蜡烛由低到高依次熄灭;灭火
(8)反应产生的气体从小孔逸出,使船本身的总质量减小
(9)试纸Ⅰ不变色,试纸Ⅱ变红
(1)甲;碳酸钙和稀硫酸反应生成的微溶物硫酸钙会覆盖在大理石表面,阻止反应的进一步进行,不能持续产生二氧化碳气体;大理石是粉末状的,与稀盐酸接触面积更大
(2)$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow$
(3)②突然增大后,维持一段时间不变
③$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow$;燃着的木条
(4)加入水,气体被压缩,压强增大,后二氧化碳和水反应,压强又逐渐减小
(5)可以收集$CO_{2}$
(6)纸花变红色;能;通入$CO_{2}$前b中湿花为紫色,说明水不能使石蕊变色,通入$CO_{2}$后a中干花不变色,说明$CO_{2}$不能使石蕊变色,而b中湿花变红,说明是水和二氧化碳反应的产物使石蕊变色,所以对比a、b两实验能说明二氧化碳与水发生了反应
(7)蜡烛由低到高依次熄灭;灭火
(8)反应产生的气体从小孔逸出,使船本身的总质量减小
(9)试纸Ⅰ不变色,试纸Ⅱ变红
查看更多完整答案,请扫码查看


