第79页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
7. 2024河南 某反应的微观示意图如图所示,该反应可用于汽车尾气处理。下列说法正确的是()
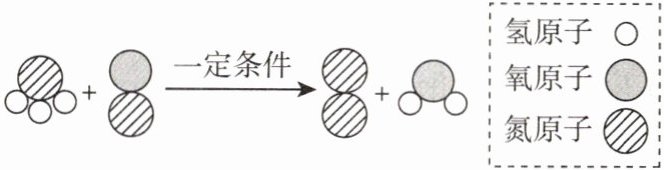
A. 图中的单质为氧气
B. 反应的产物均为无毒物质
C. 反应前后元素的化合价均无变化
D. 反应的化学方程式为$NH_3+NO\xlongequal{一定条件}N_2+H_2O$

A. 图中的单质为氧气
B. 反应的产物均为无毒物质
C. 反应前后元素的化合价均无变化
D. 反应的化学方程式为$NH_3+NO\xlongequal{一定条件}N_2+H_2O$
答案:
B
8. 古有《齐民要术》记载“粟米曲作酢”,“酢”即醋酸也;今有我国科研人员研究出制取醋酸$(CH_3COOH)$的新方法。新方法的反应微观示意图如图所示:
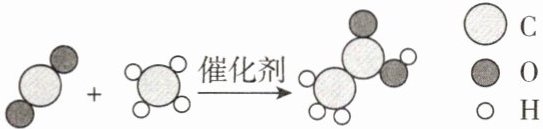
(1)古法酿醋是用粮食经过发酵而成,发酵属于____变化。
(2)保持醋酸化学性质的最小微粒是____。
(3)新方法反应的化学方程式是____;参加反应的二氧化碳和甲烷的质量比是____。
(4)这一新方法的重要意义除了制取醋酸外,还有助于减缓____效应。

(1)古法酿醋是用粮食经过发酵而成,发酵属于____变化。
(2)保持醋酸化学性质的最小微粒是____。
(3)新方法反应的化学方程式是____;参加反应的二氧化碳和甲烷的质量比是____。
(4)这一新方法的重要意义除了制取醋酸外,还有助于减缓____效应。
答案:
(1)化学
(2)醋酸分子
(3)CO₂ + CH₄$\xlongequal{催化剂}$CH₃COOH;11:4
(4)温室
(1)化学
(2)醋酸分子
(3)CO₂ + CH₄$\xlongequal{催化剂}$CH₃COOH;11:4
(4)温室
9. 下列叙述和相应原理(用化学方程式表示)及基本反应类型都正确的是()
A. 拉瓦锡测定空气成分:$2Hg+O_2\xlongequal{\triangle}2HgO,$氧化反应
B. 工业上大量制取氧气:$2H_2O_2\xlongequal{MnO_2}2H_2O+O_2↑,$分解反应
C. 红磷在空气中燃烧:$4P+5O_2\xlongequal{点燃}2P_2O_5,$化合反应
D. 电解水制取氢气:$2H_2O\xlongequal{通电}2H_2+O_2,$分解反应
A. 拉瓦锡测定空气成分:$2Hg+O_2\xlongequal{\triangle}2HgO,$氧化反应
B. 工业上大量制取氧气:$2H_2O_2\xlongequal{MnO_2}2H_2O+O_2↑,$分解反应
C. 红磷在空气中燃烧:$4P+5O_2\xlongequal{点燃}2P_2O_5,$化合反应
D. 电解水制取氢气:$2H_2O\xlongequal{通电}2H_2+O_2,$分解反应
答案:
C
10. 2025济南槐荫区期末,多选 氨气$(NH_3)$是重要的化工原料,利用$N_2$与$H_2O$合成$NH_3$的过程如图所示。下列有关说法中,正确的是()
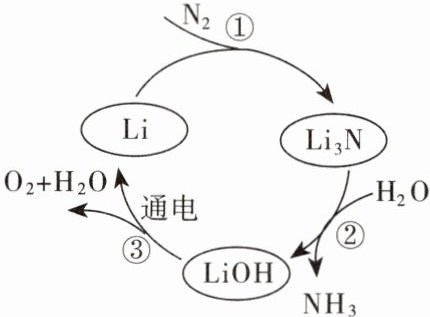
A. 反应①属于化合反应,反应③属于分解反应
B. 整个过程中不需要补充金属Li
C. 反应②中参加反应的$H_2O$与生成$NH_3$的分子个数比为3:1
D. 按照该过程,理论上生成$17gNH_3$至少需要$28gN_2$

A. 反应①属于化合反应,反应③属于分解反应
B. 整个过程中不需要补充金属Li
C. 反应②中参加反应的$H_2O$与生成$NH_3$的分子个数比为3:1
D. 按照该过程,理论上生成$17gNH_3$至少需要$28gN_2$
答案:
A、B、C 【点拨】反应①是N₂和Li反应生成Li₃N的过程,这是一个化合反应。反应③是LiOH通电分解生成Li、O₂和H₂O的过程,这是一个分解反应,A正确;从图中可以看出,锂(Li)在反应过程中不被消耗,因此整个过程中不需要补充金属锂(Li),B正确;反应②是Li₃N和水反应生成LiOH和NH₃,反应的化学方程式为Li₃N + 3H₂O = 3LiOH + NH₃↑,参加反应的H₂O与生成NH₃的分子个数比为3:1,C正确;反应的总方程式可以表示为2N₂ + 6H₂O = 4NH₃ + 3O₂,从这个方程式可以看出,理论上生成17gNH₃需要14gN₂,D不正确。
11. “侯氏制碱法”是我国著名制碱专家侯德榜经过多年研究作出的杰出贡献,其最大的优点是降低了成本,大大提高了NaCl的利用率。
(1)“侯氏制碱法”的原理可表示为$X+NaCl+NaHCO_3\xlongequal{}NH_4Cl+Na_2CO_3,$X的化学式是____,X中一种元素的质量分数:____(结果精确到0.1%)。
(2)用58.5tNaCl(其利用率在96%以上)制碱,至少能生成Na_2CO_3的质量为多少?
(1)“侯氏制碱法”的原理可表示为$X+NaCl+NaHCO_3\xlongequal{}NH_4Cl+Na_2CO_3,$X的化学式是____,X中一种元素的质量分数:____(结果精确到0.1%)。
(2)用58.5tNaCl(其利用率在96%以上)制碱,至少能生成Na_2CO_3的质量为多少?
答案:
解:
(1)NH₃;氮元素的质量分数为82.4%(或氢元素的质量分数为17.6%)
(2)设至少能生成Na₂CO₃的质量为x。
NH₃ + NaCl + NaHCO₃ = NH₄Cl + Na₂CO₃
58.5 106
58.5t×96% x
$\frac{58.5}{106}$ = $\frac{58.5t×96\%}{x}$
x = 101.76t
答:至少能生成Na₂CO₃的质量为101.76t。
(1)NH₃;氮元素的质量分数为82.4%(或氢元素的质量分数为17.6%)
(2)设至少能生成Na₂CO₃的质量为x。
NH₃ + NaCl + NaHCO₃ = NH₄Cl + Na₂CO₃
58.5 106
58.5t×96% x
$\frac{58.5}{106}$ = $\frac{58.5t×96\%}{x}$
x = 101.76t
答:至少能生成Na₂CO₃的质量为101.76t。
查看更多完整答案,请扫码查看


