第47页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
7. 如图所示为四种微观粒子的结构示意图,下列有关说法中错误的是()
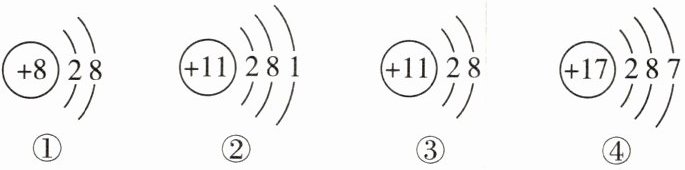
A. ①的化学性质比较稳定
B. ③是一种阴离子
C. ②③属于同种元素
D. ④在化学反应中容易得到电子

A. ①的化学性质比较稳定
B. ③是一种阴离子
C. ②③属于同种元素
D. ④在化学反应中容易得到电子
答案:
B 点拨:①的最外层电子数为8,属于相对稳定结构,化学性质比较稳定,A正确;③中质子数=11,电子数=10,是一种阳离子,B错;②③的质子数相同,属于同种元素,C正确;④的最外层电子数是7,大于4,在化学反应中容易得到电子,D正确。
8. 根据如图有关信息判断,下列说法中,错误的是()

A. 镁原子核内有12个质子
B. 硫原子在化学反应中易失去2个电子
C. 镁元素的相对原子质量为24.30
D. 在元素周期表中,镁和硫都位于第三周期

A. 镁原子核内有12个质子
B. 硫原子在化学反应中易失去2个电子
C. 镁元素的相对原子质量为24.30
D. 在元素周期表中,镁和硫都位于第三周期
答案:
B
9. 如图是元素周期表中部分元素的原子结构示意图。
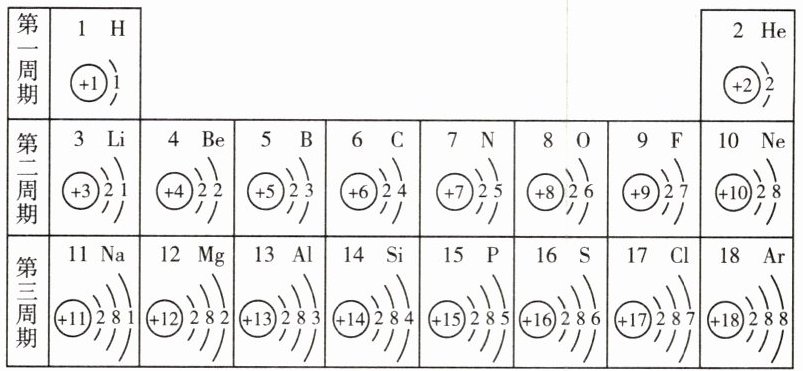
(1)氟原子核内有____个质子,在化学反应中氟原子容易____(填“得到”或“失去”)电子。
(2)不同种元素的本质区别是____。
(3)下列各组元素具有相似化学性质的是____(填字母)。挑选一个你认为正确的选项,并从原子结构的角度说明原因:____。
A. He和Ne
B. O和S
C. He和Mg
D. Al和Si
(4)请写出核外电子排布与氖原子相同的一种阳离子____(写离子符号)。

(1)氟原子核内有____个质子,在化学反应中氟原子容易____(填“得到”或“失去”)电子。
(2)不同种元素的本质区别是____。
(3)下列各组元素具有相似化学性质的是____(填字母)。挑选一个你认为正确的选项,并从原子结构的角度说明原因:____。
A. He和Ne
B. O和S
C. He和Mg
D. Al和Si
(4)请写出核外电子排布与氖原子相同的一种阳离子____(写离子符号)。
答案:
(1)9;得到
(2)质子数不同
(3)A、B;He原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;Ne原子的最外层电子数为8,属于稀有气体元素的原子,化学性质稳定(或O和S的最外层电子数相同,化学性质相似)
(4)$Na^{+}$(或$Mg^{2+}$、$Al^{3+}$)
点拨:
(1)由氟原子的结构示意图可知,氟原子的核内质子数是9;氟原子最外层电子数是7,多于4,在化学反应中易得到1个电子而形成带1个单位负电荷的阴离子。
(2)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素的本质区别是质子数不同。
(3)决定元素化学性质的是原子的最外层电子数,O和S的最外层电子数相同,化学性质相似。He原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定。Ne原子的最外层电子数为8,属于稀有气体元素的原子,化学性质稳定。镁原子的最外层电子数为2,在化学反应中易失去2个电子而形成阳离子,尽管最外层电子数与氦相同,但氦和镁的化学性质不相似。
(4)钠离子、镁离子、铝离子均是核外电子排布与氖原子相同的阳离子,其离子符号分别是$Na^{+}$、$Mg^{2+}$、$Al^{3+}$。
(1)9;得到
(2)质子数不同
(3)A、B;He原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定;Ne原子的最外层电子数为8,属于稀有气体元素的原子,化学性质稳定(或O和S的最外层电子数相同,化学性质相似)
(4)$Na^{+}$(或$Mg^{2+}$、$Al^{3+}$)
点拨:
(1)由氟原子的结构示意图可知,氟原子的核内质子数是9;氟原子最外层电子数是7,多于4,在化学反应中易得到1个电子而形成带1个单位负电荷的阴离子。
(2)元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),不同种元素的本质区别是质子数不同。
(3)决定元素化学性质的是原子的最外层电子数,O和S的最外层电子数相同,化学性质相似。He原子的最外层电子数为2,但其核外只有一个电子层,属于稀有气体元素的原子,化学性质稳定。Ne原子的最外层电子数为8,属于稀有气体元素的原子,化学性质稳定。镁原子的最外层电子数为2,在化学反应中易失去2个电子而形成阳离子,尽管最外层电子数与氦相同,但氦和镁的化学性质不相似。
(4)钠离子、镁离子、铝离子均是核外电子排布与氖原子相同的阳离子,其离子符号分别是$Na^{+}$、$Mg^{2+}$、$Al^{3+}$。
10. 如图为探究微观粒子性质的实验装置。

回答下列问题。
(1)连接好装置。打开弹簧夹,推动注射器的活塞,注入空气,____(填现象),说明该装置气密性良好。再关闭弹簧夹,拔下注射器。
(2)用注射器吸取30mL浓氨水,重新连接该装置。____(填操作),推动注射器的活塞将浓氨水通过导管注入装置下端两侧玻璃管内,此时观察到玻璃管内湿润的酚酞滤纸条自下而上慢慢变红,该现象主要说明:氨水的性质是____,微观粒子的性质是____。
(3)马上将装置下端玻璃管底部同时浸入装有等体积的热水和冷水的烧杯中,发现____(填“左侧”或“右侧”)玻璃管内湿润的酚酞滤纸条自下而上变红的速率加快,说明温度对微观粒子的运动速率产生了影响。拆除装置前,向装置内注入稀盐酸或稀硫酸防止氨气逸散到空气中,污染环境。

回答下列问题。
(1)连接好装置。打开弹簧夹,推动注射器的活塞,注入空气,____(填现象),说明该装置气密性良好。再关闭弹簧夹,拔下注射器。
(2)用注射器吸取30mL浓氨水,重新连接该装置。____(填操作),推动注射器的活塞将浓氨水通过导管注入装置下端两侧玻璃管内,此时观察到玻璃管内湿润的酚酞滤纸条自下而上慢慢变红,该现象主要说明:氨水的性质是____,微观粒子的性质是____。
(3)马上将装置下端玻璃管底部同时浸入装有等体积的热水和冷水的烧杯中,发现____(填“左侧”或“右侧”)玻璃管内湿润的酚酞滤纸条自下而上变红的速率加快,说明温度对微观粒子的运动速率产生了影响。拆除装置前,向装置内注入稀盐酸或稀硫酸防止氨气逸散到空气中,污染环境。
答案:
(1)两侧气球变大,且一段时间内不缩小
(2)打开弹簧夹;易挥发(合理即可);分子在不停运动着
(3)左侧
点拨:
(1)打开弹簧夹,推动注射器的活塞,装置内压强变大,若装置气密性良好,两侧气球变大,且一段时间内不缩小。
(2)打开弹簧夹才能将浓氨水注入装置内。玻璃管内湿润的酚酞滤纸条自下而上慢慢变红是因为氨水易挥发,挥发出的氨分子在不停运动着,遇水形成氨水,氨水能使酚酞变红。
(3)温度越高分子运动越快,所以左侧玻璃管内湿润的酚酞滤纸条自下而上变红的速率加快。
(1)两侧气球变大,且一段时间内不缩小
(2)打开弹簧夹;易挥发(合理即可);分子在不停运动着
(3)左侧
点拨:
(1)打开弹簧夹,推动注射器的活塞,装置内压强变大,若装置气密性良好,两侧气球变大,且一段时间内不缩小。
(2)打开弹簧夹才能将浓氨水注入装置内。玻璃管内湿润的酚酞滤纸条自下而上慢慢变红是因为氨水易挥发,挥发出的氨分子在不停运动着,遇水形成氨水,氨水能使酚酞变红。
(3)温度越高分子运动越快,所以左侧玻璃管内湿润的酚酞滤纸条自下而上变红的速率加快。
查看更多完整答案,请扫码查看


