第35页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
10. 如图为某原子结构模型图,其中a、b、c是构成该原子的三种不同微观粒子。下列说法中正确的是()
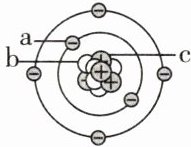
A. 原子核由b和c构成
B. 原子中a与c的数目可能相等
C. 原子中b与c的数目一定相等
D. 原子的质量主要集中在a和b上

A. 原子核由b和c构成
B. 原子中a与c的数目可能相等
C. 原子中b与c的数目一定相等
D. 原子的质量主要集中在a和b上
答案:
A
11. 2025福州仓山区期中 科学家运用了模型建构的方法探索原子的结构。下列对原子结构模型演变过程的认识,不正确的是()
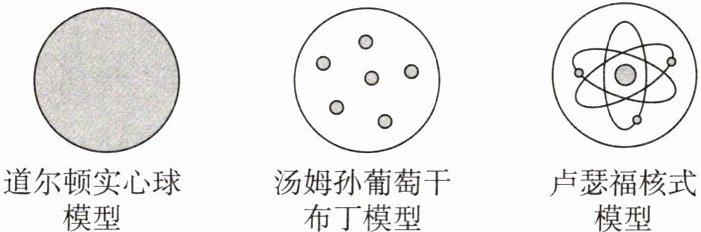
A. 道尔顿认为原子是不可再分的实心球,是构成物质的最小粒子
B. 汤姆孙等人在原子中发现了电子,推翻了道尔顿实心球模型
C. 卢瑟福等人通过α粒子散射实验修正了汤姆孙葡萄干布丁模型
D. 卢瑟福核式模型是最完善的原子结构模型,不会被替代

A. 道尔顿认为原子是不可再分的实心球,是构成物质的最小粒子
B. 汤姆孙等人在原子中发现了电子,推翻了道尔顿实心球模型
C. 卢瑟福等人通过α粒子散射实验修正了汤姆孙葡萄干布丁模型
D. 卢瑟福核式模型是最完善的原子结构模型,不会被替代
答案:
D
12. 根据所学知识,回答下列问题。
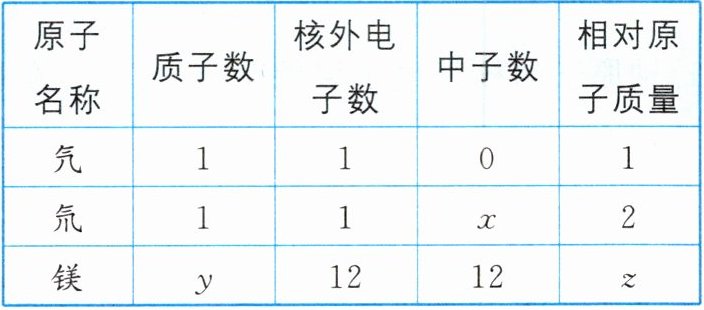
(1)上表中x的值为______,y的值为______,z的值为______。
(2)已知碳-12原子的实际质量约为$1.993×10⁻^2^6kg,$则表中镁原子的实际质量约为______(写出计算过程)。

(1)上表中x的值为______,y的值为______,z的值为______。
(2)已知碳-12原子的实际质量约为$1.993×10⁻^2^6kg,$则表中镁原子的实际质量约为______(写出计算过程)。
答案:
(1)1;12;24
(2)$24×(1.993×10^{-26}kg×\frac {1}{12})=3.986×10^{-26}kg$
点拨:
(1)相对原子质量≈中子数+质子数,则有$2=1+x,x=1$;在原子中质子数=核外电子数,则$y=12$;相对原子质量≈中子数+质子数,则有$z=y+12=12+12=24$。
(2)镁的相对原子质量为24,根据某原子的相对原子质量=$\frac{一个该原子的质量}{碳-12原子的质量×\frac{1}{12}}$,计算镁原子的实际质量。
(1)1;12;24
(2)$24×(1.993×10^{-26}kg×\frac {1}{12})=3.986×10^{-26}kg$
点拨:
(1)相对原子质量≈中子数+质子数,则有$2=1+x,x=1$;在原子中质子数=核外电子数,则$y=12$;相对原子质量≈中子数+质子数,则有$z=y+12=12+12=24$。
(2)镁的相对原子质量为24,根据某原子的相对原子质量=$\frac{一个该原子的质量}{碳-12原子的质量×\frac{1}{12}}$,计算镁原子的实际质量。
13. 学科素养·科学史 19世纪以前,人们一直认为原子是不可分的。1897年汤姆孙发现了带负电的电子,并提出类似“西瓜”的原子模型。为进一步探究原子的结构,1909年英国科学家卢瑟福进行了著名的α粒子轰击金箔实验。
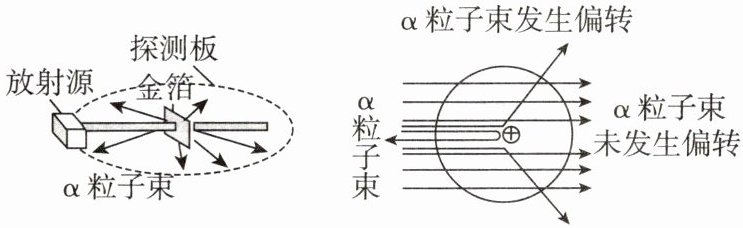
【收集证据】绝大多数α粒子(带正电的氦原子核)穿过金箔后仍沿原来的方向前进,只有少数α粒子发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样,运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”,其中的“很小的结构”指的是______。
(2)能说明原子内部绝大部分是空的证据是______。
(3)根据卢瑟福的实验所产生的现象,不能够获得的结论是______(填字母)。
A. 原子核体积很小
B. 原子核质量较大
C. 原子核带正电
D. 核外电子带负电
(4)请你根据对原子结构的认识,分析原子不显电性的原因:______。

【收集证据】绝大多数α粒子(带正电的氦原子核)穿过金箔后仍沿原来的方向前进,只有少数α粒子发生了较大的偏转,并且有极少数α粒子的偏转超过90°,有的甚至几乎达到180°,像是被金箔弹了回来。
【猜想与假设】α粒子遇到电子后,就像飞行的子弹碰到灰尘一样,运动方向不会发生明显的改变,而结果却出乎意料,除非原子的大部分质量集中到了一个很小的结构上,否则大角度的散射是不可能的。
【解释与结论】
(1)卢瑟福所说的“除非原子的大部分质量集中到了一个很小的结构上”,其中的“很小的结构”指的是______。
(2)能说明原子内部绝大部分是空的证据是______。
(3)根据卢瑟福的实验所产生的现象,不能够获得的结论是______(填字母)。
A. 原子核体积很小
B. 原子核质量较大
C. 原子核带正电
D. 核外电子带负电
(4)请你根据对原子结构的认识,分析原子不显电性的原因:______。
答案:
(1)原子核
(2)绝大多数α粒子穿过金箔后仍沿原来的方向前进
(3)D
(4)原子核内质子所带正电荷与核外电子所带负电荷数量相等、电性相反
(1)原子核
(2)绝大多数α粒子穿过金箔后仍沿原来的方向前进
(3)D
(4)原子核内质子所带正电荷与核外电子所带负电荷数量相等、电性相反
查看更多完整答案,请扫码查看


