2025年高考必刷题高三化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年高考必刷题高三化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第37页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
1. [湖南衡阳2024月考]已知:100%硫酸吸收SO₃可生成焦硫酸(分子式为H₂S₂O₇或H₂SO₄·SO₃);焦硫酸可与水发生反应。下列说法不正确的是 ( )
A. 焦硫酸具有强氧化性
B. Na₂S₂O₇溶于水所得溶液显中性
C. 98%的H₂SO₄可以表示为SO₃·$\frac{10}{9}$H₂O
D. 焦硫酸与水反应的产物是强电解质
A. 焦硫酸具有强氧化性
B. Na₂S₂O₇溶于水所得溶液显中性
C. 98%的H₂SO₄可以表示为SO₃·$\frac{10}{9}$H₂O
D. 焦硫酸与水反应的产物是强电解质
答案:
B 考查点:焦硫酸的性质
【解析】由浓硫酸中 +6 价硫具有强氧化性可知,焦硫酸中 +6 价硫也具有强氧化性,A 正确;$Na_{2}S_{2}O_{7}$可写成$Na_{2}SO_{4}\cdot SO_{3}$,溶于水后和水反应生成硫酸,溶液显酸性,B 错误;假设 98%浓硫酸的质量为 100 g,则$H_{2}SO_{4}$的质量为$100g×98\% = 98g$,$H_{2}O$的质量为$100g - 98g = 2g$,则$H_{2}SO_{4}$的物质的量为$\frac{98g}{98g\cdot mol^{-1}} = 1mol$,$H_{2}O$的物质的量为$\frac{2g}{18g\cdot mol^{-1}}=\frac{1}{9}mol$,故 98%的$H_{2}SO_{4}$可表示为$H_{2}SO_{4}\cdot\frac{1}{9}H_{2}O$,若把$H_{2}SO_{4}$表示为$SO_{3}\cdot H_{2}O$,则 98%的浓硫酸可表示为$SO_{3}\cdot\frac{10}{9}H_{2}O$,C 正确;焦硫酸与水反应生成硫酸,反应的化学方程式为$H_{2}SO_{4}\cdot SO_{3}+H_{2}O = 2H_{2}SO_{4}$,硫酸属于强电解质,D 正确。
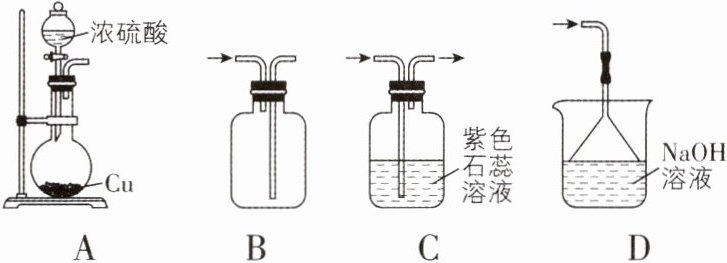
2. [江苏2024联考]下列装置按制备SO₂、收集、验证漂白性及尾气处理的顺序进行实验(“→”表示气流方向),能达到实验目的的是 ( )

答案:
D 考查点:$SO_{2}$的制备、收集、检验装置分析
【解析】铜与浓硫酸需在加热条件下才能反应生成二氧化硫,A 错误;二氧化硫密度比空气大,应该采用向上排空气法进行收集(“长进短出”),B 错误;$SO_{2}$具有漂白性,但不能漂白酸碱指示剂,C 错误;二氧化硫与$NaOH$能发生反应,可以用氢氧化钠溶液进行尾气处理,且要防倒吸,D 正确。
3. [广东广州2024一模]浓硫酸与蔗糖发生作用的过程如图所示。下列说法不正确的是( )

A. 过程①白色固体变黑,体现了浓硫酸的脱水性
B. 过程②产生具有刺激性气味的气体,体现了浓硫酸的酸性
C. 过程②中固体体积膨胀与SO₂、CO₂的生成有关
D. 过程中硫酸分子发生了化学键的断裂

A. 过程①白色固体变黑,体现了浓硫酸的脱水性
B. 过程②产生具有刺激性气味的气体,体现了浓硫酸的酸性
C. 过程②中固体体积膨胀与SO₂、CO₂的生成有关
D. 过程中硫酸分子发生了化学键的断裂
答案:
B 考查点:浓硫酸的性质
【解析】浓硫酸具有脱水性,能将有机物分子中的 H 原子和 O 原子按 2:1 的比例脱除,故蔗糖中加入浓硫酸,白色固体变黑,体现浓硫酸的脱水性,A 正确;浓硫酸作用下蔗糖脱水炭化并释放大量热,则发生反应$C + 2H_{2}SO_{4}(浓)\stackrel{\triangle}{=\!=\!=}CO_{2}\uparrow + 2SO_{2}\uparrow + 2H_{2}O$,该反应体现了浓硫酸的氧化性,B 错误;浓硫酸发生反应$C + 2H_{2}SO_{4}(浓)\stackrel{\triangle}{=\!=\!=}CO_{2}\uparrow + 2SO_{2}\uparrow + 2H_{2}O$,使固体疏松,固体体积膨胀与$SO_{2}$、$CO_{2}$的生成有关,C 正确;该过程中,硫酸分子发生化学反应,发生了化学键的断裂,D 正确。
4. [北京海淀区2024期中]几种含硫物质的转化如图(部分反应条件略去),下列判断不正确的是 ( )

A. ①中,试剂a可以是Cu
B. ②中,需要确保NaOH溶液足量
C. ③中,生成1 mol Na₂S₂O₃时,转移4 mol电子
D. ③中,将S换为Cl₂,氧化产物为Na₂SO₄

A. ①中,试剂a可以是Cu
B. ②中,需要确保NaOH溶液足量
C. ③中,生成1 mol Na₂S₂O₃时,转移4 mol电子
D. ③中,将S换为Cl₂,氧化产物为Na₂SO₄
答案:
C 考查点:硫及其化合物的性质与转化
【解析】$Cu$与浓$H_{2}SO_{4}$加热条件下发生氧化还原反应,生成硫酸铜、二氧化硫和水,A 正确;$NaOH$溶液足量可保证二氧化硫被完全吸收且生成$Na_{2}SO_{3}$,B 正确;S 和$Na_{2}SO_{3}$发生反应$Na_{2}SO_{3}+S = Na_{2}S_{2}O_{3}$,生成 1 mol $Na_{2}S_{2}O_{3}$时,转移 2 mol 电子,C 错误;$Cl_{2}$具有强氧化性,能将$Na_{2}SO_{3}$氧化成$Na_{2}SO_{4}$,D 正确。
5. [湖北名校联盟2024联考]工业制硫酸的原理示意图如图:

下列说法不正确的是 ( )
A. 燃烧的化学方程式为4FeS₂ + 11O₂$\stackrel{燃烧}{=\!=\!=}$2Fe₂O₃+8SO₂
B. 1 mol SO₂和足量O₂充分反应转移2 mol电子
C. 用98.3%的浓硫酸吸收三氧化硫可避免形成酸雾
D. 可用浓氨水吸收生产过程中的尾气并转化为铵盐

下列说法不正确的是 ( )
A. 燃烧的化学方程式为4FeS₂ + 11O₂$\stackrel{燃烧}{=\!=\!=}$2Fe₂O₃+8SO₂
B. 1 mol SO₂和足量O₂充分反应转移2 mol电子
C. 用98.3%的浓硫酸吸收三氧化硫可避免形成酸雾
D. 可用浓氨水吸收生产过程中的尾气并转化为铵盐
答案:
B 考查点:硫及其化合物的转化及应用
【解析】$FeS_{2}$燃烧生成氧化铁和二氧化硫,化学方程式为$4FeS_{2}+11O_{2}\stackrel{燃烧}{=\!=\!=}2Fe_{2}O_{3}+8SO_{2}$,A 正确;$2SO_{2}+O_{2}\stackrel{催化剂}{\underset{\triangle}{\rightleftharpoons}}2SO_{3}$反应可逆,1 mol $SO_{2}$和足量$O_{2}$充分反应转移电子的物质的量小于 2 mol,B 错误;用 98.3%的浓硫酸吸收三氧化硫可避免形成酸雾,C 正确;用浓氨水吸收生产过程中的尾气(二氧化硫)可生成亚硫酸铵,D 正确。
6. [贵州贵阳2024一模]下列各实验的操作、现象或结论有错误的是 ( )
|选项|实验|现象|结论|
| ---- | ---- | ---- | ---- |
|A|将SO₂分别通入品红的乙醇溶液和品红的水溶液|品红的乙醇溶液不褪色,品红的水溶液慢慢褪色|说明使品红褪色的不是SO₂而是SO₂与水反应后的产物|
|B|将氧气通入H₂S的水溶液中|溶液变浑浊|氧的非金属性强于硫|
|C|向溶有SO₂的BaCl₂溶液中通入气体X|出现白色沉淀|X一定具有强氧化性|
|D|向某溶液中滴加盐酸酸化的BaCl₂溶液|有白色沉淀生成|该溶液中不一定含有SO₄²⁻|
|选项|实验|现象|结论|
| ---- | ---- | ---- | ---- |
|A|将SO₂分别通入品红的乙醇溶液和品红的水溶液|品红的乙醇溶液不褪色,品红的水溶液慢慢褪色|说明使品红褪色的不是SO₂而是SO₂与水反应后的产物|
|B|将氧气通入H₂S的水溶液中|溶液变浑浊|氧的非金属性强于硫|
|C|向溶有SO₂的BaCl₂溶液中通入气体X|出现白色沉淀|X一定具有强氧化性|
|D|向某溶液中滴加盐酸酸化的BaCl₂溶液|有白色沉淀生成|该溶液中不一定含有SO₄²⁻|
答案:
C 突破点:实验设计与评价
【解析】将$SO_{2}$分别通入品红的乙醇溶液和品红的水溶液,观察到品红的乙醇溶液不褪色,而品红的水溶液慢慢褪色,可以说明使品红褪色的不是$SO_{2}$,而是$SO_{2}$与水反应后的产物,A 正确;将氧气通入$H_{2}S$的水溶液中,溶液变浑浊说明发生反应$O_{2}+2H_{2}S = 2S\downarrow + 2H_{2}O$,则氧化性:$O_{2}>S$,氧的非金属性强于硫,B 正确;气体 X 是不具有强氧化性的氨气时,向溶有$SO_{2}$的$BaCl_{2}$溶液中通入氨气,氨气与二氧化硫优先反应生成亚硫酸铵,然后亚硫酸铵与$BaCl_{2}$发生复分解反应生成$BaSO_{3}$白色沉淀,C 错误;白色沉淀可能是$BaSO_{4}$,也可能是$AgCl$,故溶液中不一定含有$SO_{4}^{2 - }$,也可能含有$Ag^{ + }$,D 正确。
**易错警示**:$SO_{2}$通入$BaCl_{2}$溶液不能产生白色沉淀,再通入气体 X 能产生白色沉淀,该沉淀可能是由$NH_{3}$中和酸后生成的$BaSO_{3}$,也可能是由$Cl_{2}$氧化$SO_{2}$产生的$BaSO_{4}$。
查看更多完整答案,请扫码查看


