2025年学霸高考黑题化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学霸高考黑题化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第9页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
经典真题1 (2025·云南,10,3分)
铜催化下,由CO₂电合成正丙醇的关键步骤如图。下列说法正确的是(

A.Ⅰ到Ⅱ的过程中发生氧化反应
B.Ⅱ到Ⅲ的过程中有非极性键生成
C.Ⅳ的示意图为
D.催化剂Cu可降低反应热
铜催化下,由CO₂电合成正丙醇的关键步骤如图。下列说法正确的是(
C
)
A.Ⅰ到Ⅱ的过程中发生氧化反应
B.Ⅱ到Ⅲ的过程中有非极性键生成
C.Ⅳ的示意图为

D.催化剂Cu可降低反应热
答案:
经典真题1 C 解题思路
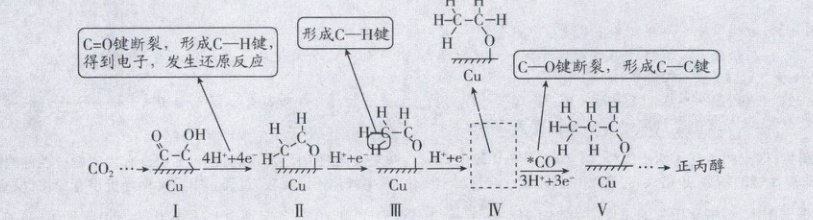
C=O键断裂,形成C—H键,得到电子,发生还原反应
形成C—H键
$\mathrm{H-\overset{H}{\overset{|}{C}}-\overset{H}{\overset{|}{C}}-H}$
$\mathrm{\overset{H}{|}O}$
$\mathrm{Cu}$
C—O键断裂,形成C—C键
$\mathrm{CO_2·s \overset{O}{\overset{||}{C}}-C-OH+4H^++4e^-\rightarrow H-\overset{H}{\overset{|}{C}}-C-OH+H^++e^-\rightarrow H^++e^-\rightarrow *CO+3H^++3e^-\rightarrow 正丙醇}$ (其中中间过程图示含Cu催化作用)
解析:I到II的过程中消耗了氢离子和电子,属于还原反应,A错误;II到III的过程中生成了一根C—H键,如图 ,有极性键生成,不是非极性键,B错误;II到III的过程中生成了一根C—H键,由III结合氢离子和电子可知,III到IV也生成了一根C—H键,IV到V才结合CO,可知IV的示意图为
,有极性键生成,不是非极性键,B错误;II到III的过程中生成了一根C—H键,由III结合氢离子和电子可知,III到IV也生成了一根C—H键,IV到V才结合CO,可知IV的示意图为 ,C正确;催化剂可改变活化能,加快反应速率,不能改变反应热,D错误。
,C正确;催化剂可改变活化能,加快反应速率,不能改变反应热,D错误。
经典真题1 C 解题思路

C=O键断裂,形成C—H键,得到电子,发生还原反应
形成C—H键
$\mathrm{H-\overset{H}{\overset{|}{C}}-\overset{H}{\overset{|}{C}}-H}$
$\mathrm{\overset{H}{|}O}$
$\mathrm{Cu}$
C—O键断裂,形成C—C键
$\mathrm{CO_2·s \overset{O}{\overset{||}{C}}-C-OH+4H^++4e^-\rightarrow H-\overset{H}{\overset{|}{C}}-C-OH+H^++e^-\rightarrow H^++e^-\rightarrow *CO+3H^++3e^-\rightarrow 正丙醇}$ (其中中间过程图示含Cu催化作用)
解析:I到II的过程中消耗了氢离子和电子,属于还原反应,A错误;II到III的过程中生成了一根C—H键,如图
 ,有极性键生成,不是非极性键,B错误;II到III的过程中生成了一根C—H键,由III结合氢离子和电子可知,III到IV也生成了一根C—H键,IV到V才结合CO,可知IV的示意图为
,有极性键生成,不是非极性键,B错误;II到III的过程中生成了一根C—H键,由III结合氢离子和电子可知,III到IV也生成了一根C—H键,IV到V才结合CO,可知IV的示意图为 ,C正确;催化剂可改变活化能,加快反应速率,不能改变反应热,D错误。
,C正确;催化剂可改变活化能,加快反应速率,不能改变反应热,D错误。 经典真题2 (2024·贵州,14,3分)
AgCN与CH₃CH₂Br可发生取代反应,反应过程中CN⁻的C原子和N原子均可进攻CH₃CH₂Br,分别生成腈(CH₃CH₂CN)和异腈(CH₃CH₂NC)两种产物。通过量子化学计算得到的反应历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。

由图示信息,下列说法错误的是(
A.从CH₃CH₂Br生成CH₃CH₂CN和CH₃CH₂NC的反应都是放热反应
B.过渡态TS1是由CN⁻的C原子进攻CH₃CH₂Br的α-C而形成的
C.Ⅰ中“N—Ag”之间的作用力比Ⅱ中“C—Ag”之间的作用力弱
D.生成CH₃CH₂CN放热更多,低温时CH₃CH₂CN是主要产物
AgCN与CH₃CH₂Br可发生取代反应,反应过程中CN⁻的C原子和N原子均可进攻CH₃CH₂Br,分别生成腈(CH₃CH₂CN)和异腈(CH₃CH₂NC)两种产物。通过量子化学计算得到的反应历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。

由图示信息,下列说法错误的是(
D
)A.从CH₃CH₂Br生成CH₃CH₂CN和CH₃CH₂NC的反应都是放热反应
B.过渡态TS1是由CN⁻的C原子进攻CH₃CH₂Br的α-C而形成的
C.Ⅰ中“N—Ag”之间的作用力比Ⅱ中“C—Ag”之间的作用力弱
D.生成CH₃CH₂CN放热更多,低温时CH₃CH₂CN是主要产物
答案:
经典真题2 D 解题思路
明确初始状态、过程与结果的位置,将题目中问题的目标信息与对应的能量位置相对应,以内容明确的图示能量位置进行针对性的分析;当信息不明确时,注意寻找其中的特征内容,并以此代入符合图示的能量位置进行针对性的分析。

解析:由图可知,两种路径生成的产物的总能量均低于反应物,故从$\mathrm{CH_3CH_2Br}$生成$\mathrm{CH_3CH_2CN}$和$\mathrm{CH_3CH_2NC}$的反应都是放热反应,A正确;与Br原子相连的C原子为α - C,由反应历程及能量变化图可知,过渡态TS1是由$\mathrm{CN^-}$的C原子与$\mathrm{CH_3CH_2Br}$的α - C相作用,形成碳碳键,一般来说是由带负电的原子进攻,$\mathrm{CN^-}$为带负电的进攻方,B正确;分析图示,N—Ag相连的为最右下角的I状态,C—Ag相连且形态与N—Ag连接相似的为最左下角的II状态,圆圈内为各自断裂C—Ag和N—Ag的过程,可以看出断裂C—Ag反应的能量大于断裂N—Ag反应的,故C—Ag作用力强于N—Ag,C正确;低温状态时,反应的决速步取决于产生过渡态的反应,由于生成$\mathrm{CH_3CH_2CN}$所需要的活化能高,反应速率慢,故低温时更容易生成$\mathrm{CH_3CH_2NC}$(主要产物),D错误。
经典真题2 D 解题思路
明确初始状态、过程与结果的位置,将题目中问题的目标信息与对应的能量位置相对应,以内容明确的图示能量位置进行针对性的分析;当信息不明确时,注意寻找其中的特征内容,并以此代入符合图示的能量位置进行针对性的分析。

解析:由图可知,两种路径生成的产物的总能量均低于反应物,故从$\mathrm{CH_3CH_2Br}$生成$\mathrm{CH_3CH_2CN}$和$\mathrm{CH_3CH_2NC}$的反应都是放热反应,A正确;与Br原子相连的C原子为α - C,由反应历程及能量变化图可知,过渡态TS1是由$\mathrm{CN^-}$的C原子与$\mathrm{CH_3CH_2Br}$的α - C相作用,形成碳碳键,一般来说是由带负电的原子进攻,$\mathrm{CN^-}$为带负电的进攻方,B正确;分析图示,N—Ag相连的为最右下角的I状态,C—Ag相连且形态与N—Ag连接相似的为最左下角的II状态,圆圈内为各自断裂C—Ag和N—Ag的过程,可以看出断裂C—Ag反应的能量大于断裂N—Ag反应的,故C—Ag作用力强于N—Ag,C正确;低温状态时,反应的决速步取决于产生过渡态的反应,由于生成$\mathrm{CH_3CH_2CN}$所需要的活化能高,反应速率慢,故低温时更容易生成$\mathrm{CH_3CH_2NC}$(主要产物),D错误。
经典真题3 (2024·北京,10,3分)
可采用Deacon催化氧化法将工业副产物HCl制成Cl₂,实现氯资源的再利用。反应的热化学方程式为4HCl(g)+O₂(g)$\xlongequal{CuO}$2Cl₂(g)+2H₂O(g) $\Delta H$=-114.4 kJ·mol⁻¹。下图所示为该法的一种催化机理。

下列说法不正确的是(
A.Y为反应物HCl,W为生成物H₂O
B.反应制得1 mol Cl₂,须投入2 mol CuO
C.升高反应温度,HCl被O₂氧化制Cl₂的反应平衡常数减小
D.图中转化涉及的反应中有两个属于氧化还原反应
可采用Deacon催化氧化法将工业副产物HCl制成Cl₂,实现氯资源的再利用。反应的热化学方程式为4HCl(g)+O₂(g)$\xlongequal{CuO}$2Cl₂(g)+2H₂O(g) $\Delta H$=-114.4 kJ·mol⁻¹。下图所示为该法的一种催化机理。

下列说法不正确的是(
B
)A.Y为反应物HCl,W为生成物H₂O
B.反应制得1 mol Cl₂,须投入2 mol CuO
C.升高反应温度,HCl被O₂氧化制Cl₂的反应平衡常数减小
D.图中转化涉及的反应中有两个属于氧化还原反应
答案:
经典真题3 B 解题思路
分析流程图,我们要注意物质的变化状况和反应流程主体外的其他物质。CuO和$\mathrm{Cu(OH)Cl}$相比多出了H和Cl元素,可以推测加入的Y为HCl,$\mathrm{Cu(OH)Cl}$相对于$\mathrm{Cu_2OCl_2}$少了H和O元素,可以推测W为$\mathrm{H_2O}$。
解析:由分析可知,Y为反应物HCl,W为生成物$\mathrm{H_2O}$,A正确;CuO在反应中作催化剂,会不断循环,适量即可,B错误;总反应为放热反应,其他条件一定,升温平衡逆向移动,平衡常数减小,C正确;图中涉及的两个氧化还原反应是$\mathrm{CuCl_2\rightarrow CuCl}$和$\mathrm{CuCl\rightarrow Cu_2OCl_2}$,D正确。
分析流程图,我们要注意物质的变化状况和反应流程主体外的其他物质。CuO和$\mathrm{Cu(OH)Cl}$相比多出了H和Cl元素,可以推测加入的Y为HCl,$\mathrm{Cu(OH)Cl}$相对于$\mathrm{Cu_2OCl_2}$少了H和O元素,可以推测W为$\mathrm{H_2O}$。
解析:由分析可知,Y为反应物HCl,W为生成物$\mathrm{H_2O}$,A正确;CuO在反应中作催化剂,会不断循环,适量即可,B错误;总反应为放热反应,其他条件一定,升温平衡逆向移动,平衡常数减小,C正确;图中涉及的两个氧化还原反应是$\mathrm{CuCl_2\rightarrow CuCl}$和$\mathrm{CuCl\rightarrow Cu_2OCl_2}$,D正确。
查看更多完整答案,请扫码查看


