2025年学霸高考黑题化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学霸高考黑题化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第21页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
二氯化二硫(S₂Cl₂)是一种黄色至略微红的液体,有剧毒。向熔融的硫中通入限量的氯气即可生成S₂Cl₂,进一步氯化则会得到SCl₂。
已知:Ⅰ.S₂Cl₂、SCl₂、S的部分性质如下:
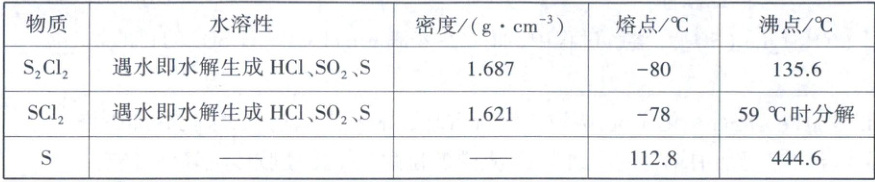
Ⅱ.Kₛₚ(AgCl)=1.8×10⁻¹⁰、Kₛₚ(Ag₂CrO₄)=1.12×10⁻¹²,Ag₂CrO₄为砖红色沉淀。
下列是某兴趣小组制备S₂Cl₂并分析其纯度的实验,回答下列问题:
(1)S₂Cl₂所有原子满足最外层8电子稳定结构,其电子式为
(2)写出S₂Cl₂溶于水发生反应的化学方程式:
(3)兴趣小组利用如下装置制备S₂Cl₂。
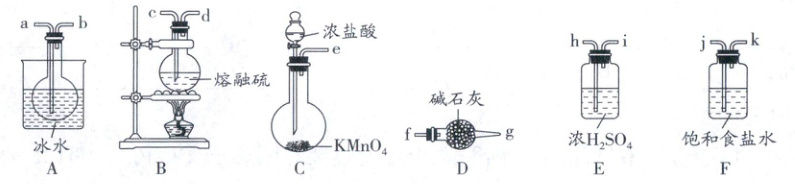
①A、B、C装置中均用到的玻璃容器的名称是
②C装置中发生反应的离子方程式为
③装置的正确连接顺序是e→j→k→h→i→
④D装置中碱石灰的作用是
(4)S₂Cl₂(所含杂质为SCl₂)纯度的测定:准确称取1.35 g所得产品溶于水,加入Ba(OH)₂溶液调节pH至9.0左右,过滤后将滤液配成250.00 mL溶液,用移液管量取25.00 mL溶液放入锥形瓶中,加入几滴K₂CrO₄溶液,用0.10 mol·L⁻¹的AgNO₃溶液滴定,平行滴定三次,平均消耗AgNO₃溶液的体积为20.40 mL。
①加入Ba(OH)₂溶液调节pH至9.0左右的目的是。
②滴定终点的判断依据是
③S₂Cl₂的纯度为
已知:Ⅰ.S₂Cl₂、SCl₂、S的部分性质如下:

Ⅱ.Kₛₚ(AgCl)=1.8×10⁻¹⁰、Kₛₚ(Ag₂CrO₄)=1.12×10⁻¹²,Ag₂CrO₄为砖红色沉淀。
下列是某兴趣小组制备S₂Cl₂并分析其纯度的实验,回答下列问题:
(1)S₂Cl₂所有原子满足最外层8电子稳定结构,其电子式为
:Cl:S:S:Cl:
。(2)写出S₂Cl₂溶于水发生反应的化学方程式:
2S₂Cl₂+2H₂O══4HCl+SO₂↑+3S↓
。(3)兴趣小组利用如下装置制备S₂Cl₂。

①A、B、C装置中均用到的玻璃容器的名称是
圆底烧瓶
。②C装置中发生反应的离子方程式为
2MnO₄⁻+10Cl⁻+16H⁺══2Mn²⁺+5Cl₂↑+8H₂O
。③装置的正确连接顺序是e→j→k→h→i→
c→d→a→b
→f(按气流流出方向)。④D装置中碱石灰的作用是
除去过量的氯气,防止环境污染;防止空气中的水蒸气进入装置A与S₂Cl₂反应
。(4)S₂Cl₂(所含杂质为SCl₂)纯度的测定:准确称取1.35 g所得产品溶于水,加入Ba(OH)₂溶液调节pH至9.0左右,过滤后将滤液配成250.00 mL溶液,用移液管量取25.00 mL溶液放入锥形瓶中,加入几滴K₂CrO₄溶液,用0.10 mol·L⁻¹的AgNO₃溶液滴定,平行滴定三次,平均消耗AgNO₃溶液的体积为20.40 mL。
①加入Ba(OH)₂溶液调节pH至9.0左右的目的是。
②滴定终点的判断依据是
当滴入最后半滴AgNO₃溶液时,白色沉淀中出现砖红色,且半分钟内砖红色未消失
。③S₂Cl₂的纯度为
93.6%
(保留三位有效数字)。
答案:
(1):Cl:S:S:Cl:
(2)2S₂Cl₂+2H₂O══4HCl+SO₂↑+3S↓
(3)①圆底烧瓶 ②2MnO₄⁻+10Cl⁻+16H⁺══2Mn²⁺+5Cl₂↑+8H₂O ③c→d→a→b ④除去过量的氯气,防止环境污染;防止空气中的水蒸气进入装置A与S₂Cl₂反应
(4)①防止pH过低,CrO₄²⁻会转化为Cr₂O₇²⁻;防止pH过高,会与滴入的Ag⁺反应生成AgOH,均会干扰滴定 ②当滴入最后半滴AgNO₃溶液时,白色沉淀中出现砖红色,且半分钟内砖红色未消失 ③93.6%
解题思路
装置C利用高锰酸钾固体与浓盐酸制备氯气,同时生成氯化锰、氯化钾与水,先通过F中饱和食盐水除去氯气中混有的氯化氢气体,再通过E用浓硫酸干燥氯气,氯气与硫单质在B中反应,A冷凝收集产物,D中碱石灰吸收空气中水蒸气,防止进入A中导致S₂Cl₂水解,同时吸收未反应的氯气,防止污染空气。
解析:
(1)S₂Cl₂所有原子符合最外层8电子稳定结构,根据S和Cl原子结构可知,S要形成2个共价键,Cl只需形成1个共价键,故其电子式为:Cl:S:S:Cl:。
(2)根据题干中信息,S₂Cl₂溶于水生成HCl、SO₂、S。
(3)①C装置是KMnO₄与浓盐酸反应制Cl₂的装置;③根据题意,S₂Cl₂制备实验的顺序是:制备Cl₂→除HCl→干燥→制S₂Cl₂→收集S₂Cl₂→防水→尾气处理,故装置连接顺序是e→j→k→h→i→c→d→a→b→f(→g)(气流流向流出方向);④该实验中碱石灰既要除去氯气,防止环境污染,也要防止空气中的水蒸气进入收集装置,使之与S₂Cl₂反应。
(4)②实验中,当Cl⁻达到滴定终点时,再滴入AgNO₃溶液,即生成砖红色的Ag₂CrO₄沉淀,故滴定终点的判断依据是当滴入最后半滴AgNO₃溶液时,产生砖红色沉淀,且半分钟内砖红色未消失;③S₂Cl₂及SCl₂均会与水反应产生Cl⁻,故该题计算时可利用Cl原子守恒进行计算。设原1.35 g产品中S₂Cl₂的物质的量为x,SCl₂的物质的量为y,结合题意可得:135x+103y=1.35 g,2x+2y=0.10 mol·L⁻¹×20.40×10⁻³L×$\frac{250 mL}{25.00 mL}$,解得x≈0.009 36 mol,最终得到S₂Cl₂的纯度约为$\frac{0.009 36 mol×135 g·mol⁻¹}{1.35 g}$×100% = 93.6%。
提分技能
(1)实验装置连接的顺序及思路
发生装置→除杂装置→干燥装置→收集或检验装置→尾气吸收装置
决定 ↓ ↓ ↓ ↓ ↓
发生装置 除杂装置 干燥装置 收集方法 尾气吸收装置
选择 ↓ ↓ ↓ ↓ ↓
除杂试剂状态 干燥剂状态 气体密度与水溶性 气体性质
分析 ↓
杂质气体种类及性质
(2)实验装置连接的注意事项
①除杂和干燥装置的先后顺序
a.溶液除杂,先除杂后干燥;b.加热法除杂,先干燥后除杂。
②接口的连接顺序
a.吸收装置,“长”进“短”出;b.量气装置,“短”进“长”出;c.洗气装置,“长”进“短”出;d.干燥管,“大”进“小”出。
(1):Cl:S:S:Cl:
(2)2S₂Cl₂+2H₂O══4HCl+SO₂↑+3S↓
(3)①圆底烧瓶 ②2MnO₄⁻+10Cl⁻+16H⁺══2Mn²⁺+5Cl₂↑+8H₂O ③c→d→a→b ④除去过量的氯气,防止环境污染;防止空气中的水蒸气进入装置A与S₂Cl₂反应
(4)①防止pH过低,CrO₄²⁻会转化为Cr₂O₇²⁻;防止pH过高,会与滴入的Ag⁺反应生成AgOH,均会干扰滴定 ②当滴入最后半滴AgNO₃溶液时,白色沉淀中出现砖红色,且半分钟内砖红色未消失 ③93.6%
解题思路
装置C利用高锰酸钾固体与浓盐酸制备氯气,同时生成氯化锰、氯化钾与水,先通过F中饱和食盐水除去氯气中混有的氯化氢气体,再通过E用浓硫酸干燥氯气,氯气与硫单质在B中反应,A冷凝收集产物,D中碱石灰吸收空气中水蒸气,防止进入A中导致S₂Cl₂水解,同时吸收未反应的氯气,防止污染空气。
解析:
(1)S₂Cl₂所有原子符合最外层8电子稳定结构,根据S和Cl原子结构可知,S要形成2个共价键,Cl只需形成1个共价键,故其电子式为:Cl:S:S:Cl:。
(2)根据题干中信息,S₂Cl₂溶于水生成HCl、SO₂、S。
(3)①C装置是KMnO₄与浓盐酸反应制Cl₂的装置;③根据题意,S₂Cl₂制备实验的顺序是:制备Cl₂→除HCl→干燥→制S₂Cl₂→收集S₂Cl₂→防水→尾气处理,故装置连接顺序是e→j→k→h→i→c→d→a→b→f(→g)(气流流向流出方向);④该实验中碱石灰既要除去氯气,防止环境污染,也要防止空气中的水蒸气进入收集装置,使之与S₂Cl₂反应。
(4)②实验中,当Cl⁻达到滴定终点时,再滴入AgNO₃溶液,即生成砖红色的Ag₂CrO₄沉淀,故滴定终点的判断依据是当滴入最后半滴AgNO₃溶液时,产生砖红色沉淀,且半分钟内砖红色未消失;③S₂Cl₂及SCl₂均会与水反应产生Cl⁻,故该题计算时可利用Cl原子守恒进行计算。设原1.35 g产品中S₂Cl₂的物质的量为x,SCl₂的物质的量为y,结合题意可得:135x+103y=1.35 g,2x+2y=0.10 mol·L⁻¹×20.40×10⁻³L×$\frac{250 mL}{25.00 mL}$,解得x≈0.009 36 mol,最终得到S₂Cl₂的纯度约为$\frac{0.009 36 mol×135 g·mol⁻¹}{1.35 g}$×100% = 93.6%。
提分技能
(1)实验装置连接的顺序及思路
发生装置→除杂装置→干燥装置→收集或检验装置→尾气吸收装置
决定 ↓ ↓ ↓ ↓ ↓
发生装置 除杂装置 干燥装置 收集方法 尾气吸收装置
选择 ↓ ↓ ↓ ↓ ↓
除杂试剂状态 干燥剂状态 气体密度与水溶性 气体性质
分析 ↓
杂质气体种类及性质
(2)实验装置连接的注意事项
①除杂和干燥装置的先后顺序
a.溶液除杂,先除杂后干燥;b.加热法除杂,先干燥后除杂。
②接口的连接顺序
a.吸收装置,“长”进“短”出;b.量气装置,“短”进“长”出;c.洗气装置,“长”进“短”出;d.干燥管,“大”进“小”出。
查看更多完整答案,请扫码查看


