2025年学霸高考黑题化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学霸高考黑题化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第66页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
巩固训练4 (2025·河北邢台模拟) 电池级${MnSO_{4}}$对纯度要求特别高,以工业级${MnSO_{4}}$(含${Ca^{2+}}$、${Mg^{2+}}$、${Zn^{2+}}$、${Co^{2+}}$、${Ni^{2+}}$等金属离子)为原料制备高纯${MnSO_{4}}$的过程如下。回答下列问题:
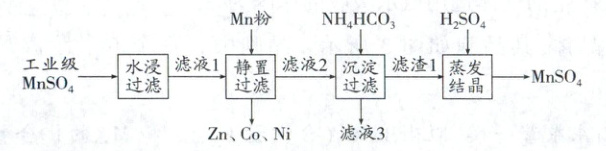
工业级${MnSO_{4}}$经水浸过滤得滤液1,滤液1中加入${Mn}$粉、静置过滤得滤液2,滤液2中加入${NH_{4}HCO_{3}}$、沉淀过滤得滤渣1和滤液3,滤渣1中加入${H_{2}SO_{4}}$、蒸发结晶得${MnSO_{4}}$。
(1)加入${Mn}$粉过程中,${Mn}$粉的作用为
(2)加入${NH_{4}HCO_{3}}$时主要反应的化学方程式为
(3)“沉淀过滤”的反应温度不宜过高的原因是
(4)将“滤渣1”用纯水洗涤,证明沉淀洗涤干净的操作是
(5)结合$K_{sp}$可知加入${NH_{4}HCO_{3}}$的最好方式是

A. 向${NH_{4}HCO_{3}}$溶液中滴加滤液2
B. 同时滴加${NH_{4}HCO_{3}}$溶液和滤液2
C. 向滤液2中滴加${NH_{4}HCO_{3}}$溶液
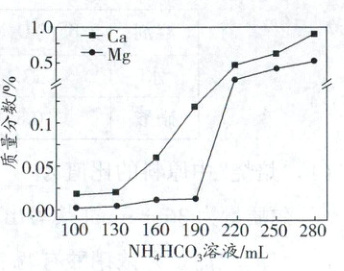
(6)取样$200mL$“滤液2”,${MnSO_{4}}$的浓度为$1.35mol· L^{-1}$,${Ca^{2+}}$、${Mg^{2+}}$随着$2mol· L^{-1}\ {NH_{4}HCO_{3}}$溶液的加入转化的沉淀的量的变化如图,${NH_{4}HCO_{3}}$加入量应为
(7)“滤液3”中仍有大量${Mn^{2+}}$,为了提高原料利用率可采取的处理方法是
(8)最终制得的${MnSO_{4}}$晶体颗粒大小不均匀,可能的原因是

工业级${MnSO_{4}}$经水浸过滤得滤液1,滤液1中加入${Mn}$粉、静置过滤得滤液2,滤液2中加入${NH_{4}HCO_{3}}$、沉淀过滤得滤渣1和滤液3,滤渣1中加入${H_{2}SO_{4}}$、蒸发结晶得${MnSO_{4}}$。
(1)加入${Mn}$粉过程中,${Mn}$粉的作用为
将$Zn^{2+}$、$Co^{2+}$、$Ni^{2+}$还原为单质
。(2)加入${NH_{4}HCO_{3}}$时主要反应的化学方程式为
$MnSO_4 + 2NH_4HCO_3 = MnCO_3 \downarrow + (NH_4)_2SO_4 + CO_2 \uparrow + H_2O$
。(3)“沉淀过滤”的反应温度不宜过高的原因是
温度过高,$NH_4HCO_3$易分解
。(4)将“滤渣1”用纯水洗涤,证明沉淀洗涤干净的操作是
取最后一次洗涤液于试管中,加入$BaCl_2$溶液,若不生成白色沉淀,则已洗净
。(5)结合$K_{sp}$可知加入${NH_{4}HCO_{3}}$的最好方式是
C
(填字母)。
A. 向${NH_{4}HCO_{3}}$溶液中滴加滤液2
B. 同时滴加${NH_{4}HCO_{3}}$溶液和滤液2
C. 向滤液2中滴加${NH_{4}HCO_{3}}$溶液

(6)取样$200mL$“滤液2”,${MnSO_{4}}$的浓度为$1.35mol· L^{-1}$,${Ca^{2+}}$、${Mg^{2+}}$随着$2mol· L^{-1}\ {NH_{4}HCO_{3}}$溶液的加入转化的沉淀的量的变化如图,${NH_{4}HCO_{3}}$加入量应为
130 mL
。(7)“滤液3”中仍有大量${Mn^{2+}}$,为了提高原料利用率可采取的处理方法是
将多次实验的滤液集中浓缩,继续加入$NH_4HCO_3$溶液沉淀
。(8)最终制得的${MnSO_{4}}$晶体颗粒大小不均匀,可能的原因是
升温速率不均匀(或升温速率过快)
。
答案:
巩固训练4
(1)将$Zn^{2+}$、$Co^{2+}$、$Ni^{2+}$还原为单质
(2)$MnSO_4 + 2NH_4HCO_3 = MnCO_3 \downarrow + (NH_4)_2SO_4 + CO_2 \uparrow + H_2O$
(3)温度过高,$NH_4HCO_3$易分解
(4)取最后一次洗涤液于试管中,加入$BaCl_2$溶液,若不生成白色沉淀,则已洗净
(5)C
(6)130 mL
(7)将多次实验的滤液集中浓缩,继续加入$NH_4HCO_3$溶液沉淀
(8)升温速率不均匀(或升温速率过快)
解题思路
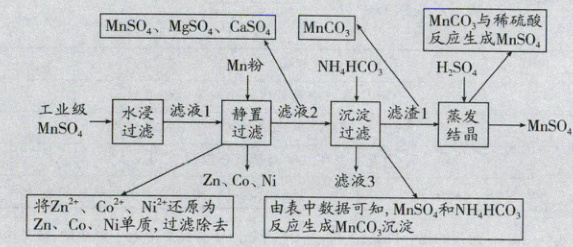
解析:
(1)由题给流程图分析可知,加入$Mn$粉,得到单质$Zn$、$Co$、$Ni$,说明$Mn$将$Zn^{2+}$、$Co^{2+}$、$Ni^{2+}$还原为单质。
(2)分析流程可知,“沉淀过滤”中加入碳酸氢铵,得到的“滤渣1”为$MnCO_3$,$MnCO_3$不溶于水但溶于酸,所以产物中不能有$H^+$生成。
(3)由于碳酸氢铵受热易分解,故“沉淀过滤”的反应温度不宜过高。
(4)“滤液2”中含有$SO_4^{2-}$,“滤渣1”为$MnCO_3$,可通过检验$SO_4^{2-}$判断“滤渣1”是否洗净。
(5)滤液2中含$MnSO_4$、$MgSO_4$、$CaSO_4$,若$NH_4HCO_3$过量,沉淀$Mn^{2+}$的同时,$Ca^{2+}$和$Mg^{2+}$也会转化为沉淀,难以分离;若滤液2过量,根据题给溶度积可知,$NH_4HCO_3$会优先与$Mn^{2+}$反应,少量的$NH_4HCO_3$不与其他离子反应,则应向滤液2中滴加$NH_4HCO_3$溶液。
(6)由题图可知,当加入130 mL$NH_4HCO_3$溶液时,能保证$MnCO_3$沉淀量大且$CaCO_3$、$MgCO_3$沉淀量小。
(8)升温速度不均匀或温度升高过快均会导致产生的晶体颗粒大小不均匀。
巩固训练4
(1)将$Zn^{2+}$、$Co^{2+}$、$Ni^{2+}$还原为单质
(2)$MnSO_4 + 2NH_4HCO_3 = MnCO_3 \downarrow + (NH_4)_2SO_4 + CO_2 \uparrow + H_2O$
(3)温度过高,$NH_4HCO_3$易分解
(4)取最后一次洗涤液于试管中,加入$BaCl_2$溶液,若不生成白色沉淀,则已洗净
(5)C
(6)130 mL
(7)将多次实验的滤液集中浓缩,继续加入$NH_4HCO_3$溶液沉淀
(8)升温速率不均匀(或升温速率过快)
解题思路

解析:
(1)由题给流程图分析可知,加入$Mn$粉,得到单质$Zn$、$Co$、$Ni$,说明$Mn$将$Zn^{2+}$、$Co^{2+}$、$Ni^{2+}$还原为单质。
(2)分析流程可知,“沉淀过滤”中加入碳酸氢铵,得到的“滤渣1”为$MnCO_3$,$MnCO_3$不溶于水但溶于酸,所以产物中不能有$H^+$生成。
(3)由于碳酸氢铵受热易分解,故“沉淀过滤”的反应温度不宜过高。
(4)“滤液2”中含有$SO_4^{2-}$,“滤渣1”为$MnCO_3$,可通过检验$SO_4^{2-}$判断“滤渣1”是否洗净。
(5)滤液2中含$MnSO_4$、$MgSO_4$、$CaSO_4$,若$NH_4HCO_3$过量,沉淀$Mn^{2+}$的同时,$Ca^{2+}$和$Mg^{2+}$也会转化为沉淀,难以分离;若滤液2过量,根据题给溶度积可知,$NH_4HCO_3$会优先与$Mn^{2+}$反应,少量的$NH_4HCO_3$不与其他离子反应,则应向滤液2中滴加$NH_4HCO_3$溶液。
(6)由题图可知,当加入130 mL$NH_4HCO_3$溶液时,能保证$MnCO_3$沉淀量大且$CaCO_3$、$MgCO_3$沉淀量小。
(8)升温速度不均匀或温度升高过快均会导致产生的晶体颗粒大小不均匀。
查看更多完整答案,请扫码查看


