2025年学霸高考黑题化学人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年学霸高考黑题化学人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第108页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
巩固训练8 (2025·辽宁丹东一模节选)硫广泛应用于医药、储能电池等领域。采用不同的方法制备单质硫。利用H₂S+O₂=S+H₂O₂产生硫,装置如下。电解质溶液均为稀硫酸。
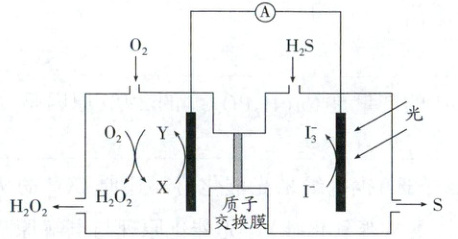
(1)加入少量KI能持续生成S,结合有关反应解释原因:
(2)X、Y代表 中的一种。X是。
中的一种。X是。
(3)由光直接驱动的化学反应是

(1)加入少量KI能持续生成S,结合有关反应解释原因:
$3I^- - 2e^- \longrightarrow I_3^-$,$I_3^- + H_2S \longrightarrow 3I^- + S + 2H^+$,$I^-$、$I_3^-$不断循环转化
。(2)X、Y代表
 中的一种。X是。
中的一种。X是。(3)由光直接驱动的化学反应是
$3I^- + $ $ +2H^+$
$ +2H^+$
(用一个完整的离子方程式表示)。 $ +2H^+$
$ +2H^+$
答案:
巩固训练8
(1)$3I^- - 2e^- \longrightarrow I_3^-$,$I_3^- + H_2S \longrightarrow 3I^- + S + 2H^+$,$I^-$、$I_3^-$不断循环转化
(2)
(3)$3I^- + $ $ +2H^+$
$ +2H^+$
解题思路
装置右侧电极在光照条件下$I^-$失去电子生成$I_3^-$,发生氧化反应,为负极,左侧为正极,电极上X生成Y,发生还原反应。
解析:
(1)加入$KI$,电离出$I^-$,发生反应$3I^- - 2e^- \longrightarrow I_3^-$,$I_3^- + H_2S \longrightarrow 3I^- + S + 2H^+$,$I^-$和$I_3^-$不断循环转化;能持续生成$S$。
巩固训练8
(1)$3I^- - 2e^- \longrightarrow I_3^-$,$I_3^- + H_2S \longrightarrow 3I^- + S + 2H^+$,$I^-$、$I_3^-$不断循环转化
(2)
(3)$3I^- + $
 $ +2H^+$
$ +2H^+$解题思路
装置右侧电极在光照条件下$I^-$失去电子生成$I_3^-$,发生氧化反应,为负极,左侧为正极,电极上X生成Y,发生还原反应。
解析:
(1)加入$KI$,电离出$I^-$,发生反应$3I^- - 2e^- \longrightarrow I_3^-$,$I_3^- + H_2S \longrightarrow 3I^- + S + 2H^+$,$I^-$和$I_3^-$不断循环转化;能持续生成$S$。
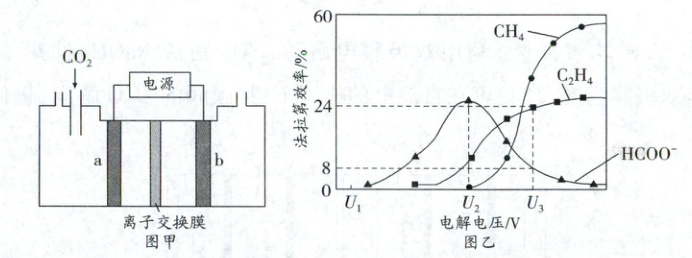
巩固训练9 (2025·北京一模节选)“双碳”背景下,CO₂的资源化利用成为全世界的研究热点。电催化还原CO₂也可以制备甲酸,原理如图甲所示,电解质溶液为KOH。
(1)电极b是电解池的
(2)2024年,我国研究人员为降低系统能耗,对图甲装置改进,搭建“(阴阳极)共产甲酸耦合系统”,将KOH电解液更换为KOH+CH₃OH混合溶液,应将
(3)CO₂的电化学还原过程比较复杂,在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。
已知:FE%=\$\frac{Q_X(生成还原产物X所需要的电量)}{Q_总(电解过程中通过的总电量)}\$×100%,其中,Q_X=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为U₁V时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物是
②当电解电压为U₃V时,电解生成的C₂H₄和HCOO⁻的物质的量之比为
(1)电极b是电解池的
阳
极,电极反应式为$4OH^- - 4e^- \longrightarrow O_2 \uparrow + 2H_2O$
。(2)2024年,我国研究人员为降低系统能耗,对图甲装置改进,搭建“(阴阳极)共产甲酸耦合系统”,将KOH电解液更换为KOH+CH₃OH混合溶液,应将
b
极区(填“a”或“b”)电解液更换。此时,该电极的电极反应式为$CH_3OH - 4e^- + 5OH^- \longrightarrow HCOO^- + 4H_2O$
。(3)CO₂的电化学还原过程比较复杂,在相同条件下,恒定通过电解池的电量,电解得到的部分还原产物的法拉第效率(FE%)随电解电压的变化如图乙所示。
已知:FE%=\$\frac{Q_X(生成还原产物X所需要的电量)}{Q_总(电解过程中通过的总电量)}\$×100%,其中,Q_X=nF,n表示电解生成还原产物X所转移电子的物质的量,F表示法拉第常数。
①当电解电压为U₁V时,电解过程中含碳还原产物的FE%为0,阴极主要还原产物是
$H_2$
(填化学式)。②当电解电压为U₃V时,电解生成的C₂H₄和HCOO⁻的物质的量之比为
$1:2$
。
答案:
巩固训练9
(1)阳 $4OH^- - 4e^- \longrightarrow O_2 \uparrow + 2H_2O$
(2)b $CH_3OH - 4e^- + 5OH^- \longrightarrow HCOO^- + 4H_2O$
(3)①$H_2$ ②$1:2$
解题思路
电催化还原$CO_2$制备甲酸,则通入$CO_2$的电极($a$极)为阴极,电极反应为$H_2O + CO_2 + 2e^- \longrightarrow HCOO^- + OH^-$;$b$极为阳极,电极反应为$4OH^- - 4e^- \longrightarrow O_2 \uparrow + 2H_2O$。
解析:
(3)①当电解电压为$U_1V$时,若电解过程中含碳还原产物的$FE\%$为0,则水放电生成$H_2$,即阴极反应为$2H_2O + 2e^- \longrightarrow H_2 \uparrow + 2OH^-$;②由图乙可知$\frac{FE\%(C_2H_4)}{FE\%(HCOO^-)} = \frac{Q_总}{F × 12n(C_2H_4)} = \frac{24}{8} , \frac{n(C_2H_4)}{n(HCOO^-)} = 1:2$。
(1)阳 $4OH^- - 4e^- \longrightarrow O_2 \uparrow + 2H_2O$
(2)b $CH_3OH - 4e^- + 5OH^- \longrightarrow HCOO^- + 4H_2O$
(3)①$H_2$ ②$1:2$
解题思路
电催化还原$CO_2$制备甲酸,则通入$CO_2$的电极($a$极)为阴极,电极反应为$H_2O + CO_2 + 2e^- \longrightarrow HCOO^- + OH^-$;$b$极为阳极,电极反应为$4OH^- - 4e^- \longrightarrow O_2 \uparrow + 2H_2O$。
解析:
(3)①当电解电压为$U_1V$时,若电解过程中含碳还原产物的$FE\%$为0,则水放电生成$H_2$,即阴极反应为$2H_2O + 2e^- \longrightarrow H_2 \uparrow + 2OH^-$;②由图乙可知$\frac{FE\%(C_2H_4)}{FE\%(HCOO^-)} = \frac{Q_总}{F × 12n(C_2H_4)} = \frac{24}{8} , \frac{n(C_2H_4)}{n(HCOO^-)} = 1:2$。
查看更多完整答案,请扫码查看


