2025年全优课堂九年级化学下册
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年全优课堂九年级化学下册 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第9页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
8. 为验证铁、铜、锌、银的金属活动性顺序,某小组做了如图甲、乙、丙所示的三个实验(所用金属形状与大小、稀盐酸的质量与浓度均相同)。

(1)通过实验甲和丙可比较锌和铁的金属活动性强弱,依据的实验现象是______________。
(2)一段时间后,通过观察实验乙的现象可以得到结论:______________________________。
(3)由于图甲、乙、丙所示三个实验仍不能完全得出四种金属的活动性顺序,该小组设计了一个补充实验丁。若按图丁所示实验进行探究,选用下列哪组试剂实验后可以达到实验目的______(填选项字母)。
A. 铜和硫酸铝溶液
B. 铁和稀硫酸
C. 银和稀盐酸
D. 铜和稀盐酸

(1)通过实验甲和丙可比较锌和铁的金属活动性强弱,依据的实验现象是______________。
(2)一段时间后,通过观察实验乙的现象可以得到结论:______________________________。
(3)由于图甲、乙、丙所示三个实验仍不能完全得出四种金属的活动性顺序,该小组设计了一个补充实验丁。若按图丁所示实验进行探究,选用下列哪组试剂实验后可以达到实验目的______(填选项字母)。
A. 铜和硫酸铝溶液
B. 铁和稀硫酸
C. 银和稀盐酸
D. 铜和稀盐酸
答案:
(1)锌与稀盐酸反应产生气泡的速率比铁与稀盐酸反应产生气泡的速率快
(2)铜的金属活动性比银强(或铜能置换出硝酸银溶液中的银)
(3)D
(1)锌与稀盐酸反应产生气泡的速率比铁与稀盐酸反应产生气泡的速率快
(2)铜的金属活动性比银强(或铜能置换出硝酸银溶液中的银)
(3)D
9. (昭通中考)某化学小组在AgNO₃和Cu(NO₃)₂的混合溶液中加入一定质量的锌粉,充分反应后过滤,得到滤液和滤渣。他们对所得滤液和滤渣有如下描述:①滤液中一定含有Zn(NO₃)₂;②滤渣中一定含有Ag,可能含有Cu和Zn;③若滤液呈蓝色,则向滤渣中滴加稀盐酸无明显现象;④若向滤渣中滴加稀盐酸有气泡产生,则滤液中一定没有AgNO₃和Cu(NO₃)₂。上述四种描述中正确的个数为( )
A. 1个
B. 2个
C. 4个
D. 3个
A. 1个
B. 2个
C. 4个
D. 3个
答案:
C 提示:由金属活动性顺序可知,锌>铜>银。向含有AgNO₃、Cu(NO₃)₂的混合液中加入一定量的锌粉,锌粉会首先置换硝酸银中的银,待硝酸银完全反应后继续与硝酸铜发生反应,化学方程式为Zn + 2AgNO₃ = Zn(NO₃)₂ + 2Ag、Zn + Cu(NO₃)₂ = Zn(NO₃)₂ + Cu。①滤液中一定含有Zn(NO₃)₂,故正确;②滤渣中一定含有Ag,可能含有Cu和Zn,故正确;③若滤液呈蓝色,则Cu(NO₃)₂未反应完,滤渣中没有锌,故向滤渣中滴加稀盐酸无明显现象,故正确;④在滤渣中加入稀盐酸有气体产生,则一定含有锌,说明加入的锌粉过量,滤液中一定没有AgNO₃和Cu(NO₃)₂,故正确。
10. (宁波中考)将一定量的铜锌混合粉末放入盛有硝酸银溶液的烧杯中,不断搅拌,充分反应后过滤。向得到的滤渣和滤液中分别加入足量的稀盐酸,均无现象,则滤渣中(硝酸银与盐酸能反应生成白色沉淀)( )
A. 一定有银,可能有铜和锌
B. 一定有银,可能有铜,一定没有锌
C. 一定有银和铜,可能有锌
D. 一定有银和铜,一定没有锌
A. 一定有银,可能有铜和锌
B. 一定有银,可能有铜,一定没有锌
C. 一定有银和铜,可能有锌
D. 一定有银和铜,一定没有锌
答案:
B 提示:金属活动性:锌>铜>银,将铜粉和锌粉的混合物放入一定量的硝酸银溶液中时,硝酸银先和锌反应生成硝酸锌和银,当锌完全反应后,硝酸银再和铜反应生成硝酸铜和银。稀盐酸能和锌反应产生氢气,稀盐酸能和硝酸银溶液反应产生白色沉淀,向滤渣和滤液中分别加入足量的稀盐酸,均无现象,说明滤液中不含有硝酸银、滤渣中不含有金属锌,则溶液中硝酸银全部被置换为银,滤渣中一定含有银。溶液中的硝酸银可能和锌恰好完全反应,也可能和铜恰好完全反应,也可能和部分铜反应,则滤渣中可能含有铜。
11. 金属在生产生活中起着重要作用。
(1)对Ag、Mg、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是______(填序号)。①Mg、Ag、CuSO₄溶液 ②Cu、Ag、MgSO₄溶液③Cu、MgSO₄溶液、AgNO₃溶液
(2)化学小组在实验结束后,进行了如下废液处理:

①写出II中一定发生反应的化学方程式:______________________________。
②滤液的组成可能是____________________。
(1)对Ag、Mg、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是______(填序号)。①Mg、Ag、CuSO₄溶液 ②Cu、Ag、MgSO₄溶液③Cu、MgSO₄溶液、AgNO₃溶液
(2)化学小组在实验结束后,进行了如下废液处理:

①写出II中一定发生反应的化学方程式:______________________________。
②滤液的组成可能是____________________。
答案:
(1)②
(2)①Fe + H₂SO₄ = FeSO₄ + H₂↑ ②硫酸锌或硫酸锌和硫酸亚铁
提示:
(1)②因为Mg的活动性在三种金属中最强,所以Cu、Ag都不能和MgSO₄溶液反应,可以得出Cu、Ag的活动性都比Mg弱,但不能比较Cu、Ag的活动性强弱,所以此试剂组不可行;
(2)①铜、铁和锌三种金属的活动性由强到弱的顺序为锌>铁>铜,因此锌先与硫酸铜溶液反应,当硫酸铜溶液反应完,再和硫酸亚铁反应。由题图可知,滤渣能与稀硫酸反应生成气体,说明滤渣中含铁,如果锌过量,则滤渣中含有铜、铁和锌,如果锌不足,则滤渣中只含有铜、铁,因此II中一定发生反应的化学方程式为Fe + H₂SO₄ = FeSO₄ + H₂↑。②如果锌过量,则滤液中只含有硫酸锌,如果锌不足,则滤液中含有硫酸锌和硫酸亚铁。
(1)②
(2)①Fe + H₂SO₄ = FeSO₄ + H₂↑ ②硫酸锌或硫酸锌和硫酸亚铁
提示:
(1)②因为Mg的活动性在三种金属中最强,所以Cu、Ag都不能和MgSO₄溶液反应,可以得出Cu、Ag的活动性都比Mg弱,但不能比较Cu、Ag的活动性强弱,所以此试剂组不可行;
(2)①铜、铁和锌三种金属的活动性由强到弱的顺序为锌>铁>铜,因此锌先与硫酸铜溶液反应,当硫酸铜溶液反应完,再和硫酸亚铁反应。由题图可知,滤渣能与稀硫酸反应生成气体,说明滤渣中含铁,如果锌过量,则滤渣中含有铜、铁和锌,如果锌不足,则滤渣中只含有铜、铁,因此II中一定发生反应的化学方程式为Fe + H₂SO₄ = FeSO₄ + H₂↑。②如果锌过量,则滤液中只含有硫酸锌,如果锌不足,则滤液中含有硫酸锌和硫酸亚铁。
12. 向等质量的锌粉和铁粉中分别加入足量稀硫酸,如图所示图象能正确表示产生的氢气质量与反应时间之间关系的是( )
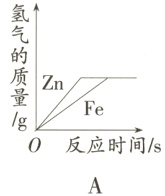
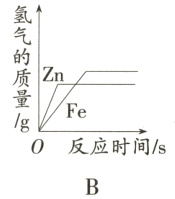
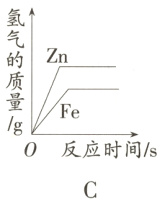





答案:
B 提示:由化学方程式可知,每56份质量的铁能置换出2份质量的氢气,每65份质量的锌也可置换出2份质量的氢气,则等质量的锌和铁分别与足量的稀硫酸反应,铁产生的氢气比锌多,故A、C项错误,又因为铁的金属活动性比锌弱,锌和稀硫酸反应的速率快于铁和稀硫酸反应的速率,故D项错误。
查看更多完整答案,请扫码查看


