2025年全优课堂九年级化学下册
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年全优课堂九年级化学下册 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第77页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
8. 根据如图所示实验,判断以下说法错误的是 ( )
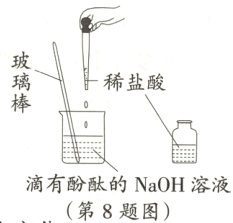
A. 取液后的滴管不能倒置
B. 用玻璃棒搅拌使反应充分
C. 用酚酞溶液判断该反应是否发生
D. 生成盐和水的反应都是中和反应

A. 取液后的滴管不能倒置
B. 用玻璃棒搅拌使反应充分
C. 用酚酞溶液判断该反应是否发生
D. 生成盐和水的反应都是中和反应
答案:
D 提示:酸和碱反应生成盐和水的反应叫中和反应,但是生成盐和水的反应不一定是中和反应,如二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,不属于中和反应,故D项错误。
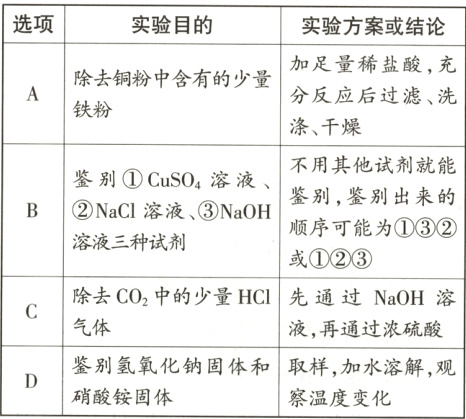
9. 为达到实验目的,如表实验方案或结论不正确的是 ( )

答案:
C 提示:CO₂和HCl气体均能与NaOH溶液反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,C项错误。
10. 如图所示的四个图象,分别对应四种过程,其中正确的是 ( )
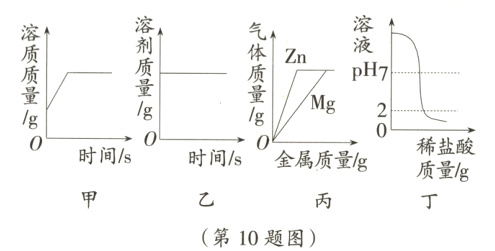
A. 甲:浓盐酸在空气中敞口放置一段时间
B. 乙:将一定量的60℃硝酸钾饱和溶液冷却至室温
C. 丙:向等质量等质量分数的稀硫酸中分别加入足量的镁和锌
D. 丁:向一定量的氢氧化钠溶液中逐滴加入pH = 2的稀盐酸至过量

A. 甲:浓盐酸在空气中敞口放置一段时间
B. 乙:将一定量的60℃硝酸钾饱和溶液冷却至室温
C. 丙:向等质量等质量分数的稀硫酸中分别加入足量的镁和锌
D. 丁:向一定量的氢氧化钠溶液中逐滴加入pH = 2的稀盐酸至过量
答案:
B 提示:浓盐酸具有挥发性,在空气中敞口放置一段时间,溶质质量会减少,A项错误;向等质量等质量分数的稀硫酸中分别加入足量的镁和锌,镁与酸完全反应前,相同质量的金属与酸反应时,镁产生的氢气多,C项错误;向一定量的氢氧化钠溶液中逐滴加入pH = 2的稀盐酸至过量,溶液的pH不可能小于2,D项错误。
11. 金属材料与人类的生产和生活密切相关。请回答下列问题。
(1) 洁净的铁钉在下列情况下容易生锈的是________(填选项字母)。
A. 在干燥的空气中
B. 在潮湿的空气中
C. 浸没在植物油中
(2) 除去铁制品表面的铁锈(主要成分是Fe₂O₃)可用稀盐酸,反应的化学方程式为________。
(3) 向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有________(填化学式,下同),滤液中一定含有的溶质是________。
(1) 洁净的铁钉在下列情况下容易生锈的是________(填选项字母)。
A. 在干燥的空气中
B. 在潮湿的空气中
C. 浸没在植物油中
(2) 除去铁制品表面的铁锈(主要成分是Fe₂O₃)可用稀盐酸,反应的化学方程式为________。
(3) 向硝酸银和硝酸铜的混合溶液中,加入一定量的铁粉,反应停止后过滤,得到滤渣和滤液。向滤渣中滴加稀盐酸,无气泡产生,则滤渣中一定含有________(填化学式,下同),滤液中一定含有的溶质是________。
答案:
(1)B
(2)Fe₂O₃ + 6HCl = 2FeCl₃ + 3H₂O
(3)Ag Fe(NO₃)₂
提示:
(1)铁在与氧气、水同时接触时易发生锈蚀;
(2)盐酸与氧化铁反应生成氯化铁和水,反应的化学方程式为Fe₂O₃ + 6HCl = 2FeCl₃ + 3H₂O;
(3)向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,则铁先与硝酸银反应生成硝酸亚铁和银,可能与硝酸铜反应生成硝酸亚铁和铜,向滤渣中滴加稀盐酸,无气泡产生,说明滤渣中一定不含有铁,且一定含有银,可能含有铜;滤液中一定含有的溶质是硝酸亚铁。
(1)B
(2)Fe₂O₃ + 6HCl = 2FeCl₃ + 3H₂O
(3)Ag Fe(NO₃)₂
提示:
(1)铁在与氧气、水同时接触时易发生锈蚀;
(2)盐酸与氧化铁反应生成氯化铁和水,反应的化学方程式为Fe₂O₃ + 6HCl = 2FeCl₃ + 3H₂O;
(3)向硝酸银和硝酸铜的混合溶液中加入一定量的铁粉,则铁先与硝酸银反应生成硝酸亚铁和银,可能与硝酸铜反应生成硝酸亚铁和铜,向滤渣中滴加稀盐酸,无气泡产生,说明滤渣中一定不含有铁,且一定含有银,可能含有铜;滤液中一定含有的溶质是硝酸亚铁。
12. 某同学配制100g溶质质量分数为0.9%的NaCl溶液,准备了下列实验用品。
(1) 该同学按下列实验步骤进行:①计算,②称量,③量取,④________。
(2) 配制过程还缺少一种玻璃仪器是________,用来量取所需的水(水的密度为1g/cm³),量筒的规格是________(选填“10mL”“50mL”或“100mL”)。
(3) 计算所需NaCl的质量为________g。

(1) 该同学按下列实验步骤进行:①计算,②称量,③量取,④________。
(2) 配制过程还缺少一种玻璃仪器是________,用来量取所需的水(水的密度为1g/cm³),量筒的规格是________(选填“10mL”“50mL”或“100mL”)。
(3) 计算所需NaCl的质量为________g。

答案:
(1)溶解
(2)玻璃棒
(3)0.9 100mL
提示:
(1)配制100g溶质质量分数为0.9%的NaCl溶液,首先计算配制溶液所需NaCl和水的质量,再称量所需的NaCl和量取水,最后进行溶解;
(2)称量所需的NaCl和量取水时需要用到的仪器为托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,故配制过程还缺少的一种玻璃仪器是玻璃棒;
(3)溶质质量 = 溶液质量×溶质的质量分数,配制100g溶质质量分数为0.9%的NaCl溶液,需氯化钠的质量 = 100g×0.9% = 0.9g;溶剂质量 = 溶液质量 - 溶质质量,则所需水的质量 = 100g - 0.9g = 99.1g(合99.1mL),应用规格为100mL的量筒量取水的体积。
(1)溶解
(2)玻璃棒
(3)0.9 100mL
提示:
(1)配制100g溶质质量分数为0.9%的NaCl溶液,首先计算配制溶液所需NaCl和水的质量,再称量所需的NaCl和量取水,最后进行溶解;
(2)称量所需的NaCl和量取水时需要用到的仪器为托盘天平、药匙、量筒、胶头滴管、烧杯和玻璃棒,故配制过程还缺少的一种玻璃仪器是玻璃棒;
(3)溶质质量 = 溶液质量×溶质的质量分数,配制100g溶质质量分数为0.9%的NaCl溶液,需氯化钠的质量 = 100g×0.9% = 0.9g;溶剂质量 = 溶液质量 - 溶质质量,则所需水的质量 = 100g - 0.9g = 99.1g(合99.1mL),应用规格为100mL的量筒量取水的体积。
13. A~G是初中化学常见的物质,已知A、D、F均为单质,其中D是日常生产生活中使用最多的金属,B是一种氧化物,C是一种常见的酸,E(相对分子质量为160)的水溶液呈蓝色,它们相互转化关系如图所示(部分生成物和反应条件已略去)。试回答下列问题。

(1) 写出B的化学式________________。
(2) A在生产生活中的一种用途是________________。
(3) 反应③的化学方程式为______________________________;图中所涉及的反应中,与③同属于置换反应的是________(填序号)。

(1) 写出B的化学式________________。
(2) A在生产生活中的一种用途是________________。
(3) 反应③的化学方程式为______________________________;图中所涉及的反应中,与③同属于置换反应的是________(填序号)。
答案:
(1)CuO
(2)冶炼金属(合理即可)
(3)Fe + CuSO₄ = FeSO₄ + Cu ①
提示:A~G是初中化学常见的物质,已知A、D、F均为单质,其中D是日常生产生活中使用最多的金属,所以D为铁;E(相对分子质量为160)的水溶液呈蓝色,所以E为硫酸铜;B(氧化物)和C(一种常见的酸)反应生成E(CuSO₄),则B为氧化铜,C为硫酸;G通电会生成A,A会与B(氧化铜)反应生成F(单质)和G,所以G为水,A为氢气,F为铜,经过验证,推导正确。
(1)B为氧化铜,化学式为CuO;
(2)A为氢气,氢气在生产生活中的用途为冶炼金属、作燃料等;
(3)反应③是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为Fe + CuSO₄ = FeSO₄ + Cu;①是氢气和氧化铜的反应,属于置换反应,②是氧化铜和硫酸的反应,不属于置换反应,所以图中所涉及的反应中,与③同属于置换反应的是①。
(1)CuO
(2)冶炼金属(合理即可)
(3)Fe + CuSO₄ = FeSO₄ + Cu ①
提示:A~G是初中化学常见的物质,已知A、D、F均为单质,其中D是日常生产生活中使用最多的金属,所以D为铁;E(相对分子质量为160)的水溶液呈蓝色,所以E为硫酸铜;B(氧化物)和C(一种常见的酸)反应生成E(CuSO₄),则B为氧化铜,C为硫酸;G通电会生成A,A会与B(氧化铜)反应生成F(单质)和G,所以G为水,A为氢气,F为铜,经过验证,推导正确。
(1)B为氧化铜,化学式为CuO;
(2)A为氢气,氢气在生产生活中的用途为冶炼金属、作燃料等;
(3)反应③是铁和硫酸铜反应生成硫酸亚铁和铜,化学方程式为Fe + CuSO₄ = FeSO₄ + Cu;①是氢气和氧化铜的反应,属于置换反应,②是氧化铜和硫酸的反应,不属于置换反应,所以图中所涉及的反应中,与③同属于置换反应的是①。
查看更多完整答案,请扫码查看


