2025年全优课堂九年级化学下册
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年全优课堂九年级化学下册 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第20页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
1.下列有关金属的说法正确的是( )
A.金属都是坚硬的固体
B.夏商时期的青铜器属于合金
C.金属的颜色都是银白色的
D.合金不属于金属材料
A.金属都是坚硬的固体
B.夏商时期的青铜器属于合金
C.金属的颜色都是银白色的
D.合金不属于金属材料
答案:
B 提示:金属不一定都是坚硬的固体,如汞在常温下是液体,A项错误;金属的颜色不一定都是银白色的,如铜呈紫红色,C项错误;金属材料包括纯金属以及它们的合金,合金属于金属材料,D项错误。
2.下列金属中,只能与硝酸银反应,不能与稀硫酸反应的是( )
A.镁
B.铁
C.铜
D.锌
A.镁
B.铁
C.铜
D.锌
答案:
C 提示:金属活动性顺序中,镁、银、铜、铁、锌的活动性顺序为镁>锌>铁>氢>铜>银,只能与硝酸银溶液反应,不能与稀硫酸反应,说明该金属活动性顺序在氢后,在银前,故为铜。
3.用化学方法制高纯硅的反应原理为
①2C + SiO₂$\stackrel{高温}{=\!=\!=}$2CO↑ + Si(粗硅)
②Si + 2Cl₂$\stackrel{加热}{=\!=\!=}$SiCl₄(液态)
③2H₂ + SiCl₄$\stackrel{高温}{=\!=\!=}$4HCl + Si(高纯硅)
其中属于置换反应的是( )
A.①
B.①②
C.②③
D.①③
①2C + SiO₂$\stackrel{高温}{=\!=\!=}$2CO↑ + Si(粗硅)
②Si + 2Cl₂$\stackrel{加热}{=\!=\!=}$SiCl₄(液态)
③2H₂ + SiCl₄$\stackrel{高温}{=\!=\!=}$4HCl + Si(高纯硅)
其中属于置换反应的是( )
A.①
B.①②
C.②③
D.①③
答案:
D 提示:②Si + 2Cl₂$\stackrel{加热}{=\!=\!=}$SiCl₄,该反应符合“多变一”的形式,符合化合反应的特征,属于化合反应,故D项符合题意。
4.下列有关说法正确的是( )
A.铁在潮湿的环境中比在干燥的环境中更容易生锈
B.铝制品不用涂任何保护层来防腐,因为铝不与空气反应
C.“真金不怕火炼”说明黄金的硬度非常大
D.我国的矿物储量比较丰富,所以废旧金属直接扔掉,没有必要回收
A.铁在潮湿的环境中比在干燥的环境中更容易生锈
B.铝制品不用涂任何保护层来防腐,因为铝不与空气反应
C.“真金不怕火炼”说明黄金的硬度非常大
D.我国的矿物储量比较丰富,所以废旧金属直接扔掉,没有必要回收
答案:
A 提示:常温下,铝易与空气中的氧气反应生成致密的氧化物膜,可阻止金属进一步被腐蚀,B项错误;“真金不怕火炼”说明黄金的化学性质不活泼,在高温下也不易反应,C项错误;废旧金属的回收利用可以保护环境和节约金属资源,D项错误。
5.有A、B两种金属放入等浓度的稀硫酸中,生成氢气的质量与反应时间的关系如图所示,下列结论合理的是( )
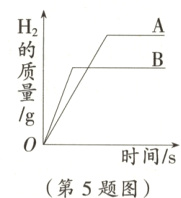
A.金属活动性A>B
B.生成氢气的质量A>B
C.反应的硫酸质量A<B
D.反应的金属质量A<B

A.金属活动性A>B
B.生成氢气的质量A>B
C.反应的硫酸质量A<B
D.反应的金属质量A<B
答案:
B 提示:刚开始相同时间内B放出氢气的质量大于A,可判断金属活动性顺序是B>A,故A项错误;金属与酸反应生成氢气时,氢气来源于酸中的氢元素,所以生成的氢气的质量与消耗的酸的多少顺序一致,由题图可知,生成氢气的质量A>B,所以消耗硫酸的质量A>B,故C项错误;金属的相对原子质量不确定,所以不能确定参加反应的金属的质量,故D项错误。
6.为探究锌、铜、铁三种金属的活动性顺序,某学习小组做了如图甲所示实验。实验结束后,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多(如图乙所示),下列说法正确的是( )

A.反应后烧杯中的固体一定含有铁
B.甲图试管②中反应后固体一定不含铁
C.反应后烧杯中的溶液一定不含有氯化铜
D.烧杯中最后所得固体的质量一定小于2ag

A.反应后烧杯中的固体一定含有铁
B.甲图试管②中反应后固体一定不含铁
C.反应后烧杯中的溶液一定不含有氯化铜
D.烧杯中最后所得固体的质量一定小于2ag
答案:
B 提示:三种金属的活动性由强到弱的顺序是锌、铁、铜,所以铁不会与氯化锌反应,铁会置换出氯化铜中的铜,将试管①、试管②内的物质全部倒入同一烧杯中,充分反应后发现烧杯中的红色固体物质明显增多,说明铁又置换出氯化铜中的铜,所以通过上面的分析可知,铁会置换出氯化铜中的铜,但是氯化铜的量不能确定,所以反应后烧杯中的溶液是否含有氯化铜,反应后烧杯中的固体中是否含铁,不能确定,故A、C项错误;通过题中的分析可知,加入铁的质量是2ag,每56份质量的铁会置换出64份质量的铜,所以反应后固体的质量一定大于2ag,故D项错误。
7.随着人们生活水平的不断提高,汽车已走进千家万户。制造汽车要用到含铜、铁、铝等成分的多种金属材料。
(1)在汽车电路中,经常用铜作导线,这是利用了铜的________性。
(2)车体多用钢材制造且要对其表面进行喷漆处理,这样不仅美观,而且可有效防止钢材与________________(填名称)接触而生锈。汽车使用的金属材料多为合金,是因为合金与纯金属相比,具有________________________(填一条)等优良性能。
(1)在汽车电路中,经常用铜作导线,这是利用了铜的________性。
(2)车体多用钢材制造且要对其表面进行喷漆处理,这样不仅美观,而且可有效防止钢材与________________(填名称)接触而生锈。汽车使用的金属材料多为合金,是因为合金与纯金属相比,具有________________________(填一条)等优良性能。
答案:
(1)导电
(2)氧气(或空气) 水(或水蒸气) 硬度更大(或抗腐蚀性更强等)
提示:
(1)汽车电路中的导线一般是用铜做的,这是利用了铜的导电性;
(2)表面喷漆能使铁与水和氧气隔绝,从而防止铁生锈;与组成合金的纯金属相比,合金的优点一般有硬度更大,抗腐蚀性更好等优良性能。
(1)导电
(2)氧气(或空气) 水(或水蒸气) 硬度更大(或抗腐蚀性更强等)
提示:
(1)汽车电路中的导线一般是用铜做的,这是利用了铜的导电性;
(2)表面喷漆能使铁与水和氧气隔绝,从而防止铁生锈;与组成合金的纯金属相比,合金的优点一般有硬度更大,抗腐蚀性更好等优良性能。
8.铬是最硬的金属,常镀在金属制品如水龙头的表面,使金属制品美观耐用。若将打磨过的相同大小、形状的铬片、铝片和铜片分别置于等质量、等浓度的稀硫酸中,观察到铬片表面缓慢产生气泡,铝片表面迅速产生较多气泡,铜片表面无现象。则铬、铝、铜金属活动性由强到弱的顺序是____________________。
如图所示为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题。

(1)描述A中的实验现象:____________________。
(2)写出C中反应的化学方程式:__________。
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是__________(填字母)。
如图所示为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题。

(1)描述A中的实验现象:____________________。
(2)写出C中反应的化学方程式:__________。
(3)要证明Cu、Fe、Ag的活动性顺序,至少要做的实验是__________(填字母)。
答案:
Al>Cr>Cu
(1)铜丝表面附着一层银白色固体,溶液变为蓝色
(2)Zn + 2HCl = ZnCl₂ + H₂↑
(3)A、B
提示:将打磨的相同大小、形状的铬片、铝片和铜片分别置于等浓度的稀硫酸中,观察到铬片表面缓慢产生气泡,铝片表面迅速产生较多气泡,铜片表面无现象,说明三种金属中铝的活动性最强,铬其次,铜的活动性最弱;
(1)由于在金属活动性顺序中铜>银,所以铜可以置换出银,并生成蓝色的硫酸铜溶液,所以其现象是铜丝表面附着一层银白色固体,溶液变为蓝色;
(2)C中是锌与稀盐酸的反应,其反应的化学方程式为Zn + 2HCl = ZnCl₂ + H₂↑;
(3)由A知铜能置换出硝酸银中的银,说明活动性:铜>银,B中的铁能置换出硫酸铜中的铜,说明活动性:铁>铜,所以可得活动性:铁>铜>银
(1)铜丝表面附着一层银白色固体,溶液变为蓝色
(2)Zn + 2HCl = ZnCl₂ + H₂↑
(3)A、B
提示:将打磨的相同大小、形状的铬片、铝片和铜片分别置于等浓度的稀硫酸中,观察到铬片表面缓慢产生气泡,铝片表面迅速产生较多气泡,铜片表面无现象,说明三种金属中铝的活动性最强,铬其次,铜的活动性最弱;
(1)由于在金属活动性顺序中铜>银,所以铜可以置换出银,并生成蓝色的硫酸铜溶液,所以其现象是铜丝表面附着一层银白色固体,溶液变为蓝色;
(2)C中是锌与稀盐酸的反应,其反应的化学方程式为Zn + 2HCl = ZnCl₂ + H₂↑;
(3)由A知铜能置换出硝酸银中的银,说明活动性:铜>银,B中的铁能置换出硫酸铜中的铜,说明活动性:铁>铜,所以可得活动性:铁>铜>银
查看更多完整答案,请扫码查看


