2025年赢在微点轻松课堂微讲小本高中化学选择性必修1
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年赢在微点轻松课堂微讲小本高中化学选择性必修1 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第25页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
【变式训练】
3. 碳酸二甲酯 是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
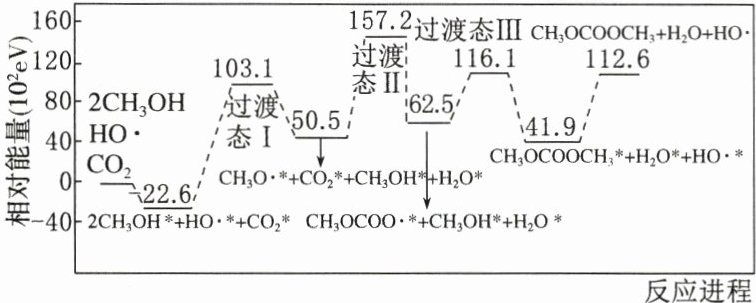
下列说法错误的是 ( )
A. $HO\cdot$降低了反应的活化能
B. 过程$CH_{3}OH^{*}+HO\cdot^{*}=CH_{3}O\cdot^{*}+H_{2}O^{*}$是该反应的决速步骤
C. 过程中既有$H - O$键的断裂,又有$H - O$键的形成
D. 吸附和脱附过程中共吸收 48.1 eV 的能量
3. 碳酸二甲酯
 是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
是一种低毒、性能优良的有机合成中间体,科学家提出了新的合成方案(吸附在催化剂表面上的物种用*标注),反应机理如图所示。
下列说法错误的是 ( )
A. $HO\cdot$降低了反应的活化能
B. 过程$CH_{3}OH^{*}+HO\cdot^{*}=CH_{3}O\cdot^{*}+H_{2}O^{*}$是该反应的决速步骤
C. 过程中既有$H - O$键的断裂,又有$H - O$键的形成
D. 吸附和脱附过程中共吸收 48.1 eV 的能量
答案:
D@@解析 HO·在反应前参与反应,反应后又生成,作催化剂,降低了反应的活化能,提高化学反应速率,A项正确;活化能大的步骤即决速步骤,由图示可知生成过渡态Ⅰ时所需的活化能最大,所以CH₃OH⁺ + HO· == CH₃O·⁺ + H₂O⁺是该反应的决速步骤,B项正确;过程中甲醇反应时有H - O键的断裂,生成水时有H - O键的形成,C项正确;吸附和脱附过程中共吸收的能量为终态减去始态的能量,始态相对能量为0 eV,终态相对能量为112.6×10² eV,则吸附和脱附过程中共吸收的能量为1.126×10⁴ eV,D项错误。
1. 用 3 g 块状大理石与 30 mL 3 mol·L⁻¹ 盐酸反应制取 CO₂ 气体,若要增大反应速率,可采取的措施是 ( )
①再加入 30 mL 3 mol·L⁻¹ 盐酸 ②改用 30 mL 6 mol·L⁻¹ 盐酸 ③改用 3 g 粉末状大理石 ④适当升高温度
A. ①②④
B. ②③④
C. ①③④
D. ①②③
①再加入 30 mL 3 mol·L⁻¹ 盐酸 ②改用 30 mL 6 mol·L⁻¹ 盐酸 ③改用 3 g 粉末状大理石 ④适当升高温度
A. ①②④
B. ②③④
C. ①③④
D. ①②③
答案:
B 解析:影响反应速率快慢的因素除浓度、温度、压强(对于有气体参加的反应)之外,其他因素还有固体反应物表面积、光、超声波等。
2. 下列化学反应的速率,前者一定大于后者的是 ( )
A. 相同温度下,颗粒大小相同的锌粒分别与 pH 相同的硫酸和盐酸反应
B. A + B$\xrightarrow{500\ ^{\circ}C}$C,D + E$\xrightarrow{100\ ^{\circ}C}$F
C. 相同温度下,与同浓度盐酸反应的锌粒和铁粉
D. G + H$\longrightarrow$W + Q,其他条件相同时分别在 200 °C 和 100 °C 时反应
A. 相同温度下,颗粒大小相同的锌粒分别与 pH 相同的硫酸和盐酸反应
B. A + B$\xrightarrow{500\ ^{\circ}C}$C,D + E$\xrightarrow{100\ ^{\circ}C}$F
C. 相同温度下,与同浓度盐酸反应的锌粒和铁粉
D. G + H$\longrightarrow$W + Q,其他条件相同时分别在 200 °C 和 100 °C 时反应
答案:
D 解析:相同温度下,颗粒大小相同的锌粒分别与pH相同的硫酸和盐酸反应,接触面积相等,氢离子浓度相同,反应速率基本相等,A项错误;A + B$\xrightarrow{500^{\circ}C}$C和D + E$\xrightarrow{100^{\circ}C}$F的反应不同,无法比较反应速率的快慢,B项错误;锌比铁活泼,但接触面积铁粉大,因此反应速率无法判断,C项错误;对于同一个化学反应,其他条件相同时,温度越高,反应速率越快,D项正确。
查看更多完整答案,请扫码查看


