第119页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
2.在一个密闭容器中加入甲、乙、丙、丁四种物质,测得反应前后各物质的质量如下表。
|物质|甲|乙|丙|丁|
|反应前的质量/g|40|40|10|32|
|反应后的质量/g|12|待测|10|0|
下列说法正确的是(
A.该反应中生成乙物质的质量为100 g
B.乙可能是化合物
C.在该反应中丙一定是催化剂
D.该反应中参加反应的甲与丁的质量比为7∶8
|物质|甲|乙|丙|丁|
|反应前的质量/g|40|40|10|32|
|反应后的质量/g|12|待测|10|0|

下列说法正确的是(
BD
)。A.该反应中生成乙物质的质量为100 g
B.乙可能是化合物
C.在该反应中丙一定是催化剂
D.该反应中参加反应的甲与丁的质量比为7∶8
答案:
解:根据质量守恒定律,反应前后物质总质量相等。
反应前总质量:40g + 40g + 10g + 32g = 122g
反应后总质量:12g + 待测 + 10g + 0g = 122g,解得待测 = 100g
A. 生成乙的质量 = 100g - 40g = 60g,A错误;
B. 甲、丁质量减少为反应物,乙质量增加为生成物,该反应为化合反应,乙一定是化合物,B正确;
C. 丙质量不变,可能是催化剂或杂质,C错误;
D. 参加反应的甲质量 = 40g - 12g = 28g,参加反应的丁质量 = 32g - 0g = 32g,甲与丁质量比 = 28g:32g = 7:8,D正确。
答案:BD
反应前总质量:40g + 40g + 10g + 32g = 122g
反应后总质量:12g + 待测 + 10g + 0g = 122g,解得待测 = 100g
A. 生成乙的质量 = 100g - 40g = 60g,A错误;
B. 甲、丁质量减少为反应物,乙质量增加为生成物,该反应为化合反应,乙一定是化合物,B正确;
C. 丙质量不变,可能是催化剂或杂质,C错误;
D. 参加反应的甲质量 = 40g - 12g = 28g,参加反应的丁质量 = 32g - 0g = 32g,甲与丁质量比 = 28g:32g = 7:8,D正确。
答案:BD
3.aNH_3+bO_2$\frac{\underline{\;一定条件\;}}{}$4X+dH_2O是工业上制取硝酸的关键反应。34 g NH_3与一定质量的O_2反应时,NH_3、H_2O的质量随消耗O_2质量的变化如图。 下列说法错误的是( )
下列说法错误的是( )
$A.80g O_2$参加反应时,生成X的质量为60g
B.化学方程式中a和d的比为2∶3
C.化学计量数b= 5
D.X为$NO_2$
 下列说法错误的是( )
下列说法错误的是( )D
。$A.80g O_2$参加反应时,生成X的质量为60g
B.化学方程式中a和d的比为2∶3
C.化学计量数b= 5
D.X为$NO_2$
答案:
【解析】:
选项A:根据图像可知,当消耗$70g$氧气时,氨气完全反应,设氨气与氧气反应的化学方程式为$aNH_{3} + bO_{2}\xlongequal{一定条件}4X + dH_{2}O$,$34g$氨气中氮元素的质量为$34g×\frac{14}{14 + 1×3}=28g$,氢元素的质量为$34g - 28g = 6g$,生成水中氢元素的质量为$54g×\frac{1×2}{1×2 + 16}=6g$,说明$X$中不含氢元素,$X$中氮元素质量为$28g$,氧元素质量为$70g - 54g + 34g - 34g = 16g$(根据质量守恒定律),则$X$中氮、氧原子个数比为$\frac{28g}{14}:\frac{16g}{16}=2:1$,所以$X$为$NO$,化学方程式为$4NH_{3} + 5O_{2}\xlongequal{一定条件}4NO + 6H_{2}O$。当$80g$氧气参加反应时,设生成$NO$的质量为$x$,$\begin{matrix}&4NH_{3} + &5O_{2}\xlongequal{一定条件}&4NO + &6H_{2}O\\&&160&120\\&&80g&x\end{matrix}$,$\frac{160}{120}=\frac{80g}{x}$,解得$x = 60g$,故A选项正确。
选项B:由化学方程式$4NH_{3} + 5O_{2}\xlongequal{一定条件}4NO + 6H_{2}O$可知,$a = 4$,$d = 6$,$a:d = 4:6 = 2:3$,故B选项正确。
选项C:由化学方程式$4NH_{3} + 5O_{2}\xlongequal{一定条件}4NO + 6H_{2}O$可知,$b = 5$,故C选项正确。
选项D:由前面分析可知$X$为$NO$,不是$NO_{2}$,故D选项错误。
【答案】:D
选项A:根据图像可知,当消耗$70g$氧气时,氨气完全反应,设氨气与氧气反应的化学方程式为$aNH_{3} + bO_{2}\xlongequal{一定条件}4X + dH_{2}O$,$34g$氨气中氮元素的质量为$34g×\frac{14}{14 + 1×3}=28g$,氢元素的质量为$34g - 28g = 6g$,生成水中氢元素的质量为$54g×\frac{1×2}{1×2 + 16}=6g$,说明$X$中不含氢元素,$X$中氮元素质量为$28g$,氧元素质量为$70g - 54g + 34g - 34g = 16g$(根据质量守恒定律),则$X$中氮、氧原子个数比为$\frac{28g}{14}:\frac{16g}{16}=2:1$,所以$X$为$NO$,化学方程式为$4NH_{3} + 5O_{2}\xlongequal{一定条件}4NO + 6H_{2}O$。当$80g$氧气参加反应时,设生成$NO$的质量为$x$,$\begin{matrix}&4NH_{3} + &5O_{2}\xlongequal{一定条件}&4NO + &6H_{2}O\\&&160&120\\&&80g&x\end{matrix}$,$\frac{160}{120}=\frac{80g}{x}$,解得$x = 60g$,故A选项正确。
选项B:由化学方程式$4NH_{3} + 5O_{2}\xlongequal{一定条件}4NO + 6H_{2}O$可知,$a = 4$,$d = 6$,$a:d = 4:6 = 2:3$,故B选项正确。
选项C:由化学方程式$4NH_{3} + 5O_{2}\xlongequal{一定条件}4NO + 6H_{2}O$可知,$b = 5$,故C选项正确。
选项D:由前面分析可知$X$为$NO$,不是$NO_{2}$,故D选项错误。
【答案】:D
4.甲、乙、丙、丁四种物质在一定条件下反应,测得反应前后各物质的质量分数如图所示, 则下列有关说法中正确的是(
则下列有关说法中正确的是(
A.该反应为分解反应
B.甲可能是单质
C.丙、丁两物质变化的质量比为9∶10
D.乙一定是这个反应的催化剂
 则下列有关说法中正确的是(
则下列有关说法中正确的是(B
)。A.该反应为分解反应
B.甲可能是单质
C.丙、丁两物质变化的质量比为9∶10
D.乙一定是这个反应的催化剂
答案:
【解析】:
由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了$14\%-6\%=8\%$,故甲是反应物;反应前乙的质量分数为$10\%$,反应后乙的质量分数也是$10\%$,乙的质量分数不变,故乙可能是该反应的催化剂,也可能没有参加反应;反应后丙的质量分数增加了$36\%-25\%=11\%$,丙是生成物;丁的质量分数减少了$48\%-40\%=8\%$,丁是反应物。故该反应可表示为甲+丁→丙。
A选项:该反应的反应物是甲和丁,生成物是丙,符合“多变一”的特征,属于化合反应,不是分解反应,故A错误。
B选项:甲是化合反应的反应物,可能是单质,也可能是化合物,故B正确。
C选项:丙、丁两物质变化的质量比为$11\%:8\%=11:8$,不是$9:10$,故C错误。
D选项:乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,故D错误。
【答案】:B
由四种物质反应前后各物质的质量分数可知,反应前后甲的质量分数减少了$14\%-6\%=8\%$,故甲是反应物;反应前乙的质量分数为$10\%$,反应后乙的质量分数也是$10\%$,乙的质量分数不变,故乙可能是该反应的催化剂,也可能没有参加反应;反应后丙的质量分数增加了$36\%-25\%=11\%$,丙是生成物;丁的质量分数减少了$48\%-40\%=8\%$,丁是反应物。故该反应可表示为甲+丁→丙。
A选项:该反应的反应物是甲和丁,生成物是丙,符合“多变一”的特征,属于化合反应,不是分解反应,故A错误。
B选项:甲是化合反应的反应物,可能是单质,也可能是化合物,故B正确。
C选项:丙、丁两物质变化的质量比为$11\%:8\%=11:8$,不是$9:10$,故C错误。
D选项:乙的质量分数不变,可能作该反应的催化剂,也可能没有参加反应,故D错误。
【答案】:B
5.在密闭容器中放入甲、乙、丙、丁四种物质,一定条件下发生化学反应,一段时间后,测得相关数据如图所示。 下列说法正确的是(
下列说法正确的是(
A.x= 3.1
B.该反应中甲、丁的质量变化比为14∶85
C.该反应属于分解反应
D.乙一定是该反应的催化剂
 下列说法正确的是(
下列说法正确的是(AB
)。A.x= 3.1
B.该反应中甲、丁的质量变化比为14∶85
C.该反应属于分解反应
D.乙一定是该反应的催化剂
答案:
解:根据质量守恒定律,反应前后总质量相等。
反应前总质量:10 + 3.5 + 10 + 6 = 29.5
反应后总质量:8.6 + 3.5 + x + 14.5 = 29.5,解得x = 3.1。
甲质量变化:10 - 8.6 = 1.4(减少)
丁质量变化:14.5 - 6 = 8.5(增加)
甲、丁质量变化比:1.4∶8.5 = 14∶85。
乙质量不变,可能是催化剂或杂质;丙质量减少,甲、丙为反应物,丁为生成物,反应为化合反应。
答案:AB
反应前总质量:10 + 3.5 + 10 + 6 = 29.5
反应后总质量:8.6 + 3.5 + x + 14.5 = 29.5,解得x = 3.1。
甲质量变化:10 - 8.6 = 1.4(减少)
丁质量变化:14.5 - 6 = 8.5(增加)
甲、丁质量变化比:1.4∶8.5 = 14∶85。
乙质量不变,可能是催化剂或杂质;丙质量减少,甲、丙为反应物,丁为生成物,反应为化合反应。
答案:AB
6.在宏观、微观和符号之间建立联系,是化学学科的特点。如图是某化学反应的微观过程示意图(“●”表示氢原子,“○”表示氧原子)。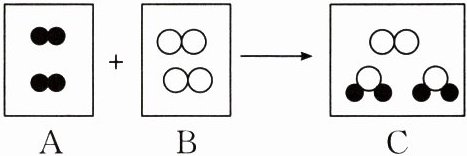
(1)从宏观角度看,物质C属于______
(2)从微观角度看,物质B是由______
(3)从反应类型看,该反应是______

(1)从宏观角度看,物质C属于______
混合物
(填“混合物”或“纯净物”)。(2)从微观角度看,物质B是由______
分子
(填“分子”“原子”或“离子”)构成的,参加反应的A与B的粒子个数比为______2:1
。(3)从反应类型看,该反应是______
化合反应
。
答案:
【解析】
(1) 从宏观角度看,物质C由两种物质组成(由图可知,C中有水分子和未反应的氧分子),属于混合物。
(2) 从微观角度看,物质B是氧气,由氧分子构成。由图可知,参加反应的A(氢分子)与B(氧分子)的微粒个数比为$2:1$。
(3) 该反应是氢气和氧气反应生成水,由两种物质反应生成一种物质,属于化合反应。
【答案】
(1) 混合物
(2) 分子;$2:1$
(3) 化合反应
(1) 从宏观角度看,物质C由两种物质组成(由图可知,C中有水分子和未反应的氧分子),属于混合物。
(2) 从微观角度看,物质B是氧气,由氧分子构成。由图可知,参加反应的A(氢分子)与B(氧分子)的微粒个数比为$2:1$。
(3) 该反应是氢气和氧气反应生成水,由两种物质反应生成一种物质,属于化合反应。
【答案】
(1) 混合物
(2) 分子;$2:1$
(3) 化合反应
7.观察、比较与归纳是学习化学的重要方法,对于以下三个化学方程式:
2Mg+O₂$\frac{\underline{\;点燃\;}}{}$2MgO;2H₂+O₂$\frac{\underline{\;点燃\;}}{}$2H₂O;2CO+O₂$\frac{\underline{\;点燃\;}}{}$2CO₂。
(1)通过比较,发现它们有许多共同点,请你写出其中的两点:①
(2)以上化学方程式也有许多不同之处,请你写出其中一个与另外两个的一点不同之处:
2Mg+O₂$\frac{\underline{\;点燃\;}}{}$2MgO;2H₂+O₂$\frac{\underline{\;点燃\;}}{}$2H₂O;2CO+O₂$\frac{\underline{\;点燃\;}}{}$2CO₂。
(1)通过比较,发现它们有许多共同点,请你写出其中的两点:①
都是化合反应
;②生成物都是氧化物(或 反应条件都是点燃;或 反应中都有元素化合价的变化等,合理即可)
。(2)以上化学方程式也有许多不同之处,请你写出其中一个与另外两个的一点不同之处:
第一个反应的反应物中有固体,而另外两个反应的反应物都是气体(或 第一个反应的生成物是固体,而另外两个反应的生成物中既有固体也有液体等,合理即可)
。
答案:
【解析】:
(1)对于给出的三个化学方程式,我们可以从反应物、生成物、反应条件以及元素化合价的变化等方面进行比较。
首先,观察反应物,可以发现它们都是两种物质反应生成一种物质,这符合化合反应的特征,即“多变一”。
其次,从生成物来看,它们都是氧化物,说明这些反应都涉及到了氧元素与其他元素的结合。
再次,从反应条件来看,这三个反应都需要点燃才能发生,因此反应条件相同。
最后,从元素化合价的变化来看,反应物中的镁、氢、一氧化碳在反应后都变成了正二价或正四价的离子,说明它们的化合价在反应中都发生了变化。
综合以上分析,我们可以得出其中的两点共同点为:①都是化合反应;②生成物都是氧化物(或反应条件都是点燃;或反应中都有元素化合价的变化等,合理即可)。
(2)对于这三个化学方程式的不同之处,我们可以从反应物的种类、状态以及生成物的性质等方面进行比较。
观察反应物,可以发现镁是固体,氢气和一氧化碳是气体,因此其中一个与另外两个的一点不同之处可以是:第一个反应的反应物中有固体,而另外两个反应的反应物都是气体(或第一个反应的生成物是固体,而另外两个反应的生成物中既有固体也有液体等,合理即可)。
【答案】:
(1)①都是化合反应;②生成物都是氧化物(或 反应条件都是点燃;或 反应中都有元素化合价的变化等,合理即可);
(2)第一个反应的反应物中有固体,而另外两个反应的反应物都是气体(或 第一个反应的生成物是固体,而另外两个反应的生成物中既有固体也有液体等,合理即可)。
(1)对于给出的三个化学方程式,我们可以从反应物、生成物、反应条件以及元素化合价的变化等方面进行比较。
首先,观察反应物,可以发现它们都是两种物质反应生成一种物质,这符合化合反应的特征,即“多变一”。
其次,从生成物来看,它们都是氧化物,说明这些反应都涉及到了氧元素与其他元素的结合。
再次,从反应条件来看,这三个反应都需要点燃才能发生,因此反应条件相同。
最后,从元素化合价的变化来看,反应物中的镁、氢、一氧化碳在反应后都变成了正二价或正四价的离子,说明它们的化合价在反应中都发生了变化。
综合以上分析,我们可以得出其中的两点共同点为:①都是化合反应;②生成物都是氧化物(或反应条件都是点燃;或反应中都有元素化合价的变化等,合理即可)。
(2)对于这三个化学方程式的不同之处,我们可以从反应物的种类、状态以及生成物的性质等方面进行比较。
观察反应物,可以发现镁是固体,氢气和一氧化碳是气体,因此其中一个与另外两个的一点不同之处可以是:第一个反应的反应物中有固体,而另外两个反应的反应物都是气体(或第一个反应的生成物是固体,而另外两个反应的生成物中既有固体也有液体等,合理即可)。
【答案】:
(1)①都是化合反应;②生成物都是氧化物(或 反应条件都是点燃;或 反应中都有元素化合价的变化等,合理即可);
(2)第一个反应的反应物中有固体,而另外两个反应的反应物都是气体(或 第一个反应的生成物是固体,而另外两个反应的生成物中既有固体也有液体等,合理即可)。
查看更多完整答案,请扫码查看


