第100页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
5. 某物质的分子模型如图所示。下列说法错误的是(
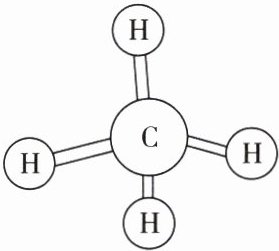
A.该物质属于化合物
B.该物质的化学式为$CH_4$
C.相对分子质量为16
D.该物质由1个碳原子和4个氢原子构成
D
)。
A.该物质属于化合物
B.该物质的化学式为$CH_4$
C.相对分子质量为16
D.该物质由1个碳原子和4个氢原子构成
答案:
【解析】:
A选项:该物质由碳元素和氢元素组成,是两种元素组成的纯净物,属于化合物,故A选项正确。
B选项:从分子模型可知,一个分子中有1个碳原子和4个氢原子,所以化学式为$CH_{4}$,故B选项正确。
C选项:根据相对分子质量的计算方法,$CH_{4}$的相对分子质量为$12 + 1×4 = 16$,故C选项正确。
D选项:应该说一个该物质分子由1个碳原子和4个氢原子构成,而不能说该物质由1个碳原子和4个氢原子构成,故D选项错误。
【答案】:D
A选项:该物质由碳元素和氢元素组成,是两种元素组成的纯净物,属于化合物,故A选项正确。
B选项:从分子模型可知,一个分子中有1个碳原子和4个氢原子,所以化学式为$CH_{4}$,故B选项正确。
C选项:根据相对分子质量的计算方法,$CH_{4}$的相对分子质量为$12 + 1×4 = 16$,故C选项正确。
D选项:应该说一个该物质分子由1个碳原子和4个氢原子构成,而不能说该物质由1个碳原子和4个氢原子构成,故D选项错误。
【答案】:D
6. 如图是某有机酸分子的微观结构示意图。下列关于该物质的描述正确的是(
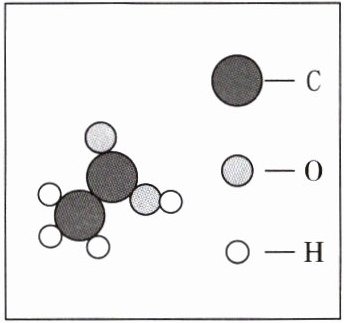
(注:●表示C,○表示O,○表示H)
A.该分子由C、H、O三种元素组成
B.该分子中C、H、O三种原子的个数比为1:2:1
C.该物质的相对分子质量为60 g
D.该物质的化学式为$C_3H_4O_2$
B
)。
(注:●表示C,○表示O,○表示H)
A.该分子由C、H、O三种元素组成
B.该分子中C、H、O三种原子的个数比为1:2:1
C.该物质的相对分子质量为60 g
D.该物质的化学式为$C_3H_4O_2$
答案:
解:由微观结构示意图可知,该分子中C原子个数为2,H原子个数为4,O原子个数为2。
A. 分子由原子构成,物质由元素组成,该物质由C、H、O三种元素组成,A错误。
B. C、H、O三种原子的个数比为2:4:2=1:2:1,B正确。
C. 相对分子质量单位是“1”,不是“g”,C错误。
D. 该物质的化学式为C₂H₄O₂,D错误。
答案:B
A. 分子由原子构成,物质由元素组成,该物质由C、H、O三种元素组成,A错误。
B. C、H、O三种原子的个数比为2:4:2=1:2:1,B正确。
C. 相对分子质量单位是“1”,不是“g”,C错误。
D. 该物质的化学式为C₂H₄O₂,D错误。
答案:B
7. 维生素C$(C_6H_8O_6)$具有增强机体抵抗力,预防坏血病等作用。
(1)维生素C中碳、氢、氧三种元素的质量比为
(2)
(1)维生素C中碳、氢、氧三种元素的质量比为
9:1:12
(填最简整数比)。(2)
88
g维生素C中含碳元素的质量是36 g。
答案:
【解析】:
(1)维生素C中碳、氢、氧三种元素的质量比可以通过各自的相对原子质量来计算。碳的相对原子质量为12,氢的相对原子质量为1,氧的相对原子质量为16。因此,维生素C中碳、氢、氧三种元素的质量比为:
$(6 × 12) : (8 × 1) : (6 × 16) = 72 : 8 : 96 = 9 : 1 : 12$
(2)要找出含有36g碳元素的维生素C的质量,我们可以设置一个等式。设维生素C的质量为x,则:
$x × \frac{6 × 12}{6 × 12 + 8 × 1 + 6 × 16} = 36g$
即:
$x × \frac{72}{176} = 36g$
解这个等式,我们得到:
$x = \frac{36g × 176}{72} = 88g$
【答案】:
(1)$9 : 1 : 12$
(2)88
(1)维生素C中碳、氢、氧三种元素的质量比可以通过各自的相对原子质量来计算。碳的相对原子质量为12,氢的相对原子质量为1,氧的相对原子质量为16。因此,维生素C中碳、氢、氧三种元素的质量比为:
$(6 × 12) : (8 × 1) : (6 × 16) = 72 : 8 : 96 = 9 : 1 : 12$
(2)要找出含有36g碳元素的维生素C的质量,我们可以设置一个等式。设维生素C的质量为x,则:
$x × \frac{6 × 12}{6 × 12 + 8 × 1 + 6 × 16} = 36g$
即:
$x × \frac{72}{176} = 36g$
解这个等式,我们得到:
$x = \frac{36g × 176}{72} = 88g$
【答案】:
(1)$9 : 1 : 12$
(2)88
8. 我国是全球海域可燃冰试开采连续产气时间最长的国家。已知某种可燃冰的化学式为$CH_4\cdot8H_2O$,请回答下列问题。
(1)这种可燃冰的相对分子质量是______
(2)这种可燃冰中各元素的质量比为$C:H:O= $______
(3)该可燃冰中碳元素的质量分数为______
(1)这种可燃冰的相对分子质量是______
160
。(2)这种可燃冰中各元素的质量比为$C:H:O= $______
3:5:32
(填最简整数比)。(3)该可燃冰中碳元素的质量分数为______
7.5%
。
答案:
(1)解:相对分子质量=12+(1×4)+8×(1×2+16)=12+4+8×18=16+144=160
(2)解:C:H:O=12:(1×4+8×2):(8×16)=12:(4+16):128=12:20:128=3:5:32
(3)解:碳元素的质量分数=12/160×100%=7.5%
(1)解:相对分子质量=12+(1×4)+8×(1×2+16)=12+4+8×18=16+144=160
(2)解:C:H:O=12:(1×4+8×2):(8×16)=12:(4+16):128=12:20:128=3:5:32
(3)解:碳元素的质量分数=12/160×100%=7.5%
9. 炒菜时,又加料酒又加醋,可使菜变得可口,原因是醋中的乙酸与料酒中的乙醇生成乙酸乙酯。下表中是几种常见的酯,请回答下列问题。
| 酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
| 化学式 | $C_2H_4O_2$ | $C_3H_6O_2$ | $C_3H_6O_2$ | X |

(1)甲酸甲酯$(C_2H_4O_2)$中碳元素、氢元素、氧元素的质量比为
(2)甲酸乙酯$(C_3H_6O_2)$中碳元素的质量分数为
(3)比较归纳是学习化学的重要方法,据表推测X的化学式为
| 酯的名称 | 甲酸甲酯 | 甲酸乙酯 | 乙酸甲酯 | 乙酸乙酯 |
| 化学式 | $C_2H_4O_2$ | $C_3H_6O_2$ | $C_3H_6O_2$ | X |

(1)甲酸甲酯$(C_2H_4O_2)$中碳元素、氢元素、氧元素的质量比为
6:1:8
。(2)甲酸乙酯$(C_3H_6O_2)$中碳元素的质量分数为
48.6%
(计算结果精确到0.1%)。(3)比较归纳是学习化学的重要方法,据表推测X的化学式为
$C_4H_8O_2$
。
答案:
【解析】:
(1)甲酸甲酯($C_{2}H_{4}O_{2}$)中碳元素、氢元素、氧元素的质量比,需要根据相对原子质量来计算。碳的相对原子质量为12,氢的相对原子质量为1,氧的相对原子质量为16。因此,甲酸甲酯中碳、氢、氧元素的质量比为$(12×2):(1×4):(16×2)=6:1:8$。
(2)甲酸乙酯($C_{3}H_{6}O_{2}$)中碳元素的质量分数,需要计算碳元素的质量占整个分子质量的比例。甲酸乙酯的分子质量为$(12×3)+(1×6)+(16×2)=74$,碳元素的质量为$12×3=36$,所以碳元素的质量分数为$36/74×100\%\approx48.6\%$。
(3)根据表格中的信息,可以看出酯的名称与化学式之间存在一定的规律。甲酸某酯的化学式中,碳原子数为2,氢原子数为4,氧原子数为2,且另一个醇羟基部分碳原子数加1;乙酸某酯的化学式中,碳原子数为3,氢原子数为6,氧原子数为2,且另一个醇羟基部分碳原子数加1.因此,可以推测乙酸乙酯的化学式中,碳原子数应为4(乙酸部分3个+乙醇部分1个),氢原子数应为8(根据酯化反应原理,氢原子数应为醇羟基部分氢原子数的2倍加乙酸部分氢原子数减去反应脱去的水的氢原子数2,即$6+2- 2×1=8$),氧原子数应为2(保持酯的基本结构)。所以,X的化学式为$C_{4}H_{8}O_{2}$。
【答案】:
(1)$6:1:8$
(2)$48.6\%$
(3)$C_{4}H_{8}O_{2}$
(1)甲酸甲酯($C_{2}H_{4}O_{2}$)中碳元素、氢元素、氧元素的质量比,需要根据相对原子质量来计算。碳的相对原子质量为12,氢的相对原子质量为1,氧的相对原子质量为16。因此,甲酸甲酯中碳、氢、氧元素的质量比为$(12×2):(1×4):(16×2)=6:1:8$。
(2)甲酸乙酯($C_{3}H_{6}O_{2}$)中碳元素的质量分数,需要计算碳元素的质量占整个分子质量的比例。甲酸乙酯的分子质量为$(12×3)+(1×6)+(16×2)=74$,碳元素的质量为$12×3=36$,所以碳元素的质量分数为$36/74×100\%\approx48.6\%$。
(3)根据表格中的信息,可以看出酯的名称与化学式之间存在一定的规律。甲酸某酯的化学式中,碳原子数为2,氢原子数为4,氧原子数为2,且另一个醇羟基部分碳原子数加1;乙酸某酯的化学式中,碳原子数为3,氢原子数为6,氧原子数为2,且另一个醇羟基部分碳原子数加1.因此,可以推测乙酸乙酯的化学式中,碳原子数应为4(乙酸部分3个+乙醇部分1个),氢原子数应为8(根据酯化反应原理,氢原子数应为醇羟基部分氢原子数的2倍加乙酸部分氢原子数减去反应脱去的水的氢原子数2,即$6+2- 2×1=8$),氧原子数应为2(保持酯的基本结构)。所以,X的化学式为$C_{4}H_{8}O_{2}$。
【答案】:
(1)$6:1:8$
(2)$48.6\%$
(3)$C_{4}H_{8}O_{2}$
查看更多完整答案,请扫码查看


