第93页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
1. (教材习题改编)对溶液组成的认识,下列说法不正确的是 (
A.溶液中的溶剂只能是水
B.溶液是由溶质和溶剂组成的混合物
C.溶质可以是固体,也可以是液体或气体
D.溶液的质量等于溶质质量和溶剂质量之和
A
)A.溶液中的溶剂只能是水
B.溶液是由溶质和溶剂组成的混合物
C.溶质可以是固体,也可以是液体或气体
D.溶液的质量等于溶质质量和溶剂质量之和
答案:
A
2. (教材素材改编)写出下列溶液中的溶质和溶剂(能用化学式表示的,写出化学式)。
(1)蔗糖溶液:溶质是
(2)盐酸:溶质是
(3)氯化钠溶液:溶质是
(1)蔗糖溶液:溶质是
蔗糖
,溶剂是H₂O
。(2)盐酸:溶质是
HCl
,溶剂是H₂O
。(3)氯化钠溶液:溶质是
NaCl
,溶剂是H₂O
。
答案:
(1)蔗糖 H₂O
(2)HCl H₂O
(3)NaCl H₂O
(1)蔗糖 H₂O
(2)HCl H₂O
(3)NaCl H₂O
3. 生理盐水可用于清理伤口,其溶质为氯化钠。溶质质量分数为 3%的氯化钠溶液中的“3%”表示 (
A.100 g水中含有3g氯化钠
B.103 g水中含有3g氯化钠
C.该溶液中溶质和溶剂的质量比为3:97
D.该溶液中溶质和溶剂的质量比为3:100
C
)A.100 g水中含有3g氯化钠
B.103 g水中含有3g氯化钠
C.该溶液中溶质和溶剂的质量比为3:97
D.该溶液中溶质和溶剂的质量比为3:100
答案:
C 【解析】溶质质量分数为 3%的氯化钠溶液中的“3%”表示该溶液中溶质和溶液的质量比为3:100,溶剂质量=溶液质量-溶质质量,可知溶质和溶剂的质量比为 3:97,故选 C。
4. 20℃时,将10g蔗糖加入40g水中,全部溶解,所得溶液的溶质质量分数为 (
A.10%
B.20%
C.25%
D.40%
B
)A.10%
B.20%
C.25%
D.40%
答案:
B 【解析】20℃时,将10 g蔗糖加入40 g水中,全部溶解,所得溶液质量为10 g+40 g=50 g,所得溶液的溶质质量分数为$\frac {10g}{50g}×100\% =20\% $,故选B。
5. (教材习题改编)用氯化钠固体配制一定溶质质量分数的氯化钠溶液,不需要用到的仪器是 (
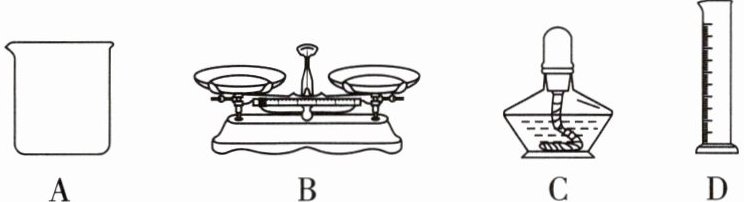
C
)
答案:
C
6. (教材实验改编)硝酸钾营养液有助于绿萝良好生长,为配制100g溶质质量分数为0.2%的硝酸钾溶液,下列相关说法正确的是 (
A.量筒应选择50 mL
B.配制硝酸钾溶液的步骤是计算、溶解和称取
C.称取时发现天平指针偏向右盘,可增加适量硝酸钾固体
D.用量筒量取水时仰视读数,会使溶液的溶质质量分数偏大
C
)A.量筒应选择50 mL
B.配制硝酸钾溶液的步骤是计算、溶解和称取
C.称取时发现天平指针偏向右盘,可增加适量硝酸钾固体
D.用量筒量取水时仰视读数,会使溶液的溶质质量分数偏大
答案:
C 【解析】选项分析判断A配制100 g溶质质量分数为0.2%的硝酸钾溶液,所需硝酸钾质量为100g×0.2%=0.2g,所需水的质量为100g-0.2g=99.8g,结合水的密度计算所需水的体积为99.8mL,因此量筒应选择100 mL。×B配制硝酸钾溶液的步骤是计算、称取、量取、溶解、转移×C称取时发现天平指针偏向右盘,说明所加硝酸钾质量不足,可增加适量硝酸钾固体直至天平平衡√D用量筒量取水时仰视读数,读数比真实值偏小,所量取水的体积偏大,会使溶液的溶质质量分数偏小×
7. (黑白卷)小洋在实验室中配制蔗糖溶液,他用托盘天平称取蔗糖时的读数如图1所示,用量筒量取水时的读数如图2所示(已知:水的密度为1g/mL)。

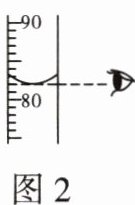
(1)小洋所称取的蔗糖的质量是
(2)小洋想配制的溶液的溶质质量分数为
(3)溶解时需要用
(4)若将量筒中的水倒入烧杯时,有少量水溅出,则最终所得蔗糖溶液的溶质质量分数


(1)小洋所称取的蔗糖的质量是
18.0
g。(2)小洋想配制的溶液的溶质质量分数为
18%
。(3)溶解时需要用
玻璃棒
搅拌,目的是加快蔗糖的溶解速率
。(4)若将量筒中的水倒入烧杯时,有少量水溅出,则最终所得蔗糖溶液的溶质质量分数
偏大
(填“偏大”“偏小”或“不变”)。
答案:
(1)18.0
(2)18%
(3)玻璃棒 加快蔗糖的溶解速率
(4)偏大【解析】
(1)根据图1可知所称取的蔗糖的质量为10g+5g+3.0g=18.0g。
(2)根据图2可知量取水的体积为82.0 mL,则水的质量为82.0 g,因此所配制的溶液的溶质质量分数=$\frac {18.0g}{18.0g+82.0g}×100\% =18\% $。
(3)溶解时用玻璃棒搅拌,目的是加快蔗糖的溶解速率。
(4)将量筒中的水倒入烧杯时,有少量水溅出,使得溶剂的质量偏小,根据溶质质量分数=$\frac {溶质质量}{溶质质量+溶剂质量}×100\% $分析,可知最终所得蔗糖溶液的溶质质量分数偏大。难点突破分析溶质质量分数的误差时,要抓住溶质质量分数=$\frac {溶质质量}{溶质质量+溶剂质量}×100\% $,结合实际操作对溶质和溶剂质量的变化作出判断,再依据溶质质量分数的含义进行判断,从而突破难点。
(1)18.0
(2)18%
(3)玻璃棒 加快蔗糖的溶解速率
(4)偏大【解析】
(1)根据图1可知所称取的蔗糖的质量为10g+5g+3.0g=18.0g。
(2)根据图2可知量取水的体积为82.0 mL,则水的质量为82.0 g,因此所配制的溶液的溶质质量分数=$\frac {18.0g}{18.0g+82.0g}×100\% =18\% $。
(3)溶解时用玻璃棒搅拌,目的是加快蔗糖的溶解速率。
(4)将量筒中的水倒入烧杯时,有少量水溅出,使得溶剂的质量偏小,根据溶质质量分数=$\frac {溶质质量}{溶质质量+溶剂质量}×100\% $分析,可知最终所得蔗糖溶液的溶质质量分数偏大。难点突破分析溶质质量分数的误差时,要抓住溶质质量分数=$\frac {溶质质量}{溶质质量+溶剂质量}×100\% $,结合实际操作对溶质和溶剂质量的变化作出判断,再依据溶质质量分数的含义进行判断,从而突破难点。
8. 日常生活情境 医疗用品 医用酒精常用于杀菌、消毒,如图是某瓶医用酒精的标签,下列说法不正确的是 (

A.溶液的质量约为425g
B.1mL医用酒精溶液的质量约为0.85g
C.配制该溶液时,可将其装入广口瓶中并贴上标签
D.95%医用酒精比75%医用酒精浓度更大
C
)
A.溶液的质量约为425g
B.1mL医用酒精溶液的质量约为0.85g
C.配制该溶液时,可将其装入广口瓶中并贴上标签
D.95%医用酒精比75%医用酒精浓度更大
答案:
C 【解析】分析标签信息,计算溶液的质量约为$0.85g\cdot mL^{-1}×500mL=425g$,A说法正确;密度的定义是物质的质量与体积的比值,对于密度约为$0.85g\cdot mL^{-1}$的医用酒精溶液,说明1 mL该溶液的质量约为0.85 g,B说法正确;配制该溶液时,应将其装入细口瓶中并贴上标签,C说法不正确;95%以及75%指的是医用酒精的体积分数,据此分析,相同体积下,95%的医用酒精比75%的医用酒精所含酒精体积更多,即浓度更大,D说法正确。
9. 日常生活情境 白酒 我国有许多历史悠久的著名白酒。白酒的度数通常是指20℃时酒精的体积百分数。如60度白酒是指100mL白酒中含酒精60mL。
(1)如何用500mL有刻度的器皿,将50度白酒勾兑出500mL40度白酒?
(2)500mL的白酒若喝掉一半后,剩余白酒的酒精度数
(1)如何用500mL有刻度的器皿,将50度白酒勾兑出500mL40度白酒?
用500 mL器皿量取400 mL 50度白酒,再加入100 mL水
。(2)500mL的白酒若喝掉一半后,剩余白酒的酒精度数
不变
(填“变大”“变小”或“不变”)。
答案:
(1)用500 mL器皿量取400 mL 50度白酒,再加入100 mL水
(2)不变【解析】
(1)500 mL 40度白酒中含有酒精200 mL,根据溶液稀释前后溶质质量不变,应用500 mL器皿量取400 mL 50度白酒,再加入100 mL水,即可勾兑出500 mL 40度的白酒。
(2)白酒属于溶液,溶液具有均一性,故喝掉一半后,酒精度数不变。
(1)用500 mL器皿量取400 mL 50度白酒,再加入100 mL水
(2)不变【解析】
(1)500 mL 40度白酒中含有酒精200 mL,根据溶液稀释前后溶质质量不变,应用500 mL器皿量取400 mL 50度白酒,再加入100 mL水,即可勾兑出500 mL 40度的白酒。
(2)白酒属于溶液,溶液具有均一性,故喝掉一半后,酒精度数不变。
查看更多完整答案,请扫码查看


