第43页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
10. (教材习题改编)某氧化物的化学式为 RO,经测定其中 R 元素的质量分数为 80%,则该氧化物的相对分子质量为(
A.20
B.40
C.60
D.80
80
)A.20
B.40
C.60
D.80
答案:
1. 首先设$R$的相对原子质量为$x$:
根据化合物中元素质量分数公式$\omega=\frac{相对原子质量×原子个数}{相对分子质量}×100\%$,对于$RO$,$R$元素质量分数$\omega(R)=\frac{x}{x + 16}×100\%=80\%$。
2. 然后求解$x$:
由$\frac{x}{x + 16}=0.8$,
去分母得$x = 0.8(x + 16)$,
展开括号得$x = 0.8x+12.8$,
移项得$x−0.8x = 12.8$,
合并同类项得$0.2x = 12.8$,
解得$x = 64$。
3. 最后求$RO$的相对分子质量:
根据相对分子质量$M = x + 16$($x$为$R$的相对原子质量),把$x = 64$代入,得$M=64 + 16=80$。
所以该氧化物的相对分子质量为$80$,答案是D。
根据化合物中元素质量分数公式$\omega=\frac{相对原子质量×原子个数}{相对分子质量}×100\%$,对于$RO$,$R$元素质量分数$\omega(R)=\frac{x}{x + 16}×100\%=80\%$。
2. 然后求解$x$:
由$\frac{x}{x + 16}=0.8$,
去分母得$x = 0.8(x + 16)$,
展开括号得$x = 0.8x+12.8$,
移项得$x−0.8x = 12.8$,
合并同类项得$0.2x = 12.8$,
解得$x = 64$。
3. 最后求$RO$的相对分子质量:
根据相对分子质量$M = x + 16$($x$为$R$的相对原子质量),把$x = 64$代入,得$M=64 + 16=80$。
所以该氧化物的相对分子质量为$80$,答案是D。
11. 已知某物质的化学式为$RSO_4$,相对分子质量为 160,则 R 的元素符号为(
A.Ca
B.Cu
C.Zn
D.Mg
B
)A.Ca
B.Cu
C.Zn
D.Mg
答案:
B
12. 某化合物由钠、氧两种元素组成,其中钠、氧元素的质量比为 23:16,则该化合物的化学式为(
A.$Na_2O$
B.$Na_2O_2$
C.$NaO_2$
D.$NaO_3$
B
)A.$Na_2O$
B.$Na_2O_2$
C.$NaO_2$
D.$NaO_3$
答案:
B
13. 现有$SO_2和SO_3$两种物质,当$SO_2和SO_3$两种物质的质量比为 1:2 时,则二者中硫元素质量比为(
A.1:2
B.2:3
C.5:8
D.8:5
C
)A.1:2
B.2:3
C.5:8
D.8:5
答案:
C
14. (教材习题改编)漂白精常用于游泳池消毒,它能消除有害微生物、细菌,其主要成分为次氯酸钙[化学式为$Ca(ClO)_2$]。下列说法正确的是(
A.次氯酸钙中氯元素的化合价为+2 价
B.次氯酸钙中钙、氧原子的个数比为 1:1
C.次氯酸钙由 3 种元素组成
D.次氯酸钙的相对分子质量为 143 g
C
)A.次氯酸钙中氯元素的化合价为+2 价
B.次氯酸钙中钙、氧原子的个数比为 1:1
C.次氯酸钙由 3 种元素组成
D.次氯酸钙的相对分子质量为 143 g
答案:
C
15. 丙烷曾是连续多届奥运会火炬使用的燃料,其分子结构模型如图所示。下列关于丙烷的说法不正确的是(
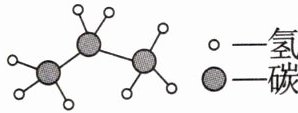
A.属于氧化物
B.由碳元素和氢元素组成
C.1 个丙烷分子中含有 11 个原子
D.丙烷中碳元素和氢元素的质量比为 9:2
A
)
A.属于氧化物
B.由碳元素和氢元素组成
C.1 个丙烷分子中含有 11 个原子
D.丙烷中碳元素和氢元素的质量比为 9:2
答案:
A
16. 传统文化情境 经典篇目 《神农本草经》中有麻黄“止咳逆上气”的记载,其有效成分是麻黄碱($C_{10}H_xNO$)。
(1)已知麻黄碱的相对分子质量为 165,则$C_{10}H_xNO中x= $
(2)麻黄碱中碳、氮、氧元素质量比为
(3)33 g 麻黄碱中氢元素的质量是多少? (写出计算过程)
(1)已知麻黄碱的相对分子质量为 165,则$C_{10}H_xNO中x= $
15
。(2)麻黄碱中碳、氮、氧元素质量比为
60:7:8
(填最简整数比)。(3)33 g 麻黄碱中氢元素的质量是多少? (写出计算过程)
33 g 麻黄碱中氢元素的质量为$33g×(\frac{1×15}{12×10+1×15+14+16}×100\% )=3g$
答:33 g 麻黄碱中氢元素的质量为 3 g。
答:33 g 麻黄碱中氢元素的质量为 3 g。
答案:
(1)15
(2)60:7:8
(3)33 g 麻黄碱中氢元素的质量为$33g×(\frac{1×15}{12×10+1×15+14+16}×100\% )=3g$
答:33 g 麻黄碱中氢元素的质量为 3 g。
(1)15
(2)60:7:8
(3)33 g 麻黄碱中氢元素的质量为$33g×(\frac{1×15}{12×10+1×15+14+16}×100\% )=3g$
答:33 g 麻黄碱中氢元素的质量为 3 g。
17. 安全情境 合理用药 锌元素是人体必需的微量元素,含锌口服液对治疗锌缺乏症具有良好的疗效。其中硫酸锌($ZnSO_4$)口服液是一种常见的补锌药物。
(1)

(2)已知每支硫酸锌口服液中硫酸锌的含量为 20 mg,假设硫酸锌提供的锌能被人体全部吸收,那么每支该口服液能为人体补充多少 mg 锌元素? (结果保留一位小数)
(1)
③
如图为硫酸锌中各元素的质量分数,图中表示硫元素质量分数的是______(填序号)。
(2)已知每支硫酸锌口服液中硫酸锌的含量为 20 mg,假设硫酸锌提供的锌能被人体全部吸收,那么每支该口服液能为人体补充多少 mg 锌元素? (结果保留一位小数)
答案:
(1)③
(2)每支硫酸锌口服液中含锌元素的质量为$20mg×(\frac{65×1}{65×1+32×1+16×4}×100\% )\approx 8.1mg$
答:每支该口服液能为人体补充约 8.1 mg 锌元素。
(1)③
(2)每支硫酸锌口服液中含锌元素的质量为$20mg×(\frac{65×1}{65×1+32×1+16×4}×100\% )\approx 8.1mg$
答:每支该口服液能为人体补充约 8.1 mg 锌元素。
18. (教材学以致用改编)硝酸铵($NH_4NO_3$)和碳酸氢铵($NH_4HCO_3$)均是常见的化肥,其中某地硝酸铵 3200 元/吨,碳酸氢铵 1200 元/吨,某农民各用 2000 元钱购买这两种化肥,哪种化肥中氮元素的质量较大? (结果保留一位小数)
答案:
解:硝酸铵中氮元素的质量分数为$\frac{14×2}{14×2+1×4+16×3}×100\% =35\% $
购买硝酸铵的质量为$2000÷3200=0.625$吨
购买的硝酸铵中氮元素的质量为$0.625×35\% \approx 0.2$吨
碳酸氢铵中氮元素的质量分数为$\frac{14×1}{14×1+1×5+12×1+16×3}×100\% \approx 17.7\% $
用 2000 元能购买碳酸氢铵的质量为$2000÷1200\approx 1.67$吨
购买的碳酸氢铵中氮元素的质量为$1.67×17.7\% \approx 0.3$吨>0.2 吨
答:购买碳酸氢铵中氮元素的质量较大。
购买硝酸铵的质量为$2000÷3200=0.625$吨
购买的硝酸铵中氮元素的质量为$0.625×35\% \approx 0.2$吨
碳酸氢铵中氮元素的质量分数为$\frac{14×1}{14×1+1×5+12×1+16×3}×100\% \approx 17.7\% $
用 2000 元能购买碳酸氢铵的质量为$2000÷1200\approx 1.67$吨
购买的碳酸氢铵中氮元素的质量为$1.67×17.7\% \approx 0.3$吨>0.2 吨
答:购买碳酸氢铵中氮元素的质量较大。
19. 日常生活情境 生活用品 下图是某品牌的尿素包装袋上的部分内容。回答下列问题。

(1)尿素的相对分子质量为
(2)尿素中氮元素的质量分数为
(3)(定心卷改编)氮元素是植物生长所必需的元素,某农田计划施用该尿素 60 kg,但由于货源短缺,现改用纯净的硝酸铵($NH_4NO_3$),为保证含氮量相当,所需硝酸铵的质量是多少? (写出计算过程,结果保留一位小数)

(1)尿素的相对分子质量为
60
。(2)尿素中氮元素的质量分数为
46.7%
(结果保留一位小数),该尿素属于______混合物
(填“纯净物”或“混合物”)。(3)(定心卷改编)氮元素是植物生长所必需的元素,某农田计划施用该尿素 60 kg,但由于货源短缺,现改用纯净的硝酸铵($NH_4NO_3$),为保证含氮量相当,所需硝酸铵的质量是多少? (写出计算过程,结果保留一位小数)
答案:
(1)60
(2)46.7% 混合物
(3)解:60 kg 该尿素中含有氮元素质量为$60kg×46\% =27.6kg$
为保证含氮量相当,所需硝酸铵的质量为$27.6kg÷(\frac{14×2}{14×2+1×4+16×3}×100\% )\approx 78.9kg$
答:为保证含氮量相当,所需硝酸铵的质量为78.9 kg。
(1)60
(2)46.7% 混合物
(3)解:60 kg 该尿素中含有氮元素质量为$60kg×46\% =27.6kg$
为保证含氮量相当,所需硝酸铵的质量为$27.6kg÷(\frac{14×2}{14×2+1×4+16×3}×100\% )\approx 78.9kg$
答:为保证含氮量相当,所需硝酸铵的质量为78.9 kg。
查看更多完整答案,请扫码查看


