2026年高考领航卷化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2026年高考领航卷化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
4. 最简单的硫氮化合物是四氮化四硫(S₄N₄,S为+2价),其结构为 ,将氨通入SCl₂溶液可发生反应24SCl₂+64NH₃=4S₄N₄+S₈+48NH₄Cl,其中S₈的分子结构为
,将氨通入SCl₂溶液可发生反应24SCl₂+64NH₃=4S₄N₄+S₈+48NH₄Cl,其中S₈的分子结构为 ,设阿伏加德罗常数的值为N_A。下列说法错误的是
,设阿伏加德罗常数的值为N_A。下列说法错误的是
A.1mol SCl₂与1mol S₈含有的孤电子对数分别为8N_A和16N_A
B.消耗标准状况下的氨17.92L时,生成的S₈中S-S键数目为0.1N_A
C.1L 1mol·L⁻¹NH₄Cl溶液中含有的NH₄⁺、NH₃·H₂O、NH₃的数目和为N_A
D.S₄N₄为氧化产物,且每生成92g S₄N₄转移电子数目为4N_A
 ,将氨通入SCl₂溶液可发生反应24SCl₂+64NH₃=4S₄N₄+S₈+48NH₄Cl,其中S₈的分子结构为
,将氨通入SCl₂溶液可发生反应24SCl₂+64NH₃=4S₄N₄+S₈+48NH₄Cl,其中S₈的分子结构为 ,设阿伏加德罗常数的值为N_A。下列说法错误的是
,设阿伏加德罗常数的值为N_A。下列说法错误的是A.1mol SCl₂与1mol S₈含有的孤电子对数分别为8N_A和16N_A
B.消耗标准状况下的氨17.92L时,生成的S₈中S-S键数目为0.1N_A
C.1L 1mol·L⁻¹NH₄Cl溶液中含有的NH₄⁺、NH₃·H₂O、NH₃的数目和为N_A
D.S₄N₄为氧化产物,且每生成92g S₄N₄转移电子数目为4N_A
答案:
4.D 阿伏加德罗常数的有关计算与判断 1mol$SCl_2$与1mol$S_8$含有的孤电子对数分别为$8N_A$和$16N_A$,A正确;消耗标准状况下的氨17.92L(0.8mol)时,生成0.0125mol$S_8$,则0.0125mol$S_8$中S - S键数目为$0.1N_A$,B正确;根据物料守恒,$NH_4Cl$溶液中N元素的存在形式为$NH_4^+$、$NH_3$和$NH_3· H_2O$,即$c(NH_4^ + ) + c(NH_3) + c(NH_3· H_2O)=1mol· L^{ - 1}$,故1L 1$mol· L^{ - 1}NH_4Cl$溶液中含有的$NH_4^+$、$NH_3$、$NH_3· H_2O$的数目和为$N_A$,C正确;由化学方程式和$S_4N_4$的结构可知,$S_4N_4$中S为 + 2价,N为 - 2价,$SCl_2$中S的化合价为 + 2,$SCl_2$得到$e^ - $生成$S_8$,$NH_3$失去$e^ - $生成$S_4N_4$,故$S_4N_4$为氧化产物,且每生成92g(0.5mol)$S_4N_4$转移电子数目为$2N_A$,D错误。
5. 科学家通过X射线测得胆矾结构示意图如图所示。已知向硫酸铜溶液中滴加过量氨水最后得到深蓝色溶液,胆矾晶体加热时依次发生如下转化:CuSO₄·5H₂O→CuSO₄·3H₂O→CuSO₄·H₂O→CuSO₄,下列说法正确的是
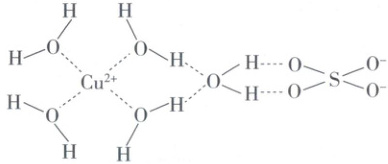
A.图中虚线均为氢键
B.加热时最先失去的是与SO₄²⁻结合的结晶水
C.晶体中SO₄²⁻中的S和H₂O中O原子的杂化方式相同
D.H₂O和NH₃与Cu²⁺结合前后,键角均不变

A.图中虚线均为氢键
B.加热时最先失去的是与SO₄²⁻结合的结晶水
C.晶体中SO₄²⁻中的S和H₂O中O原子的杂化方式相同
D.H₂O和NH₃与Cu²⁺结合前后,键角均不变
答案:
5.C 物质结构与性质 图中O与$Cu^{2 + }$结合的虚线是配位键,H与O结合的虚线是氢键,A错误;根据胆矾晶体结构中$H_2O$的作用力不同及加热过程中失水数目可知,与$SO_4^{2 - }$结合的结晶水最后失去,B错误;晶体中$SO_4^{2 - }$中的S原子和$H_2O$中的O原子的杂化方式均为$sp^3$杂化,C正确;$H_2O$和$NH_3$与$Cu^{2 + }$结合后,中心原子O和N的孤电子对数均减少[提示:孤电子对参与形成配位键],孤电子对对成键电子对的斥力大于成键电子对间的斥力,键角均变大,D错误。
6. 部分含氯化合物的"价-类"二维图如图所示。下列说法错误的是
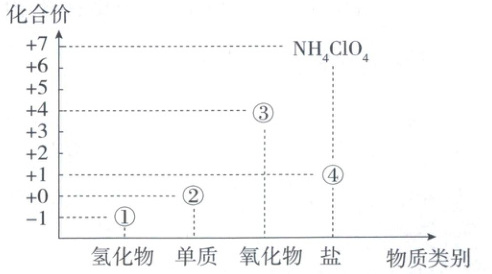
A.②③④都具有氧化性,其中③可用作自来水消毒剂
B.②可在碱溶液中转化为④
C.NH₄ClO₄分解得到①、N₂、O₂、H₂O,反应中n(氧化产物):n(还原产物)=7:4
D.工业上可通过电解④对应的钠盐溶液制备②,同时得到金属Na

A.②③④都具有氧化性,其中③可用作自来水消毒剂
B.②可在碱溶液中转化为④
C.NH₄ClO₄分解得到①、N₂、O₂、H₂O,反应中n(氧化产物):n(还原产物)=7:4
D.工业上可通过电解④对应的钠盐溶液制备②,同时得到金属Na
答案:
6.D 物质的转化关系 根据“价—类”二维图分析可知,①为HCl,②为$Cl_2$,③为$ClO_2$,④为次氯酸盐。②③④都具有氧化性,其中$ClO_2$可用作自来水消毒剂,A正确;$Cl_2$可在碱溶液中转化为次氯酸盐,B正确;$NH_4ClO_4$在强热条件下分解,化学方程式为$4NH_4ClO_4\xlongequal{\triangle}2N_2\uparrow + 5O_2\uparrow + 4HCl\uparrow + 6H_2O\uparrow$,氧化产物是$N_2$、$O_2$,还原产物是HCl,氧化产物和还原产物的物质的量之比为7:4,C正确;工业上可通过电解饱和食盐水制备氯气,通过电解熔融NaCl获得金属Na,D错误。
7. 对于下列过程中发生的化学反应,离子方程式表示错误的是
A.用Na₂CO₃溶液吸收Br₂(g):3Br₂+3CO₃²⁻=5Br⁻+BrO₃⁻+3CO₂
B.实验室制氯气:MnO₂+4H⁺+2Cl⁻$\xlongequal{\triangle}$Mn²⁺+Cl₂↑+2H₂O
C.向饱和氨盐水中投入干冰固体:NH₃+H₂O+CO₂=HCO₃⁻+NH₄⁺
D.向AgCl沉淀中加入过量氨水使AgCl溶解:AgCl+2NH₃=[Ag(NH₃)₂]⁺+Cl⁻
A.用Na₂CO₃溶液吸收Br₂(g):3Br₂+3CO₃²⁻=5Br⁻+BrO₃⁻+3CO₂
B.实验室制氯气:MnO₂+4H⁺+2Cl⁻$\xlongequal{\triangle}$Mn²⁺+Cl₂↑+2H₂O
C.向饱和氨盐水中投入干冰固体:NH₃+H₂O+CO₂=HCO₃⁻+NH₄⁺
D.向AgCl沉淀中加入过量氨水使AgCl溶解:AgCl+2NH₃=[Ag(NH₃)₂]⁺+Cl⁻
答案:
7.C 离子方程式的正误判断 $Na_2CO_3$溶液吸收$Br_2(g)$,生成$BrO_3^ - $和$Br^ - $,根据质量守恒可知同时生成二氧化碳气体,其离子方程式为$3Br_2 + 3CO_3^{2 - } = 5Br^ - + BrO_3^ - + 3CO_2$,A正确;浓盐酸与二氧化锰在加热条件下反应制氯气,离子方程式为$MnO_2 + 4H^ + + 2Cl^-\xlongequal{\triangle}Mn^{2 + } + Cl_2\uparrow + 2H_2O$,B正确;饱和氨盐水中含$NH_3$、$Cl^ - $、$Na^ + $,投入干冰,发生反应生成$NaHCO_3$沉淀和$NH_4Cl$,离子方程式应为$NH_3 + H_2O + CO_2 + Na^+=NaHCO_3\downarrow + NH_4^+$,C错误;向$AgCl$沉淀中加入过量氨水使$AgCl$溶解,其离子方程式为$AgCl + 2NH_3=[Ag(NH_3)_2]^ + + Cl^ - $,D正确。
查看更多完整答案,请扫码查看


