2025年启东中学作业本九年级化学上册人教版安徽专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年启东中学作业本九年级化学上册人教版安徽专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第8页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
7. B (2025·天津和平区一模)已知金属锰在金属活动性顺序中位于铝和锌之间。下列化学反应不能发生的是 (
A.$ Mn + 2HCl = MnCl_2 + H_2 \uparrow $
B.$ Mg + MnSO_4 = MgSO_4 + Mn $
C.$ Fe + MnSO_4 = FeSO_4 + Mn $
D.$ Mn + CuSO_4 = MnSO_4 + Cu $
C
)A.$ Mn + 2HCl = MnCl_2 + H_2 \uparrow $
B.$ Mg + MnSO_4 = MgSO_4 + Mn $
C.$ Fe + MnSO_4 = FeSO_4 + Mn $
D.$ Mn + CuSO_4 = MnSO_4 + Cu $
答案:
7.C
8. B (2024·四川雅安一模)某小组同学利用杠杆原理设计如图所示实验,实验前在杠杆的两端分别挂质量相等的铜球和锌球(均已打磨),此时杠杆平衡,然后将两个金属球分别浸没在盛有稀硫酸和 $ FeSO_4 $溶液的烧杯中进行实验。下列有关说法不正确的是 (
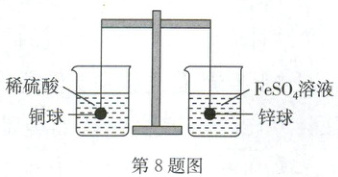
A.实验中观察到左端烧杯中无明显现象
B.右端烧杯中反应后的溶液里一定有 $ ZnSO_4 $
C.一段时间后移走烧杯,杠杆左端下沉
D.该实验可得出铁的金属活动性比铜强
D
)
A.实验中观察到左端烧杯中无明显现象
B.右端烧杯中反应后的溶液里一定有 $ ZnSO_4 $
C.一段时间后移走烧杯,杠杆左端下沉
D.该实验可得出铁的金属活动性比铜强
答案:
8.D
9. A 整理和归纳是有效的学习方法。下面是某学习小组的同学对 $ Mg、Fe、Cu、Hg、Ag $五种金属相关知识的归纳整理。请你参与并回答问题。
(1)从物理性质上看,每种金属都有自己的特性。你认为其中一种金属与其他金属的不同之处是
(2)从化学性质上看,与盐酸反应最剧烈的是
(3)性质决定用途、用途反映性质是重要的化学学科思想。用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的
(1)从物理性质上看,每种金属都有自己的特性。你认为其中一种金属与其他金属的不同之处是
常温下Hg是液体而其余均为固体(合理即可)
。(2)从化学性质上看,与盐酸反应最剧烈的是
Mg(或镁)
;有一种金属的化合物的溶液能与其他四种金属发生反应,该金属是Ag(或银)
,写出其中一个反应的化学方程式:Cu+2AgNO₃=Cu(NO₃)₂+2Ag(合理即可)
。(3)性质决定用途、用途反映性质是重要的化学学科思想。用镁粉制作的烟花在夜空中发出耀眼的白光,这是利用了镁的
可燃
性。
答案:
9.
(1)常温下Hg是液体而其余均为固体(合理即可)
(2)Mg(或镁) Ag(或银)
Cu+2AgNO₃=Cu(NO₃)₂+2Ag(合理即可)
(3)可燃
(1)常温下Hg是液体而其余均为固体(合理即可)
(2)Mg(或镁) Ag(或银)
Cu+2AgNO₃=Cu(NO₃)₂+2Ag(合理即可)
(3)可燃
10. A 如图为某学习小组探究金属化学性质时所做的四个实验,仔细分析后回答下列问题。
(1)描述 A 中的实验现象:
(2)写出 C 中反应的化学方程式:
(3)要比较 $ Cu、Fe、Ag $的活动性顺序,至少要做的实验是
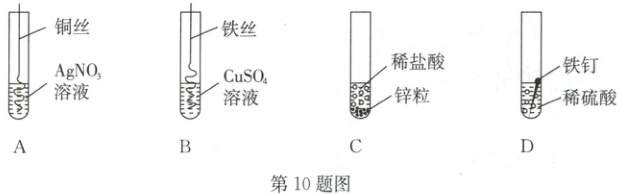
(1)描述 A 中的实验现象:
铜丝表面覆盖了一层银白色固体,溶液变为蓝色
。(2)写出 C 中反应的化学方程式:
Zn+2HCl=ZnCl₂+H₂↑
。(3)要比较 $ Cu、Fe、Ag $的活动性顺序,至少要做的实验是
AB
(填序号)。
答案:
10.
(1)铜丝表面覆盖了一层银白色固体,溶液变为蓝色
(2)Zn+2HCl=ZnCl₂+H₂↑
(3)AB
(1)铜丝表面覆盖了一层银白色固体,溶液变为蓝色
(2)Zn+2HCl=ZnCl₂+H₂↑
(3)AB
11. B 学习合金知识后,知道了不锈钢中含有金属铬。某同学想:铬与常见铁、铜相比,其金属活动性强弱如何呢?于是,他和同学们一起进行了以下探究。
【查阅资料】①铬是银白色、有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜;②能与稀硫酸反应,生成硫酸亚铬($ CrSO_4 $)。
【知识回顾】金属活动性顺序:$ K\ Ca\ Na\ Mg\ Al\ Zn $
【作出猜想】猜想①:$ Cr > Fe > Cu $;猜想②:$ Fe > Cu > Cr $;猜想③:
【设计与实验】①张明同学取大小相等的铁、铜、铬三种金属片,未经打磨就分别放入等量、等浓度的稀硫酸中,记录如下表:
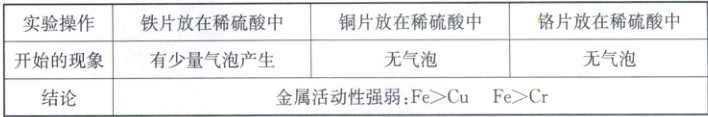
②李红同学也取大小相等的铁、铜、铬三种金属片,先用砂纸打磨后再分别放入等量、等浓度的稀硫酸中,记录如下表:
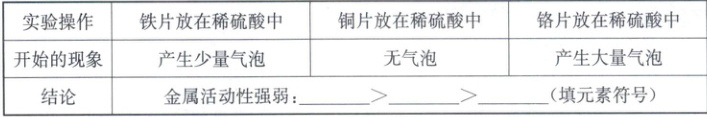
【讨论交流】为什么张明和李红两个同学记录的铬与稀硫酸反应开始的现象截然不同?原因是
【实验验证】为了进一步确认铁、铜、铬三种金属的活动性强弱,刘斌同学将打磨过的两块铁片分别放入硫酸亚铬($ CrSO_4 $)溶液和硫酸铜溶液中,观察到在硫酸亚铬溶液中无明显现象,而在硫酸铜溶液中有明显的现象是
【拓展迁移】写出铬与稀硫酸反应生成 $ CrSO_4 $的化学方程式:
【查阅资料】①铬是银白色、有光泽的金属,在空气中,像铝一样,其表面能产生致密的氧化膜;②能与稀硫酸反应,生成硫酸亚铬($ CrSO_4 $)。
【知识回顾】金属活动性顺序:$ K\ Ca\ Na\ Mg\ Al\ Zn $
Fe
$ Sn\ Pb(H) $Cu
$ Hg\ Ag\ Pt\ Au $(在横线上填写对应金属的元素符号)【作出猜想】猜想①:$ Cr > Fe > Cu $;猜想②:$ Fe > Cu > Cr $;猜想③:
Fe>Cr>Cu
。【设计与实验】①张明同学取大小相等的铁、铜、铬三种金属片,未经打磨就分别放入等量、等浓度的稀硫酸中,记录如下表:

②李红同学也取大小相等的铁、铜、铬三种金属片,先用砂纸打磨后再分别放入等量、等浓度的稀硫酸中,记录如下表:

【讨论交流】为什么张明和李红两个同学记录的铬与稀硫酸反应开始的现象截然不同?原因是
未经打磨的铬片表面有一层致密的氧化物薄膜
。【实验验证】为了进一步确认铁、铜、铬三种金属的活动性强弱,刘斌同学将打磨过的两块铁片分别放入硫酸亚铬($ CrSO_4 $)溶液和硫酸铜溶液中,观察到在硫酸亚铬溶液中无明显现象,而在硫酸铜溶液中有明显的现象是
铁片表面有红色固体析出,溶液由蓝色变为浅绿色
,其反应的化学方程式是Fe+CuSO₄=FeSO₄+Cu
。【拓展迁移】写出铬与稀硫酸反应生成 $ CrSO_4 $的化学方程式:
Cr+H₂SO₄=CrSO₄+H₂↑
。
答案:
11.【知识回顾】Fe Cu
【作出猜想】Fe>Cr>Cu
【设计与实验】Cr Fe Cu
【讨论交流】未经打磨的铬片表面有一层致密的氧化物薄膜
【实验验证】铁片表面有红色固体析出,溶液由蓝色变为浅绿色 Fe+CuSO₄=FeSO₄+Cu
【拓展迁移】Cr+H₂SO₄=CrSO₄+H₂↑
【作出猜想】Fe>Cr>Cu
【设计与实验】Cr Fe Cu
【讨论交流】未经打磨的铬片表面有一层致密的氧化物薄膜
【实验验证】铁片表面有红色固体析出,溶液由蓝色变为浅绿色 Fe+CuSO₄=FeSO₄+Cu
【拓展迁移】Cr+H₂SO₄=CrSO₄+H₂↑
查看更多完整答案,请扫码查看


