2025年启东中学作业本九年级化学上册人教版安徽专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年启东中学作业本九年级化学上册人教版安徽专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第22页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
14. B (2025·合肥45中一模)某校化学兴趣小组以“金属材料铜”为主题开展项目式学习:
【项目一】铜的冶炼
我国是最早使用湿法炼铜的国家,古书记载“曾青得铁则化为铜”。
(1)“青铜”属于
(2)“曾青”即硫酸铜溶液,湿法炼铜所发生反应的化学方程式为
【项目二】铜的化学性质
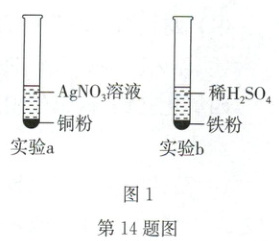
为探究铜、铁、银的金属活动性,及其与氢的位置关系,设计如图1实验。
(3)①实验a可观察到的现象有
②为达成预期实验目的,至少还需补充一个实验,该实验是
【项目三】分析铜锈的成分
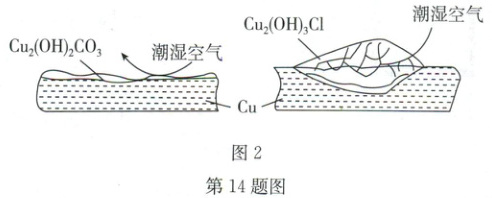
铜锈赋予青铜器历史感。铜锈主要有Cu₂(OH)₂CO₃和Cu₂(OH)₃Cl,考古界根据铜锈是否会加速铜的锈蚀分为“有害锈”和“无害锈”,其作用示意图2如下:
(4)据图可知Cu₂(OH)₃Cl具有
(5)Cu₂(OH)₂CO₃可表示为xCu(OH)₂·yCuCO₃,兼具Cu(OH)₂和CuCO₃的化学性质,x:y=
【项目一】铜的冶炼
我国是最早使用湿法炼铜的国家,古书记载“曾青得铁则化为铜”。
(1)“青铜”属于
合金
(填“单质”或“合金”)。(2)“曾青”即硫酸铜溶液,湿法炼铜所发生反应的化学方程式为
Fe+CuSO₄=FeSO₄+Cu
,该反应属于置换反应
(填基本反应类型)。【项目二】铜的化学性质
为探究铜、铁、银的金属活动性,及其与氢的位置关系,设计如图1实验。
(3)①实验a可观察到的现象有
析出银白色固体,溶液由无色变为蓝色
。②为达成预期实验目的,至少还需补充一个实验,该实验是
稀硫酸和铜粉混合(合理即可)
。【项目三】分析铜锈的成分
铜锈赋予青铜器历史感。铜锈主要有Cu₂(OH)₂CO₃和Cu₂(OH)₃Cl,考古界根据铜锈是否会加速铜的锈蚀分为“有害锈”和“无害锈”,其作用示意图2如下:
(4)据图可知Cu₂(OH)₃Cl具有
疏松
(填“致密”或“疏松”)结构,属于有害锈的原因是疏松多孔,能够吸收水蒸气、氯化物和氧气,促进生锈
。(5)Cu₂(OH)₂CO₃可表示为xCu(OH)₂·yCuCO₃,兼具Cu(OH)₂和CuCO₃的化学性质,x:y=
1:1
。

答案:
14.
(1)合金
(2)Fe+CuSO₄=FeSO₄+Cu 置换反应
(3)①析出银白色固体,溶液由无色变为蓝色 ②稀硫酸和铜粉混合(合理即可)
(4)疏松 疏松多孔,能够吸收水蒸气、氯化物和氧气,促进生锈
(5)1:1
点拨:
(3)①实验a中硝酸银与铜反应生成银和硝酸铜,可观察到的现象有析出银白色固体,溶液由无色变为蓝色;②实验a中硝酸银与铜反应生成银和硝酸铜,说明金属活动性铜>银;实验b中铁与稀硫酸反应生成氢气和硫酸亚铁,说明金属活动性铁>氢,为验证金属活动性铁>氢>铜>银,至少还需补充一个实验,该实验是稀硫酸和铜粉混合,铜与稀硫酸不反应,说明金属活动性氢>铜,根据铜>银、铁>氢、氢>铜,能得出金属活动性铁>氢>铜>银。
(4)由图可知,Cu₂(OH)₃Cl具有疏松结构,该物质疏松多孔,能够吸收水蒸气、氯化物和氧气,促进生锈,所以属于有害锈。
(5)Cu₂(OH)₃CO₃中铜原子个数为2,氢氧根离子个数为2,x Cu(OH)₂·yCuCO₃中铜原子个数为x+y,氢氧根离子个数为2x,所以x+y=2,2x=2,故x=1,y=1,所以x:y=1:1。
(1)合金
(2)Fe+CuSO₄=FeSO₄+Cu 置换反应
(3)①析出银白色固体,溶液由无色变为蓝色 ②稀硫酸和铜粉混合(合理即可)
(4)疏松 疏松多孔,能够吸收水蒸气、氯化物和氧气,促进生锈
(5)1:1
点拨:
(3)①实验a中硝酸银与铜反应生成银和硝酸铜,可观察到的现象有析出银白色固体,溶液由无色变为蓝色;②实验a中硝酸银与铜反应生成银和硝酸铜,说明金属活动性铜>银;实验b中铁与稀硫酸反应生成氢气和硫酸亚铁,说明金属活动性铁>氢,为验证金属活动性铁>氢>铜>银,至少还需补充一个实验,该实验是稀硫酸和铜粉混合,铜与稀硫酸不反应,说明金属活动性氢>铜,根据铜>银、铁>氢、氢>铜,能得出金属活动性铁>氢>铜>银。
(4)由图可知,Cu₂(OH)₃Cl具有疏松结构,该物质疏松多孔,能够吸收水蒸气、氯化物和氧气,促进生锈,所以属于有害锈。
(5)Cu₂(OH)₃CO₃中铜原子个数为2,氢氧根离子个数为2,x Cu(OH)₂·yCuCO₃中铜原子个数为x+y,氢氧根离子个数为2x,所以x+y=2,2x=2,故x=1,y=1,所以x:y=1:1。
15. C (2025·合肥长丰县一模)室外的铁制栏杆在多雨季节易生锈,小宁对铁生锈的条件进行了探索,实验装置如图1所示。3天后,发现只有装置C中的铁丝生锈了。
(1)装置A中生石灰的作用是
(2)装置B、C中的实验现象说明与
(3)使用煮沸过的蒸馏水的原因是
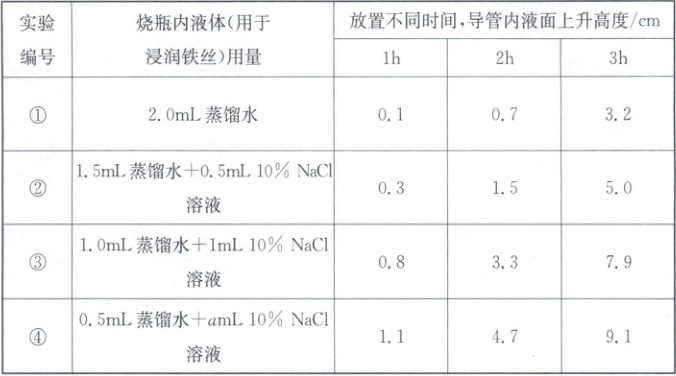
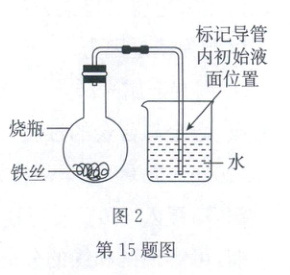
【拓展探究】为探究NaCl溶液的浓度对铁生锈速率的影响,室温下,取大小、形状相同的光亮铁丝,用如图2装置完成实验并记录如下。
【解释与结论】
(4)导管内液面上升的原因是铁生锈消耗氧气,导致瓶内气压
(5)实验编号④中的a=
(6)依据实验①~④,可以得出的结论是
(7)小组同学猜想铁生锈的快慢还可能与氧气的浓度有关,为判断该猜想是否正确,请设计实验进行验证:
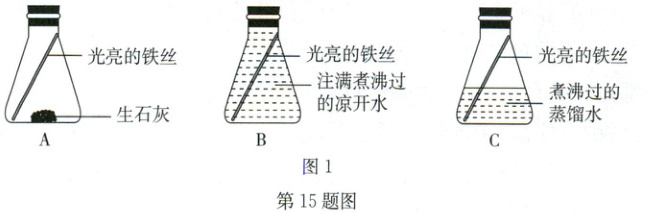
(1)装置A中生石灰的作用是
CaO+H₂O=Ca(OH)₂
(用化学方程式表示)。(2)装置B、C中的实验现象说明与
氧气
接触是铁生锈的条件之一。(3)使用煮沸过的蒸馏水的原因是
除去溶解在水中的氧气
。【拓展探究】为探究NaCl溶液的浓度对铁生锈速率的影响,室温下,取大小、形状相同的光亮铁丝,用如图2装置完成实验并记录如下。
【解释与结论】
(4)导管内液面上升的原因是铁生锈消耗氧气,导致瓶内气压
<
(填“>”“=”或“<”)外界气压,水倒流入导管中。(5)实验编号④中的a=
1.5
。(6)依据实验①~④,可以得出的结论是
在其他条件相同时,随着氯化钠溶液浓度的增加,铁生锈速率加快
。(7)小组同学猜想铁生锈的快慢还可能与氧气的浓度有关,为判断该猜想是否正确,请设计实验进行验证:
将大小相同的2根洁净的铁钉分别放入大小相同的试管中,再加入适量且等量的水,最后充入浓度不同的氧气,将试管密封,一段时间后,观察到氧气浓度较高的试管中铁钉生锈更严重。由此可得出氧气浓度越高,铁生锈越快。
(简述实验步骤、现象和结论)。


答案:
15.
(1)CaO+H₂O=Ca(OH)₂
(2)氧气
(3)除去溶解在水中的氧气
(4)<
(5)1.5
(6)在其他条件相同时,随着氯化钠溶液浓度的增加,铁生锈速率加快
(7)将大小相同的2根洁净的铁钉分别放入大小相同的试管中,再加入适量且等量的水,最后充入浓度不同的氧气,将试管密封,一段时间后,观察到氧气浓度较高的试管中铁钉生锈更严重。由此可得出氧气浓度越高,铁生锈越快。
(1)CaO+H₂O=Ca(OH)₂
(2)氧气
(3)除去溶解在水中的氧气
(4)<
(5)1.5
(6)在其他条件相同时,随着氯化钠溶液浓度的增加,铁生锈速率加快
(7)将大小相同的2根洁净的铁钉分别放入大小相同的试管中,再加入适量且等量的水,最后充入浓度不同的氧气,将试管密封,一段时间后,观察到氧气浓度较高的试管中铁钉生锈更严重。由此可得出氧气浓度越高,铁生锈越快。
查看更多完整答案,请扫码查看


