第97页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
3. 有关如图所示反应,下列说法错误的是(
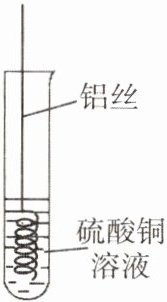
A.铝丝需要用砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性:Al > Cu
D.化学方程式为$Al + CuSO_4 = Cu + AlSO_4$
D
)
A.铝丝需要用砂纸打磨
B.溶液由蓝色变为无色
C.金属活动性:Al > Cu
D.化学方程式为$Al + CuSO_4 = Cu + AlSO_4$
答案:
D
4. 等臂杠杆两端各系一个等质量的实心铁球。将杠杆调平衡后,将球分别浸没在等质量、等密度的稀硫酸和$CuSO_4$溶液中(如图所示),一段时间后杠杆将会(
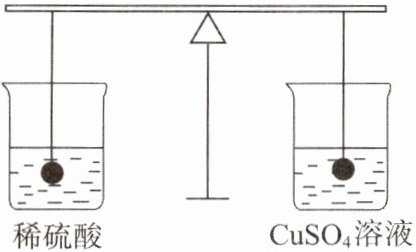
A.左端上翘
B.右端上翘
C.仍然平衡
D.无法判断
A
)
A.左端上翘
B.右端上翘
C.仍然平衡
D.无法判断
答案:
A
5. 验证镁、铜的金属活动性顺序,下列试剂不能选用的是(
$A. MgSO_4$溶液
$B. KCl溶液$
C. 稀盐酸
$D. ZnCl_2$溶液
B
)$A. MgSO_4$溶液
$B. KCl溶液$
C. 稀盐酸
$D. ZnCl_2$溶液
答案:
B
6. 铝、铁、铜三种金属中不能与稀硫酸发生置换反应的是
为验证Al、Fe、Cu的金属活动性强弱,某同学选用以下试剂设计实验方案,其中不合理的是
①Al、$FeSO_4$溶液、Cu
②$Al_2(SO_4)_3$溶液、Fe、$CuSO_4$溶液
③Al、Fe、$CuSO_4$溶液
铜
。铁制品易生锈,需要做防锈处理,而铝的化学性质比铁活泼,但铝制品通常不做防锈处理,是因为铝表面容易形成一层致密的氧化铝薄膜,防止内部的铝进一步被氧化
。为验证Al、Fe、Cu的金属活动性强弱,某同学选用以下试剂设计实验方案,其中不合理的是
③
。①Al、$FeSO_4$溶液、Cu
②$Al_2(SO_4)_3$溶液、Fe、$CuSO_4$溶液
③Al、Fe、$CuSO_4$溶液
答案:
铜 一层致密的氧化铝薄膜,防止内部的铝进一步被氧化 ③
7. 我国古代在认识、改造和应用物质方面有着辉煌的历史:①东晋《抱朴子》中记载“以曾青涂铁,铁赤色如铜”(“曾青”即硫酸铜溶液);②战国《周礼》中记载“煤饼烧蛎房成灰”(“蛎房”即牡蛎壳,主要成分是碳酸钙),将“灰”溶于水可制得沤浸树皮脱胶的碱液;③元代《庚道集》中记载“点铜成银”(即单质铜与砷熔合形成银白色的物质)。
请运用学过的化学知识回答下列问题:
(1)①中发生反应的化学方程式为
(2)②中涉及的两种基本反应类型是
(3)③中的“银”
A. 合金不是单质
B. 合金中一定不含非金属
C. 合金属于金属材料
D. 一般合金与其组分金属相比,熔点升高
E. 合金与其组分金属相比往往硬度增大
(4)某工厂欲从只含有溶质$CuSO_4$的废液中回收金属铜,并得到工业原料硫酸亚铁,其简要工业流程如图所示。
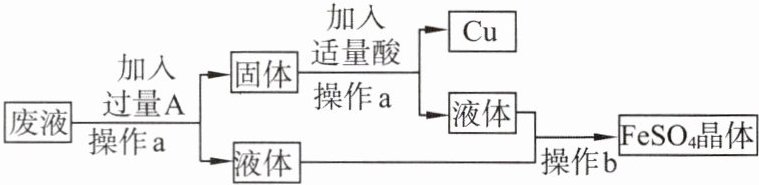
①操作a、b的名称分别是
②上述流程中A物质是
③写出上述流程中加入适量酸时反应的化学方程式:
请运用学过的化学知识回答下列问题:
(1)①中发生反应的化学方程式为
$Fe+CuSO_{4}=FeSO_{4}+Cu$
。(2)②中涉及的两种基本反应类型是
分解反应
和化合反应
。将“灰”溶于水实际是生石灰与水反应生成熟石灰或消石灰
(填物质的俗名),该变化中明显的实验现象是放出热量
。工业上用“灰”溶于水后制得的碱液与纯碱反应,可得到烧碱,写出用纯碱制烧碱的化学方程式:$Na_{2}CO_{3}+Ca(OH)_{2}=CaCO_{3}\downarrow +2NaOH$
。(3)③中的“银”
属于
(填“属于”或“不属于”)合金。下列有关合金的说法正确的是ACE
(填字母)。A. 合金不是单质
B. 合金中一定不含非金属
C. 合金属于金属材料
D. 一般合金与其组分金属相比,熔点升高
E. 合金与其组分金属相比往往硬度增大
(4)某工厂欲从只含有溶质$CuSO_4$的废液中回收金属铜,并得到工业原料硫酸亚铁,其简要工业流程如图所示。

①操作a、b的名称分别是
过滤
、蒸发
;实验室中,这两种操作都要用到的玻璃仪器是玻璃棒
。②上述流程中A物质是
铁
。③写出上述流程中加入适量酸时反应的化学方程式:
$Fe+H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow $
。
答案:
(1)$Fe+CuSO_{4}=FeSO_{4}+Cu$
(2)分解反应 化合反应 熟石灰或消石灰 热量 $Na_{2}CO_{3}+Ca(OH)_{2}=CaCO_{3}\downarrow +2NaOH$
(3)属于 ACE
(4)①过滤 蒸发 玻璃棒 ②铁 ③$Fe+H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow $
(1)$Fe+CuSO_{4}=FeSO_{4}+Cu$
(2)分解反应 化合反应 熟石灰或消石灰 热量 $Na_{2}CO_{3}+Ca(OH)_{2}=CaCO_{3}\downarrow +2NaOH$
(3)属于 ACE
(4)①过滤 蒸发 玻璃棒 ②铁 ③$Fe+H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow $
查看更多完整答案,请扫码查看


