第93页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
1. 金属镁、铁、铜都能与氧气反应生成相应的
金属氧化物
,不同金属与氧气反应的难易与剧烈程度是不同
的:例如,镁、铝常温下可与氧气反应;铁、铜常温下几乎不与氧气反应,但在加热或点燃时可与氧气反应;而金即使高温下也不与氧气反应。
答案:
金属氧化物;不同
2. 探究不同金属与酸能否反应及剧烈程度的实验中,需要控制的变量有
温度
、酸的种类
、酸的浓度
等。经实验验证,金属铁、锌能与酸反应,而铜不行,请写出铁、锌与盐酸、硫酸反应的化学方程式:$Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$
;$Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$
;$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$
;$Zn + H_{2}SO_{4}=ZnSO_{4}+H_{2}\uparrow$
。
答案:
温度、酸的种类、酸的浓度(答案不唯一);$Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$;$Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$;$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$;$Zn + H_{2}SO_{4}=ZnSO_{4}+H_{2}\uparrow$。
3. 金属与盐酸、稀硫酸反应的难易及剧烈程度体现了金属的活动性强弱:相同条件下,金属活动性越
强
,反应越易,速率越快;金属活动性越弱
,反应速率越慢或不反应。
答案:
强,弱
4. 常见金属在溶液中的活动性顺序为:K Ca Na
Mg Al Zn Fe Sn Pb
(H)Cu Hg Ag Pt Au。位置越靠前,它的活动性
就越强。排在氢前面的金属能与稀盐酸
、稀硫酸
发生反应放出氢气。
答案:
Mg Al Zn Fe Sn Pb ;活动性;稀盐酸;稀硫酸
5. 置换反应是化学反应的基本类型之一,其特征是一种单质与一种化合物反应生成
另一种单质
和另一种化合物
。
答案:
另一种单质;另一种化合物
[补充]不同金属与酸反应生成氢气的快慢与多少的问题:
(1)产生氢气的快慢:在其他因素都相同时,产生氢气的快慢由金属
(2)产生氢气的多少:当等量酸与足量金属完全反应时,产生氢气
典型例题
(1)产生氢气的快慢:在其他因素都相同时,产生氢气的快慢由金属
活动性
决定。(2)产生氢气的多少:当等量酸与足量金属完全反应时,产生氢气
一样多
。当等量金属与足量酸完全反应时,产生氢气的多少由金属的化合价和相对原子质量
决定;当金属的价态相同时,产生氢气的多少由相对原子质量
决定。典型例题
答案:
(1)活动性;
(2)一样多;化合价和相对原子质量;相对原子质量
(1)活动性;
(2)一样多;化合价和相对原子质量;相对原子质量
例题 如图所示的四个图像,分别对应四种过程,其中正确的是(
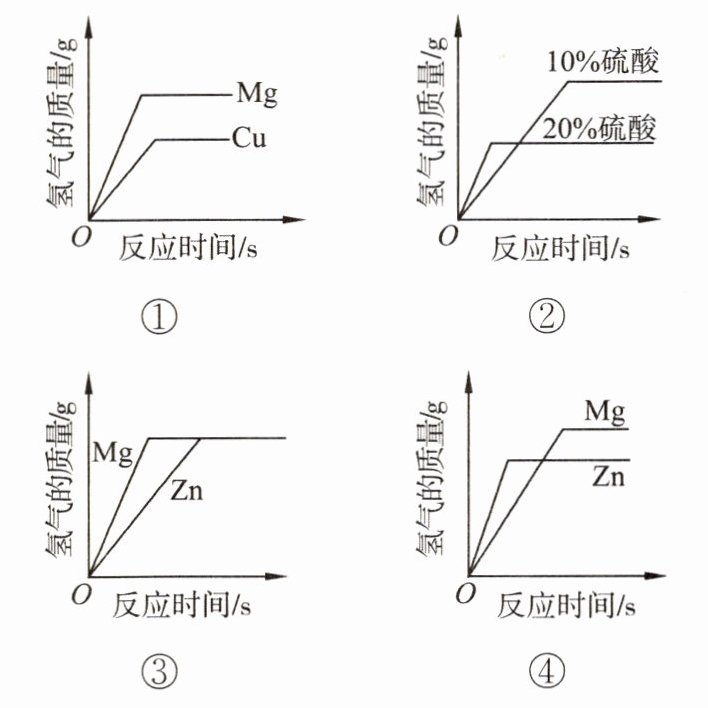
A.①分别向等质量的 Mg 和 Cu 中加入等质量、等浓度且足量的稀硫酸
B.②分别向等质量且足量的 Zn 中加入等质量、不同浓度的稀硫酸
C.③分别向等质量且足量的 Mg 和 Zn 中加入等质量、等浓度的稀硫酸
D.④分别向等质量的 Mg 和 Zn 中加入等质量、等浓度且足量的稀硫酸
C
)
A.①分别向等质量的 Mg 和 Cu 中加入等质量、等浓度且足量的稀硫酸
B.②分别向等质量且足量的 Zn 中加入等质量、不同浓度的稀硫酸
C.③分别向等质量且足量的 Mg 和 Zn 中加入等质量、等浓度的稀硫酸
D.④分别向等质量的 Mg 和 Zn 中加入等质量、等浓度且足量的稀硫酸
答案:
解析:铜的金属活动性排在氢的后面,不会与稀硫酸反应生成氢气,故 A 错误;向等质量且足量的 Zn 中加入等质量、不同浓度的稀硫酸,浓度大的稀硫酸反应生成氢气多,故 B 错误;向等质量且足量的 Mg 和 Zn 中加入等质量、等浓度的稀硫酸,稀硫酸完全反应,所以生成的氢气相等,故 C 正确;镁的金属活动性比锌强,所以镁的反应速率快,故 D 错误。
答案:C
答案:C
查看更多完整答案,请扫码查看


