第96页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
7.某化学兴趣小组的同学分别设计如图所示三个实验用于验证质量守恒定律:
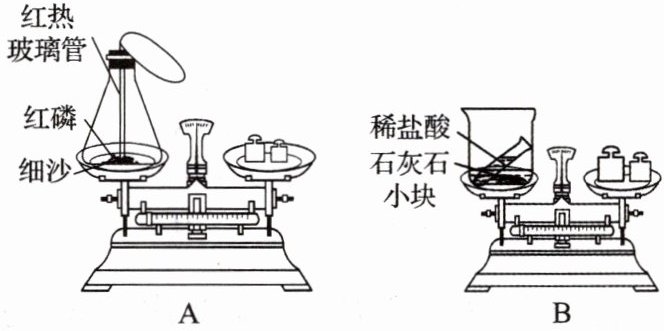
[img]
提示:CaCO₃ + 2HCl = CaCl₂ + H₂O + CO₂↑。
(1)实验A中,发生反应的化学方程式为
(2)实验B中,反应前天平平衡,然后将稀盐酸倒入烧杯中与石灰石小块充分反应后再称量,观察到反应后天平不平衡,天平指针向
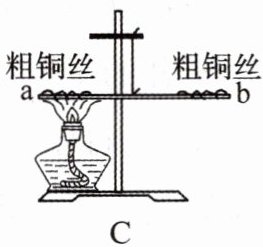
(3)如图C所示的小实验。
[img]
在一根用细铜丝吊着的长玻璃棒两端分别绕上10cm长的粗铜线,并使玻璃棒保持水平。然后,用酒精灯给左边一端铜丝加热1~2分钟。冷却后,他们观察到的现象是
①
②
(4)在三个实验中,是否有不遵循质量守恒定律的反应?

[img]
提示:CaCO₃ + 2HCl = CaCl₂ + H₂O + CO₂↑。
(1)实验A中,发生反应的化学方程式为
$4P + 5O_2\xlongequal{点燃}2P_2O_5$
,小气球的作用是平衡气压,防止橡皮塞飞出
。(2)实验B中,反应前天平平衡,然后将稀盐酸倒入烧杯中与石灰石小块充分反应后再称量,观察到反应后天平不平衡,天平指针向
右
偏转,其原因是碳酸钙和稀盐酸反应生成的二氧化碳逸出
。
(3)如图C所示的小实验。
[img]
在一根用细铜丝吊着的长玻璃棒两端分别绕上10cm长的粗铜线,并使玻璃棒保持水平。然后,用酒精灯给左边一端铜丝加热1~2分钟。冷却后,他们观察到的现象是
①
a端铜丝变黑色
②
玻璃棒a端下降,b端上升
。(4)在三个实验中,是否有不遵循质量守恒定律的反应?
否
,请从原子的角度分析质量守恒的原因反应前后原子种类、质量和总个数都不变
。
答案:
7.
(1)$4P + 5O_2\xlongequal{点燃}2P_2O_5$ 平衡气压,防止橡皮塞飞出
(2)右 碳酸钙和稀盐酸反应生成的二氧化碳逸出
(3)①a端铜丝变黑色 ②玻璃棒a端下降,b端上升
(4)否 反应前后原子种类、质量和总个数都不变
(1)$4P + 5O_2\xlongequal{点燃}2P_2O_5$ 平衡气压,防止橡皮塞飞出
(2)右 碳酸钙和稀盐酸反应生成的二氧化碳逸出
(3)①a端铜丝变黑色 ②玻璃棒a端下降,b端上升
(4)否 反应前后原子种类、质量和总个数都不变
8.(2023·眉山中考改编)磁铁矿石(主要成分为Fe₃O₄)是常用的炼铁原料,工业上可通过如下反应:Fe₃O₄ + 4CO $\xlongequal{高温}$ 3Fe + 4CO₂将其中的Fe₃O₄转化为Fe。
(1)Fe₃O₄中铁、氧的微观粒子数目之比为
(2)用含348吨Fe₃O₄的磁铁矿石,理论上可以炼出铁的质量是多少(写出计算过程)?
(1)Fe₃O₄中铁、氧的微观粒子数目之比为
$3:4$
;(2)用含348吨Fe₃O₄的磁铁矿石,理论上可以炼出铁的质量是多少(写出计算过程)?
答案:
8.
(1)$3:4$
(2)解:设理论上可以炼出铁的质量为$x$。$Fe_3O_4 + 4CO\xlongequal{高温}3Fe + 4CO_2$ $232$ $168$ $348\ t$ $x$ $\frac{232}{168}=\frac{348\ t}{x}$ $x = 252\ t$ 答:理论上可以炼出铁的质量为$252\ t$。
(1)$3:4$
(2)解:设理论上可以炼出铁的质量为$x$。$Fe_3O_4 + 4CO\xlongequal{高温}3Fe + 4CO_2$ $232$ $168$ $348\ t$ $x$ $\frac{232}{168}=\frac{348\ t}{x}$ $x = 252\ t$ 答:理论上可以炼出铁的质量为$252\ t$。
9.将MnO₂和KClO₃的固体混合物35.0g加热至质量不再变化为止,冷却后称得剩余固体质量为25.4g,回答下列问题:
(1)生成O₂的质量为
(2)计算反应前固体混合物中MnO₂的质量分数。(写出计算过程)
(1)生成O₂的质量为
$9.6\ g$
。(2)计算反应前固体混合物中MnO₂的质量分数。(写出计算过程)
答案:
9.
(1)$9.6\ g$
(2)解:设参加反应的氯酸钾的质量为$x$。$2KClO_3\xlongequal[{\triangle}]{MnO_2}2KCl + 3O_2\uparrow$ $245$ $96$ $x$ $9.6\ g$ $\frac{245}{96}=\frac{x}{9.6\ g}$ $x = 24.5\ g$ 反应前固体混合物中$MnO_2$的质量分数为$\frac{35\ g - 24.5\ g}{35\ g}×100\% = 30\%$。答:反应前固体混合物中$MnO_2$的质量分数为$30\%$。
(1)$9.6\ g$
(2)解:设参加反应的氯酸钾的质量为$x$。$2KClO_3\xlongequal[{\triangle}]{MnO_2}2KCl + 3O_2\uparrow$ $245$ $96$ $x$ $9.6\ g$ $\frac{245}{96}=\frac{x}{9.6\ g}$ $x = 24.5\ g$ 反应前固体混合物中$MnO_2$的质量分数为$\frac{35\ g - 24.5\ g}{35\ g}×100\% = 30\%$。答:反应前固体混合物中$MnO_2$的质量分数为$30\%$。
查看更多完整答案,请扫码查看


