第132页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
4. (2024 秋·九江月考)U 形管在化学实验中有广泛的应用,请回答下列问题。
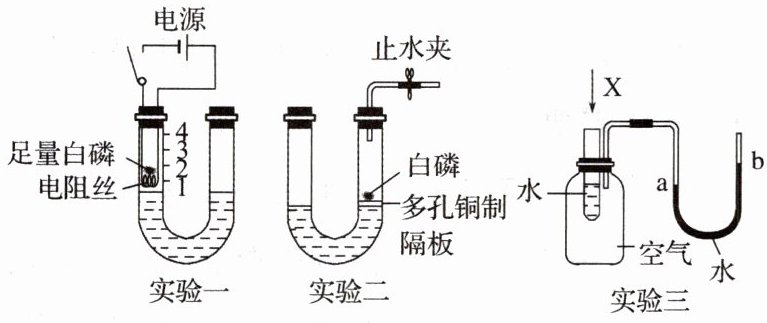
(1)白磷燃烧的化学方程式为
(2)实验一中,最终 U 形管左侧液面上升至刻度 1 附近,由此可得出的结论是
(3)实验二中,在多孔铜制隔板上放置适量的白磷,从 U 形管左侧加入 80℃的热水至浸没白磷,但白磷没有燃烧,由此可知燃烧需要的条件是
(4)实验三中,开始时 U 形管两侧液面相平,向试管中加入固体 X 后,观察到液体变化如上图所示,则 X 可能是

(1)白磷燃烧的化学方程式为
$4P + 5O₂ \xlongequal{点燃} 2P₂O₅$
。(2)实验一中,最终 U 形管左侧液面上升至刻度 1 附近,由此可得出的结论是
氧气的体积约占空气体积的五分之一
。(3)实验二中,在多孔铜制隔板上放置适量的白磷,从 U 形管左侧加入 80℃的热水至浸没白磷,但白磷没有燃烧,由此可知燃烧需要的条件是
与氧气接触
。(4)实验三中,开始时 U 形管两侧液面相平,向试管中加入固体 X 后,观察到液体变化如上图所示,则 X 可能是
氢氧化钠(合理即可)
;从分子角度解释 U 形管中液面变化的原因:分子之间的间隔变大
。
答案:
4.【解析】
(1)白磷燃烧生成五氧化二磷,反应的化学方程式为$4P + 5O₂ \xlongequal{点燃} 2P₂O₅;$
(2)白磷燃烧消耗了氧气,装置冷却到室温时,管内左侧压强减小,可观察到U形管内左侧液面上升至约1刻度处;由此可得出的结论是氧气的体积约占空气体积的五分之一;
(3)多孔铜制隔板上若放置白磷,U形管内注入80℃的热水,U形管右侧管内热水浸没白磷,此时的白磷不燃烧,原因是白磷没与氧气接触,由此可知燃烧需要的条件是与氧气接触;
(4)发现U形管中a液面比b液面低,说明容器内压强增大了,温度升高了,则试管中的固体可能是氢氧化钠;氢氧化钠溶于水放出热量,使容器内温度升高,分子之间的间隔变大,使容器内压强增大,导致U形管中a液面比b液面低。
答案:$(1)4P + 5O₂ \xlongequal{点燃} 2P₂O₅ (2)$氧气的体积约占空气体积的五分之一
(3)与氧气接触
(4)氢氧化钠(合理即可) 分子之间的间隔变大
(1)白磷燃烧生成五氧化二磷,反应的化学方程式为$4P + 5O₂ \xlongequal{点燃} 2P₂O₅;$
(2)白磷燃烧消耗了氧气,装置冷却到室温时,管内左侧压强减小,可观察到U形管内左侧液面上升至约1刻度处;由此可得出的结论是氧气的体积约占空气体积的五分之一;
(3)多孔铜制隔板上若放置白磷,U形管内注入80℃的热水,U形管右侧管内热水浸没白磷,此时的白磷不燃烧,原因是白磷没与氧气接触,由此可知燃烧需要的条件是与氧气接触;
(4)发现U形管中a液面比b液面低,说明容器内压强增大了,温度升高了,则试管中的固体可能是氢氧化钠;氢氧化钠溶于水放出热量,使容器内温度升高,分子之间的间隔变大,使容器内压强增大,导致U形管中a液面比b液面低。
答案:$(1)4P + 5O₂ \xlongequal{点燃} 2P₂O₅ (2)$氧气的体积约占空气体积的五分之一
(3)与氧气接触
(4)氢氧化钠(合理即可) 分子之间的间隔变大
5. 燃料燃烧是人类获得能量的主要来源。
(1)探究燃烧条件:
如图将三支试管(①中充满 N₂;②③中充满空气)同时放入 50℃的水中,观察到只有②中有白烟产生。
Ⅰ、对比①和②可说明
Ⅱ、对比②和③可说明
Ⅲ、气球的作用是
(2)调控燃烧:北京冬奥会火种灯如图,其创意源自青铜器精品——西汉长信宫灯。火种灯内外灯罩之间有一个导流通道,可保持火种灯外观清洁、透亮无黑烟。导流通道的作用是

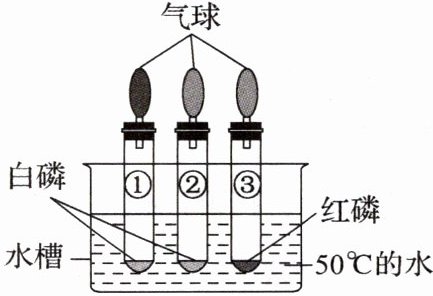
(1)探究燃烧条件:
如图将三支试管(①中充满 N₂;②③中充满空气)同时放入 50℃的水中,观察到只有②中有白烟产生。
Ⅰ、对比①和②可说明
氮气(或N₂)
不支持白磷燃烧;Ⅱ、对比②和③可说明
燃烧需要温度达到可燃物着火点
;Ⅲ、气球的作用是
平衡装置内压强
。(2)调控燃烧:北京冬奥会火种灯如图,其创意源自青铜器精品——西汉长信宫灯。火种灯内外灯罩之间有一个导流通道,可保持火种灯外观清洁、透亮无黑烟。导流通道的作用是
提供充足的氧气或空气使燃料充分燃烧
。

答案:
5.
(1)Ⅰ、氮气(或N₂) Ⅱ、燃烧需要温度达到可燃物着火点 Ⅲ、平衡装置内压强
(2)提供充足的氧气或空气使燃料充分燃烧
(1)Ⅰ、氮气(或N₂) Ⅱ、燃烧需要温度达到可燃物着火点 Ⅲ、平衡装置内压强
(2)提供充足的氧气或空气使燃料充分燃烧
6. 兴趣小组对燃烧的条件进行探究。
(1)利用图 1 所示装置进行实验,观察到的现象有
Ⅰ. 试管中白磷燃烧;
Ⅱ. 水中白磷未燃烧;
Ⅲ. 试管中红磷未燃烧;
Ⅳ. 气球 a 先变大后变小。
①由现象Ⅰ、Ⅱ可推知的结论是
②由现象Ⅰ、Ⅲ可推知的结论是
③从现象Ⅳ分析:气球 a 先变大的原因是
(2)利用图 2 所示装置进行燃烧条件的进一步探究。实验测得集气瓶中氧气的体积分数随时间的变化曲线如图 3 所示。
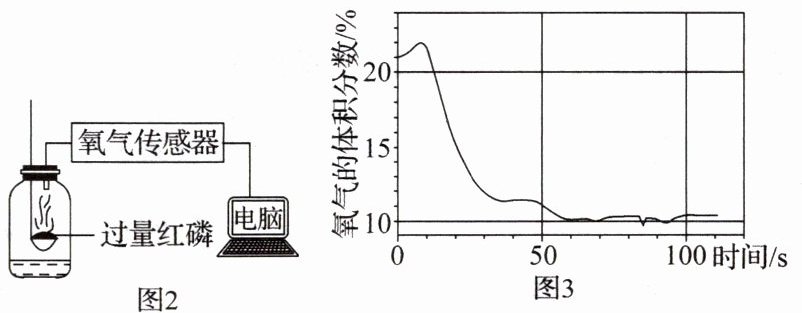
①写出红磷燃烧的化学方程式:
②红磷熄灭后,集气瓶内的氧气并未耗尽,氧气的体积分数约为 10%。你对燃烧条件的新认识是
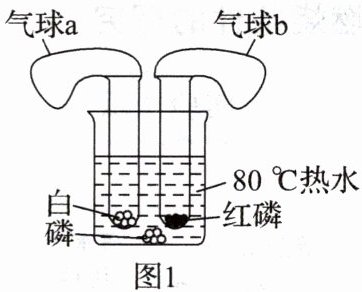
(1)利用图 1 所示装置进行实验,观察到的现象有
Ⅰ. 试管中白磷燃烧;
Ⅱ. 水中白磷未燃烧;
Ⅲ. 试管中红磷未燃烧;
Ⅳ. 气球 a 先变大后变小。
①由现象Ⅰ、Ⅱ可推知的结论是
可燃物燃烧需要与氧气接触
。②由现象Ⅰ、Ⅲ可推知的结论是
可燃物燃烧需要温度达到可燃物的着火点
。③从现象Ⅳ分析:气球 a 先变大的原因是
白磷燃烧放出热量,试管内的气体受热膨胀,使气球a变大
。(2)利用图 2 所示装置进行燃烧条件的进一步探究。实验测得集气瓶中氧气的体积分数随时间的变化曲线如图 3 所示。

①写出红磷燃烧的化学方程式:
$4P + 5O₂ \xlongequal{点燃} 2P₂O₅$
。②红磷熄灭后,集气瓶内的氧气并未耗尽,氧气的体积分数约为 10%。你对燃烧条件的新认识是
燃烧需要氧气达到一定浓度,当氧气浓度较低时,可燃物与氧气接触也不能燃烧
。
答案:
6.
(1)①可燃物燃烧需要与氧气接触
②可燃物燃烧需要温度达到可燃物的着火点 ③白磷燃烧放出热量,试管内的气体受热膨胀,使气球a变大
$(2)①4P + 5O₂ \xlongequal{点燃} 2P₂O₅ ②$燃烧需要氧气达到一定浓度,当氧气浓度较低时,可燃物与氧气接触也不能燃烧
(1)①可燃物燃烧需要与氧气接触
②可燃物燃烧需要温度达到可燃物的着火点 ③白磷燃烧放出热量,试管内的气体受热膨胀,使气球a变大
$(2)①4P + 5O₂ \xlongequal{点燃} 2P₂O₅ ②$燃烧需要氧气达到一定浓度,当氧气浓度较低时,可燃物与氧气接触也不能燃烧
查看更多完整答案,请扫码查看


