第141页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
8. (2024·吉林中考)为探究铜的化学性质,某同学借助氧气传感器在密闭装置中进行如图所示实验,观察实验现象并分析氧气含量随时间变化的曲线图。其中终点 D(203, 6.15%)表示时间为 203 秒时,装置中氧气含量为 6.15%。结合图示判断下列说法错误的是(
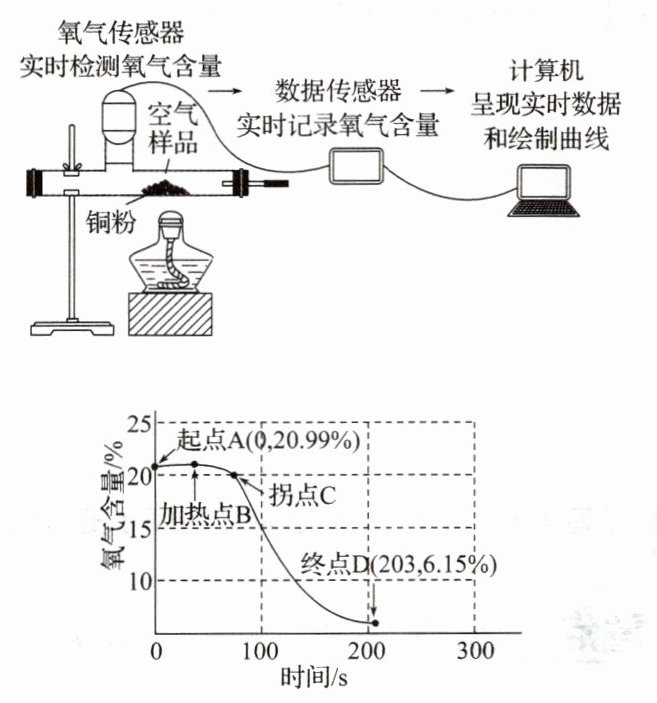
A.加热前的空气样品中氧气含量为 20.99%
B.铜在加热条件下能与氧气发生化学反应
C.拐点 C 至终点 D 所对应的时间范围内,装置内物质的总质量逐渐减少
D.通过现象证据和数据证据,可以从定性和定量的视角分析得出合理解释
C
)
A.加热前的空气样品中氧气含量为 20.99%
B.铜在加热条件下能与氧气发生化学反应
C.拐点 C 至终点 D 所对应的时间范围内,装置内物质的总质量逐渐减少
D.通过现象证据和数据证据,可以从定性和定量的视角分析得出合理解释
答案:
8.C
9. 生铁和钢都是铁和碳的合金,生铁含碳量为 2%~4.3%,钢含碳量为 0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取 11.5 g 铁合金样品盛放到锥形瓶中,将 100 g 稀盐酸分成 5 等份,分 5 次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
【查阅资料】碳不与稀盐酸反应。请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为
(2)实验数据表中 m 的值为
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到 0.1%)。
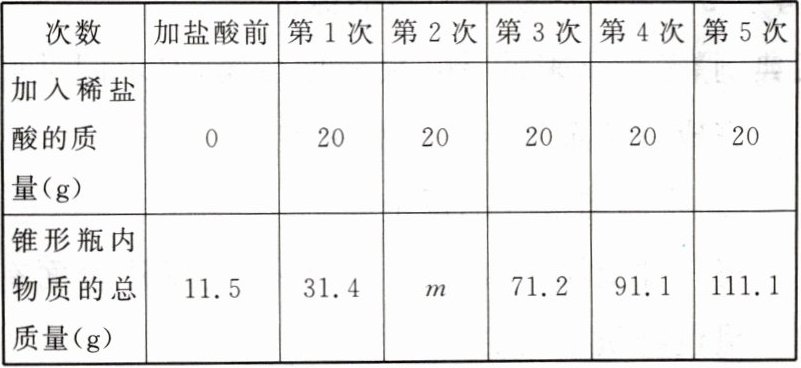
【查阅资料】碳不与稀盐酸反应。请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为
0.4g
。(2)实验数据表中 m 的值为
51.3
。(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到 0.1%)。

答案:
9.【解析】
(1)根据质量守恒定律,该反应中生成气体的总质量为$100g + 11.5g - 111.1g = 0.4g$;
(2)第一次减少的质量为$20g + 11.5g - 31.4g = 0.1g$,第三次减少的质量为$60g + 11.5g - 71.2g = 0.3g$,所以第二次减少的质量为$0.2g$,所以$40g + 11.5g - m = 0.2g$,$m = 51.3g$;
(3)解:设该铁合金中铁的质量为$x$,
$Fe + 2HCl \longrightarrow FeCl_2 + H_2\uparrow$
$56$ $2$
$x$ $0.4g$
$\frac{56}{2} = \frac{x}{0.4g}$ $x = 11.2g$,
合金中碳的质量为$11.5g - 11.2g = 0.3g$,
合金中碳的质量分数为$\frac{0.3g}{11.5g} × 100\% \approx 2.6\%$,$2.6\%$介于$2\% \sim 4.3\%$,该铁合金属于生铁。
答:该铁合金是生铁。
答案:
(1)$0.4g$
(2)$51.3$
(3)解:设该铁合金中铁的质量为$x$,
$Fe + 2HCl \longrightarrow FeCl_2 + H_2\uparrow$
$56$ $2$
$x$ $0.4g$
$\frac{56}{2} = \frac{x}{0.4g}$ $x = 11.2g$,
合金中碳的质量为$11.5g - 11.2g = 0.3g$,
合金中碳的质量分数为$\frac{0.3g}{11.5g} × 100\% \approx 2.6\%$,$2.6\%$介于$2\% \sim 4.3\%$,该铁合金属于生铁。
答:该铁合金是生铁。
(1)根据质量守恒定律,该反应中生成气体的总质量为$100g + 11.5g - 111.1g = 0.4g$;
(2)第一次减少的质量为$20g + 11.5g - 31.4g = 0.1g$,第三次减少的质量为$60g + 11.5g - 71.2g = 0.3g$,所以第二次减少的质量为$0.2g$,所以$40g + 11.5g - m = 0.2g$,$m = 51.3g$;
(3)解:设该铁合金中铁的质量为$x$,
$Fe + 2HCl \longrightarrow FeCl_2 + H_2\uparrow$
$56$ $2$
$x$ $0.4g$
$\frac{56}{2} = \frac{x}{0.4g}$ $x = 11.2g$,
合金中碳的质量为$11.5g - 11.2g = 0.3g$,
合金中碳的质量分数为$\frac{0.3g}{11.5g} × 100\% \approx 2.6\%$,$2.6\%$介于$2\% \sim 4.3\%$,该铁合金属于生铁。
答:该铁合金是生铁。
答案:
(1)$0.4g$
(2)$51.3$
(3)解:设该铁合金中铁的质量为$x$,
$Fe + 2HCl \longrightarrow FeCl_2 + H_2\uparrow$
$56$ $2$
$x$ $0.4g$
$\frac{56}{2} = \frac{x}{0.4g}$ $x = 11.2g$,
合金中碳的质量为$11.5g - 11.2g = 0.3g$,
合金中碳的质量分数为$\frac{0.3g}{11.5g} × 100\% \approx 2.6\%$,$2.6\%$介于$2\% \sim 4.3\%$,该铁合金属于生铁。
答:该铁合金是生铁。
10. 兴趣小组同学探究金属和酸反应,进行实验:在烧瓶中分别加入等质量的镁粉、铁粉、锌粉和足量的等浓度的稀盐酸,塞紧瓶塞(如图甲所示),利用传感器记录 160 s 内烧瓶中气压变化,得到相关曲线如图乙所示。下列分析正确的是(
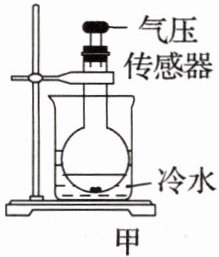
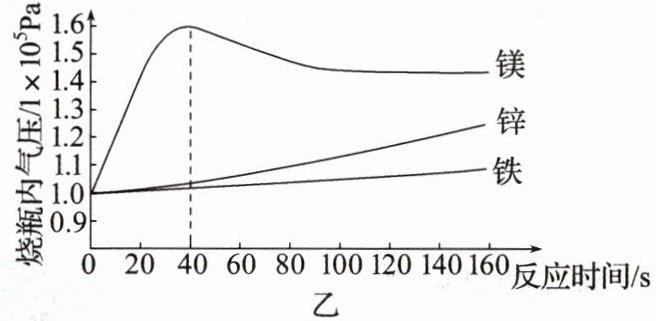
A.金属完全反应后生成氢气的质量相等
B.加入锌粉的烧瓶内气压一定大于加入铁粉的烧瓶内气压
C.0~40 s,镁与稀盐酸反应使烧瓶内气压增大的原因主要是反应放热
D.镁和稀盐酸反应的化学方程式为 Mg + 2HCl = MgCl₂ + H₂↑
D
)

A.金属完全反应后生成氢气的质量相等
B.加入锌粉的烧瓶内气压一定大于加入铁粉的烧瓶内气压
C.0~40 s,镁与稀盐酸反应使烧瓶内气压增大的原因主要是反应放热
D.镁和稀盐酸反应的化学方程式为 Mg + 2HCl = MgCl₂ + H₂↑
答案:
10.D
查看更多完整答案,请扫码查看


