2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第45页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
学思用 1. (1) 写出HF水溶液中存在的氢键:
F—H…F—、O—H…F—、F—H…O—、O—H…O—
。
答案:
F—H…F—、O—H…F—、F—H…O—、O—H…O—
(2) 下列几种氢键:①O—H…O—;②N—H…N—;③F—H…F—;④O—H…N—,由强到弱的顺序是
③①④②
(填序号)。
答案:
③①④②
学思用 2. 甲酸可通过氢键形成二聚物$,HNO_3$可形成分子内氢键。试在图中画出氢键。
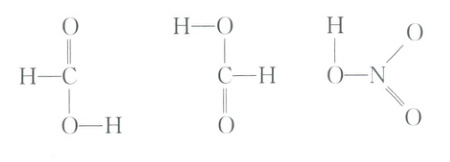

(甲酸二聚物氢键示意图:两个HCOOH分子中,一个分子的-OH的H与另一个分子C=O的O以虚线连接,形成两个氢键;HNO₃分子内氢键:-OH的H与-NO₂中的一个O以虚线连接)
答案:
(甲酸二聚物氢键示意图:两个HCOOH分子中,一个分子的-OH的H与另一个分子C=O的O以虚线连接,形成两个氢键;HNO₃分子内氢键:-OH的H与-NO₂中的一个O以虚线连接)
⑱高于 ⑲高 ⑳低于 ㉑增大 ㉒易
⑱高于 ⑲高 ⑳低于 ㉑增大 ㉒易
3. 溶解性
(1) “相似相溶”的规律
非极性溶质一般能溶于㉓
(2) 影响因素
① 外界条件:主要有㉙
② 氢键:如果存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越㉛
③ 分子结构的相似性:溶质和溶剂的分子结构相似程度越大,其溶解性越㉜
(1) “相似相溶”的规律
非极性溶质一般能溶于㉓
非极性
溶剂,极性溶质一般能溶于㉔极性
溶剂。例如,蔗糖和氨㉕易
溶于水,㉖难
溶于四氯化碳;萘和碘㉗易
溶于四氯化碳,㉘难
溶于水。(2) 影响因素
① 外界条件:主要有㉙
温度
、㉚压强
等。② 氢键:如果存在氢键,则溶剂和溶质之间的氢键作用力越大,溶解性越㉛
好
。③ 分子结构的相似性:溶质和溶剂的分子结构相似程度越大,其溶解性越㉜
好
。例如,乙醇能与水互溶,而戊醇在水中的溶解度明显减小。
答案:
㉓非极性 ㉔极性 ㉕易 ㉖难 ㉗易 ㉘难 ㉙温度 ㉚压强 ㉛好 ㉜好
学思用 3. (1) 你能利用“相似相溶”的规律解释$NH_3$和$CH_4$在水中的溶解度的不同吗?
NH₃为极性分子,CH₄为非极性分子,而水是极性分子,根据“相似相溶”的规律,NH₃易溶于水,而CH₄难溶于水,且NH₃与水分子之间可形成氢键,使得NH₃更易溶于水。
答案:
NH₃为极性分子,CH₄为非极性分子,而水是极性分子,根据“相似相溶”的规律,NH₃易溶于水,而CH₄难溶于水,且NH₃与水分子之间可形成氢键,使得NH₃更易溶于水。
(2) 如何理解低碳醇与水互溶,而高碳醇在水中的溶解度却很小?
低碳醇中的烷基较小,分子中的—OH与水分子中的—OH相似,因而低碳醇能与水互溶;而高碳醇中的烷基较大,分子中的—OH与水分子中的—OH相似因素少,因而高碳醇在水中的溶解度明显减小。
答案:
低碳醇中的烷基较小,分子中的—OH与水分子中的—OH相似,因而低碳醇能与水互溶;而高碳醇中的烷基较大,分子中的—OH与水分子中的—OH相似因素少,因而高碳醇在水中的溶解度明显减小。
查看更多完整答案,请扫码查看


