2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第30页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
1. 键长是描述共价键的物理量之一。下列各项中的距离属于键长的是(
A.水分子中两个氢原子核之间的距离
B.氯气分子中两个氯原子核之间的距离
C.氩气中两个相邻氩原子核间的距离
$D.CO_2$分子中两个氧原子核之间的距离
B
)A.水分子中两个氢原子核之间的距离
B.氯气分子中两个氯原子核之间的距离
C.氩气中两个相邻氩原子核间的距离
$D.CO_2$分子中两个氧原子核之间的距离
答案:
解析:选 B。键长是成键原子的核间距。水分子中两个氢原子间不成键,A 不符合题意;氯气分子中两个氯原子间形成共价键,两个氯原子核之间的距离属于键长,B 符合题意;氩气中两个相邻氩原子间不成键,C 不符合题意;CO₂分子中两个氧原子间不成键,D 不符合题意。
2. 已知X—X、Y—Y、Z—Z的键长分别为198 pm、74 pm、154 pm。则它们单质分子的稳定性大小关系为(
$A. X_2 > Y_2 > Z_2$
$B. Z_2 > Y_2 > X_2$
$C. Y_2 > X_2 > Z_2$
$D. Y_2 > Z_2 > X_2$
D
)$A. X_2 > Y_2 > Z_2$
$B. Z_2 > Y_2 > X_2$
$C. Y_2 > X_2 > Z_2$
$D. Y_2 > Z_2 > X_2$
答案:
解析:选 D。共价键的键长越短,键能越大,共价键越牢固,形成的分子也越稳定,而三种共价键的键长由短到长的顺序为 Y—Y<Z—Z<X—X,故三种单质分子的稳定性大小关系为 Y₂>Z₂>X₂。
3. (教材习题改编)人们常用HX表示卤化氢(X代表F、Cl、Br、I)。下列说法正确的是(
A.键长的数值可通过晶体的X射线衍射实验获得
B.H—F的键长是H—X中最长的
C.H—F中含有p - p σ键
D.H—F的键能是H—X中最小的
A
)A.键长的数值可通过晶体的X射线衍射实验获得
B.H—F的键长是H—X中最长的
C.H—F中含有p - p σ键
D.H—F的键能是H—X中最小的
答案:
解析:选 A。F、Cl、Br、I 中,F 的原子半径最小,H—F 的键长是 H—X 中最短的,B 错误;H—F 是 H 原子的 1s 轨道与 F 原子的 2p 轨道“头碰头”重叠形成的,是 s-p σ 键,C 错误;一般情况下,键长越短,键能越大,H—F 的键长是 H—X 中最短的,故 H—F 的键能是 H—X 中最大的,D 错误。
1. 概念:在多原子分子中,①
两个相邻共价键
之间的夹角。键角的数值可通过晶体的②X 射线衍射
实验获得。
答案:
①两个相邻共价键 ②X 射线衍射
2. 应用:多原子分子的键角一定,表明共价键具有③
方向
性。键角是描述分子④空间结构
的重要参数。
答案:
③方向 ④空间结构
3. 根据分子的空间结构判断键角
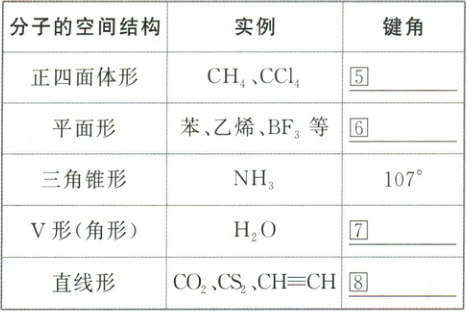

⑤109°28' ⑥120° ⑦105° ⑧180°
答案:
⑤109°28' ⑥120° ⑦105° ⑧180°
(1) 实验测得$H_2S$为共价化合物,H—S—H的夹角为92.3°,键长相同。$H_2S$的空间结构是什么?
V 形
答案:
V 形。
(2) 白磷和甲烷均为正四面体结构,结构如下图所示:
 它们的键角是否相同,为什么?
它们的键角是否相同,为什么?
 它们的键角是否相同,为什么?
它们的键角是否相同,为什么?不同,白磷分子的键角是指相邻 P—P 之间的夹角,为 60°;而甲烷分子的键角是指 H—C—H 的夹角,为 109°28'。
答案:
不同,白磷分子的键角是指相邻 P—P 之间的夹角,为 60°;而甲烷分子的键角是指 H—C—H 的夹角,为 109°28'。
自我诊断
(1) 分子的空间结构是由键角决定的(
(2) O = C = O和H—O—H的键角都为180°(
$(3) NH_3$分子中两个N—H的夹角为120°(
$(4) CH_4$和$CH_3Cl$分子的空间结构都是正四面体形(
(1) 分子的空间结构是由键角决定的(
× 键长和键角共同决定分子的空间结构
)(2) O = C = O和H—O—H的键角都为180°(
× CO₂是直线形分子,O=C=O 的键角为 180°;H₂O 是 V 形分子,H—O—H 的键角为 105°
)$(3) NH_3$分子中两个N—H的夹角为120°(
× NH₃分子中两个 N—H 的夹角为 107°
)$(4) CH_4$和$CH_3Cl$分子的空间结构都是正四面体形(
× CH₃Cl 分子的空间结构是四面体形
)
答案:
(1)× 键长和键角共同决定分子的空间结构
(2)× CO₂是直线形分子,O=C=O 的键角为 180°;H₂O 是 V 形分子,H—O—H 的键角为 105°
(3)× NH₃分子中两个 N—H 的夹角为 107°
(4)× CH₃Cl 分子的空间结构是四面体形
(1)× 键长和键角共同决定分子的空间结构
(2)× CO₂是直线形分子,O=C=O 的键角为 180°;H₂O 是 V 形分子,H—O—H 的键角为 105°
(3)× NH₃分子中两个 N—H 的夹角为 107°
(4)× CH₃Cl 分子的空间结构是四面体形
查看更多完整答案,请扫码查看


