2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第37页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
5. (教材习题改编)根据价层电子对互斥模型填写下表(加“·”的原子为中心原子):
|分子或离子|σ键电子对数|孤电子对数|空间结构|
|----|----|----|----|
|H₂Se|
|SCl₂|
|PCl₃|
|BH₄⁻|
|OF₂|
|ClF₂⁺|
|分子或离子|σ键电子对数|孤电子对数|空间结构|
|----|----|----|----|
|H₂Se|
2
|2
|V形
||SCl₂|
2
|2
|V形
||PCl₃|
3
|1
|三角锥形
||BH₄⁻|
4
|0
|正四面体形
||OF₂|
2
|2
|V形
||ClF₂⁺|
2
|2
|V形
|
答案:
|分子或离子|σ键电子对数|孤电子对数|空间结构|
|H₂Se|2|2|V形|
|SCl₂|2|2|V形|
|PCl₃|3|1|三角锥形|
|BH₄⁻|4|0|正四面体形|
|OF₂|2|2|V形|
|ClF₂⁺|2|2|V形|
|H₂Se|2|2|V形|
|SCl₂|2|2|V形|
|PCl₃|3|1|三角锥形|
|BH₄⁻|4|0|正四面体形|
|OF₂|2|2|V形|
|ClF₂⁺|2|2|V形|
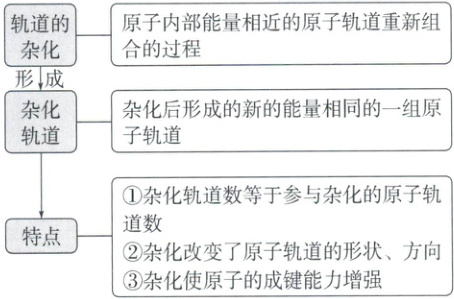
1. 杂化轨道的形成及特点
轨道的杂化:原子内部能量相近的原子轨道重新组合的过程
形成杂化轨道:杂化后形成的新的能量相同的一组原子轨道
特点:
杂化轨道数等于参与杂化的原子轨道数
杂化改变了原子轨道的形状、方向
杂化使原子的成键能力增强
轨道的杂化:原子内部能量相近的原子轨道重新组合的过程
形成杂化轨道:杂化后形成的新的能量相同的一组原子轨道
特点:
杂化轨道数等于参与杂化的原子轨道数
杂化改变了原子轨道的形状、方向
杂化使原子的成键能力增强

答案:
题目内容为杂化轨道理论的基础概念陈述,无具体问题需选择或填空,若为判断上述内容正确性,则均正确。
2. 杂化轨道类型及其空间结构
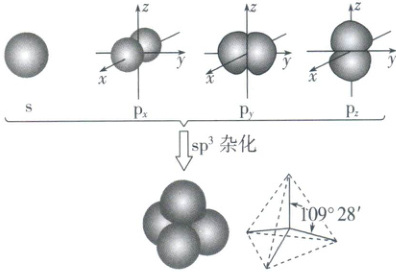
(1)$sp^3$杂化——正四面体形
$sp^3$杂化轨道由①
(2)$sp^2$杂化——平面三角形
$sp^2$杂化轨道由⑤

(3)$sp$杂化——直线形
$sp$杂化轨道由⑨

(1)$sp^3$杂化——正四面体形
$sp^3$杂化轨道由①
1
个$s$轨道和②3
个$p$轨道杂化而得,每个$sp^3杂化轨道都含有\frac{1}{4}s轨道的成分和\frac{3}{4}p$轨道的成分,$sp^3$杂化轨道间的夹角为③$109^{\circ }28'$
,空间结构为④正四面体形
。如下图所示:
(2)$sp^2$杂化——平面三角形
$sp^2$杂化轨道由⑤
1
个$s$轨道和⑥2
个$p$轨道杂化而得,每个$sp^2杂化轨道都含有\frac{1}{3}s轨道的成分和\frac{2}{3}p$轨道的成分,$sp^2$杂化轨道间的夹角为⑦$120^{\circ }$
,空间结构为⑧平面三角形
。如下图所示:
(3)$sp$杂化——直线形
$sp$杂化轨道由⑨
1
个$s$轨道和⑩1
个$p$轨道杂化而得,每个$sp杂化轨道都含有\frac{1}{2}s轨道的成分和\frac{1}{2}p$轨道的成分,$sp$杂化轨道间的夹角为⑪$180^{\circ }$
,空间结构为⑫直线形
。如下图所示:
答案:
①1 ②3 ③$109^{\circ }28'$ ④正四面体形 ⑤1 ⑥2 ⑦$120^{\circ }$ ⑧平面三角形 ⑨1 ⑩1 ⑪$180^{\circ }$ ⑫直线形
查看更多完整答案,请扫码查看


