2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年新坐标同步练习高中化学选择性必修第二册人教版青海专版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第26页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
1. 下列不属于共价键成键因素的是(
A.共用电子对在两原子核之间高概率出现
B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定
D.两原子体积大小要适中
D
)A.共用电子对在两原子核之间高概率出现
B.共用的电子必须配对
C.成键后体系能量降低,趋于稳定
D.两原子体积大小要适中
答案:
解析:选D。两原子形成共价键时,原子轨道在两个原子核间重叠,即电子在两原子核之间出现的概率更大;两原子的原子轨道重叠越多,共价键越牢固,体系的能量也越低;原子的体积大小与能否形成共价键无必然联系。
2. 从电负性变化规律的角度来判断下列元素的原子之间易形成共价键的是(
A.K和Cl
B.H和F
C.K和F
D.Ca和O
B
)A.K和Cl
B.H和F
C.K和F
D.Ca和O
答案:
解析:选B。一般电负性相差不大的非金属元素原子之间易形成共价键。
3. 下列说法正确的是(
A.$Cl_2$是双原子分子,$H_2S$是三原子分子,这是由共价键的方向性决定的
B.$H_2O与H_2S$的空间结构一样,这是由共价键的饱和性决定的
C.并非所有的共价键都有方向性
D.两原子轨道发生重叠后,电子在两核间出现的概率减小
C
)A.$Cl_2$是双原子分子,$H_2S$是三原子分子,这是由共价键的方向性决定的
B.$H_2O与H_2S$的空间结构一样,这是由共价键的饱和性决定的
C.并非所有的共价键都有方向性
D.两原子轨道发生重叠后,电子在两核间出现的概率减小
答案:
解析:选C。Cl₂是双原子分子,H₂S是三原子分子,这是由共价键的饱和性决定的,A不正确;H₂O与H₂S的空间结构一样,这是由共价键的方向性决定的,B不正确;H₂中的共价键没有方向性,C正确;两原子轨道发生重叠后,电子在两核间出现的概率增大,D不正确。
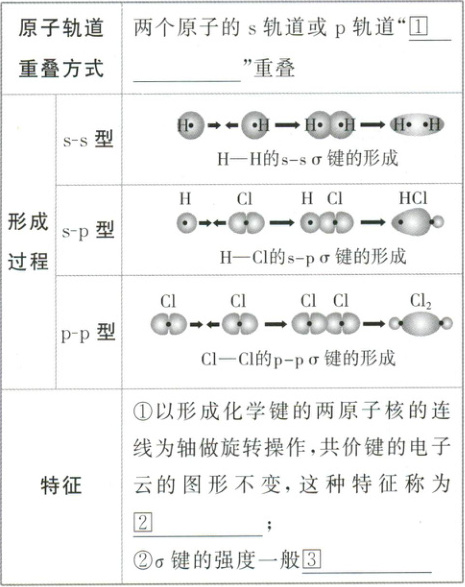
1. σ键
2. π键



2. π键


1.①头碰头 ②轴对称 ③较大 2.④肩并肩
答案:
1.①头碰头 ②轴对称 ③较大 2.④肩并肩
|形成过程| p-p π键的形成|
|特征|①每个π键的电子云由两块组成,它们互为镜像,这种特征称为⑤
②π键不能绕键轴旋转;一般不如σ键牢固,比较容易断裂|
学思用 1. 画出氮原子的轨道表示式,并说明氮气分子中的 $N\equivN$ 是由哪些类型的共价键构成的。
|特征|①每个π键的电子云由两块组成,它们互为镜像,这种特征称为⑤
镜面对称
;②π键不能绕键轴旋转;一般不如σ键牢固,比较容易断裂|
学思用 1. 画出氮原子的轨道表示式,并说明氮气分子中的 $N\equivN$ 是由哪些类型的共价键构成的。
答案:
⑤镜面对称
3. 判断σ键、π键的一般规律
共价单键是⑥
学思用 2. 观察下图乙烷、乙烯和乙炔分子的结构,并回答下列问题。

(1) 它们的分子中的共价键分别由几个σ键和几个π键构成?
(2) 乙烯和乙炔的化学性质为什么比乙烷活泼?
(3) “在气体单质分子中,一定含有σ键,可能含有π键”,这种说法对吗?为什么?
共价单键是⑥
σ
键;而共价双键中有一个⑦σ
键,另一个是⑧π
键;共价三键由一个⑨σ
键和两个⑩π
键构成。学思用 2. 观察下图乙烷、乙烯和乙炔分子的结构,并回答下列问题。

(1) 它们的分子中的共价键分别由几个σ键和几个π键构成?
(2) 乙烯和乙炔的化学性质为什么比乙烷活泼?
(3) “在气体单质分子中,一定含有σ键,可能含有π键”,这种说法对吗?为什么?
答案:
3.⑥σ ⑦σ ⑧π ⑨σ ⑩π
查看更多完整答案,请扫码查看


