第5页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
9. 「2025杭州萧山八校期中,★☆」将表面布满铁锈(铁锈的主要成分是$Fe_2O_3)$的铁钉放入盛有稀硫酸的密闭容器中,用压强传感器测得容器内压强随时间的变化曲线如图所示。下列分析正确的是(
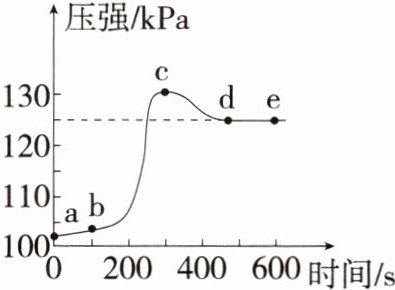
A. d点时$H_2SO_4$反应完,且温度高于a点
B. 整个反应过程,溶液中$SO_4^2⁻$逐渐减少
C. 当压强为115kPa时,溶液中的溶质只有$FeSO_4$
D. cd段压强减小是因为铁和稀硫酸反应结束,不再放热
D
)
A. d点时$H_2SO_4$反应完,且温度高于a点
B. 整个反应过程,溶液中$SO_4^2⁻$逐渐减少
C. 当压强为115kPa时,溶液中的溶质只有$FeSO_4$
D. cd段压强减小是因为铁和稀硫酸反应结束,不再放热
答案:
D 将表面布满铁锈的铁钉放入盛有稀硫酸的密闭容器中,稀硫酸先与氧化铁反应生成硫酸铁和水,此过程中没有气体产生,气压基本不变;当氧化铁反应完后,铁再与稀硫酸反应生成硫酸亚铁和氢气,且反应放热,故气压增大;c点时,反应停止,压强达到最大值,之后热量散失,温度降低至室温,压强减小到d点,则d点温度与a点相等,A错误。整个反应过程中发生的反应有Fe₂O₃ + 3H₂SO₄ = Fe₂(SO₄)₃ + 3H₂O、Fe + H₂SO₄ = FeSO₄ + H₂↑,溶液中硫酸根离子的数目没有发生变化,B错误。当压强为115kPa时,此时氧化铁与稀硫酸已反应完,铁与稀硫酸的反应在进行中,故溶液中的溶质有硫酸铁、硫酸亚铁和硫酸三种,C错误。影响cd段压强变化的主要因素是温度,是因为完全反应后温度降低,压强减小,D正确。
10. 新课标探究实践在研究硫酸的性质实验中,同学们分别进行了如下三个实验:
(1)图1是某同学在实验室用稀硫酸与锌混合制取氢气的装置。装置中出现
(2)稀硫酸与含少量氧化铁的铁粉反应实验:如图2中甲是反应的实验装置(装置气密性良好),其中U形管中红墨水变化情况(如图2中乙所示)符合该实验的是
(3)氢氧化钠溶液与稀硫酸反应实验:氢氧化钠溶液与稀硫酸反应无明显现象。为了证明氢氧化钠溶液与稀硫酸确实发生了化学反应,进行了如图3所示实验(硫酸钠溶液显中性):
取2mL氢氧化钠溶液于试管中,滴入1~2滴酚酞试液,振荡。然后逐滴加入足量稀硫酸,同时不断振荡试管,整个实验过程的现象是
(1)图1是某同学在实验室用稀硫酸与锌混合制取氢气的装置。装置中出现
3
处错误。若按照上述装置制取氢气,会造成的后果是无法收集到气体,锥形瓶内压强过大,弹开瓶塞(合理即可)
。(2)稀硫酸与含少量氧化铁的铁粉反应实验:如图2中甲是反应的实验装置(装置气密性良好),其中U形管中红墨水变化情况(如图2中乙所示)符合该实验的是
Ⅲ
(填写序号),理由是稀硫酸与铁反应产生氢气并放热,装置内的气压增大,U形管左边液面下降,反应结束恢复至室温后,U形管内左右两侧液面差程度可能较反应进行中的某一时刻要小
。(3)氢氧化钠溶液与稀硫酸反应实验:氢氧化钠溶液与稀硫酸反应无明显现象。为了证明氢氧化钠溶液与稀硫酸确实发生了化学反应,进行了如图3所示实验(硫酸钠溶液显中性):
取2mL氢氧化钠溶液于试管中,滴入1~2滴酚酞试液,振荡。然后逐滴加入足量稀硫酸,同时不断振荡试管,整个实验过程的现象是
溶液先由无色变为红色,再由红色变为无色
。由此证明,上述实验过程确实发生了化学反应,该反应的化学方程式为2NaOH + H₂SO₄ = Na₂SO₄ + 2H₂O
。
答案:
答案 (1)3 无法收集到气体,锥形瓶内压强过大,弹开瓶塞(合理即可) (2)Ⅲ 稀硫酸与铁反应产生氢气并放热,装置内的气压增大,U形管左边液面下降,反应结束恢复至室温后,U形管内左右两侧液面差程度可能较反应进行中的某一时刻要小 (3)溶液先由无色变为红色,再由红色变为无色 2NaOH + H₂SO₄ = Na₂SO₄ + 2H₂O
解析 (1)由题图1可知,锥形瓶内的导气管过长,不利于氢气的排出;氢气的密度比空气的小,不能用向上排空气法收集;集气瓶内的导气管过短,不利于空气的排出。(3)取2mLNaOH溶液于试管中,滴入1~2滴酚酞试液,溶液由无色变为红色;逐滴滴入足量稀硫酸,完全反应后溶液由红色变为无色,证明稀硫酸与氢氧化钠溶液发生了化学反应。
解析 (1)由题图1可知,锥形瓶内的导气管过长,不利于氢气的排出;氢气的密度比空气的小,不能用向上排空气法收集;集气瓶内的导气管过短,不利于空气的排出。(3)取2mLNaOH溶液于试管中,滴入1~2滴酚酞试液,溶液由无色变为红色;逐滴滴入足量稀硫酸,完全反应后溶液由红色变为无色,证明稀硫酸与氢氧化钠溶液发生了化学反应。
查看更多完整答案,请扫码查看


