第14页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
1. 新课标 科学观念「2025温州十七中期中」芯片设计的核心材料之一是高纯度的单质硅,以下是芯片制造中硅材料来源的一种重要方式:$2H_{2}+SiCl_{4}\xlongequal {高温}Si+4HCl$,该反应类型属于 (
A. 置换反应
B. 复分解反应
C. 化合反应
D. 分解反应
A
)A. 置换反应
B. 复分解反应
C. 化合反应
D. 分解反应
答案:
A 反应物$H_{2}$、$SiCl_{4}$分别是单质和化合物,生成物$Si$、$HCl$也分别属于单质和化合物,符合置换反应的特征,故选A。
2. 新课标 科学观念 下列关于金属与氧气反应的说法中正确的是 (
A. 细铁丝在空气中不能燃烧,是因为温度没有达到其着火点
B. 铜在空气中能与氧气发生化学反应,其化学方程式为$Cu+O_{2}= CuO$
C. “真金不怕火炼”说明即使在高温条件下金也不与氧气反应
D. 金属与氧气发生化学反应时,都需要在点燃或加热的条件下
C
)A. 细铁丝在空气中不能燃烧,是因为温度没有达到其着火点
B. 铜在空气中能与氧气发生化学反应,其化学方程式为$Cu+O_{2}= CuO$
C. “真金不怕火炼”说明即使在高温条件下金也不与氧气反应
D. 金属与氧气发生化学反应时,都需要在点燃或加热的条件下
答案:
C 细铁丝在空气中不能燃烧,是因为空气中氧气的浓度小,A错误;铜在空气中能与氧气发生化学反应,反应的化学方程式为$2Cu+O_{2}\xlongequal {△}2CuO$,B错误;“真金不怕火炼”意思是金即使在高温时也不与氧气反应,说明金的化学性质不活泼,C正确;金属与氧气发生化学反应时,不一定需要点燃或加热的条件,如铝在空气中能与氧气反应,不需要点燃或加热,D 错误。
3. 「2024安徽安师附中一模」将大小、形状相同的 Mg、Zn、Fe、Cu 四种金属同时投入盐酸中,下列结论不正确的是 (

A. 铜不能与盐酸发生反应
B. 四种金属中与盐酸反应最剧烈的是 Mg
C. 相等质量的锌和铁分别与足量盐酸反应,生成$H_{2}$的质量:$Zn>Fe$
D. 如果把盐酸换成稀硫酸,实验现象相同
C
)
A. 铜不能与盐酸发生反应
B. 四种金属中与盐酸反应最剧烈的是 Mg
C. 相等质量的锌和铁分别与足量盐酸反应,生成$H_{2}$的质量:$Zn>Fe$
D. 如果把盐酸换成稀硫酸,实验现象相同
答案:
C 相等质量的锌和铁分别与足量盐酸反应,金属反应完全,生成$H_{2}$的质量:$Zn\lt Fe$。
4. 跨物理 杠杆「2024陕西榆林榆阳二模」如图所示,杠杆的两端分别挂着打磨干净、质量相等的铁球和锌球,杠杆平衡。将两个金属球分别浸入等质量、等浓度的稀硫酸中,待不再产生气泡后,移走烧杯,两个金属球均有剩余。下列说法正确的是 (
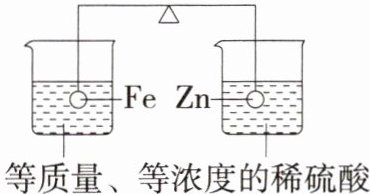
A. 两个烧杯中溶液均变为浅绿色
B. 实验开始阶段,杠杆右端下沉
C. 实验结束后,左侧烧杯中溶液质量更大
D. 移走烧杯后,要想使杠杆平衡,支点应向左移动
D
)
A. 两个烧杯中溶液均变为浅绿色
B. 实验开始阶段,杠杆右端下沉
C. 实验结束后,左侧烧杯中溶液质量更大
D. 移走烧杯后,要想使杠杆平衡,支点应向左移动
答案:
D 左侧烧杯中铁和稀硫酸反应生成硫酸亚铁和氢气,溶液变为浅绿色;右侧烧杯中锌和稀硫酸反应生成硫酸锌和氢气,溶液不变色。锌与稀硫酸的反应速率比铁快,实验开始阶段,相同时间内右侧烧杯中消耗的金属较多,杠杆左端下沉。实验结束后两个金属球均有剩余,说明稀硫酸完全反应,最终生成氢气的质量相等,消耗的锌的质量大于铁的质量,所以右侧烧杯中溶液质量比左侧烧杯中溶液质量大。因为消耗的锌的质量大于铁的质量,所以移走烧杯后,杠杆左端下沉,要想使杠杆平衡,支点应向左移动。
5. 金属与氧气反应可以生成金属氧化物。小林同学绘制了三条表示某种金属质量和其与氧气反应生成的金属氧化物质量的关系曲线,如图,请回答:
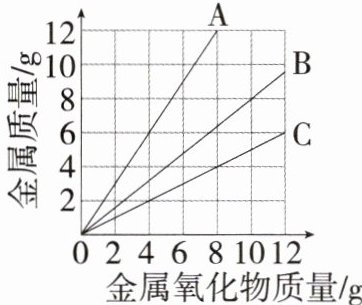
(1)曲线____
(2)三条曲线中,表示 Cu 与 CuO 质量关系的曲线是____

(1)曲线____
A
____一定是错误的。(2)三条曲线中,表示 Cu 与 CuO 质量关系的曲线是____
B
____。
答案:
答案 (1)A (2)B
解析 (1)由质量守恒定律可知,生成金属氧化物的质量一定比反应的金属的质量大,曲线A上的每一点对应的横坐标数值都小于纵坐标数值,即金属氧化物的质量小于金属的质量,不符合质量守恒定律。
(2)铜与氧气反应的化学方程式为$2Cu+O_{2}\xlongequal {△}2CuO$,参加反应的铜与生成氧化铜的质量比为$(64×2):(80×2)=4:5$,曲线B符合$Cu$与$CuO$质量关系。
解析 (1)由质量守恒定律可知,生成金属氧化物的质量一定比反应的金属的质量大,曲线A上的每一点对应的横坐标数值都小于纵坐标数值,即金属氧化物的质量小于金属的质量,不符合质量守恒定律。
(2)铜与氧气反应的化学方程式为$2Cu+O_{2}\xlongequal {△}2CuO$,参加反应的铜与生成氧化铜的质量比为$(64×2):(80×2)=4:5$,曲线B符合$Cu$与$CuO$质量关系。
6. 「2024湖南怀化鹤城模拟,★☆」现有等质量的甲、乙、丙三种金属,分别放入三份浓度相同的足量稀硫酸中,产生氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中化合价相同)。下列说法中错误的是 (
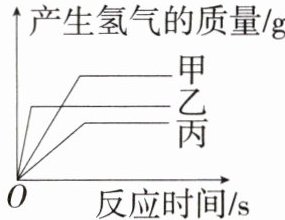
A. 反应速率:乙>甲>丙
B. 产生氢气的质量:甲>乙>丙
C. 相对原子质量:乙>丙>甲
D. 消耗硫酸的质量:甲>乙>丙
C
)
A. 反应速率:乙>甲>丙
B. 产生氢气的质量:甲>乙>丙
C. 相对原子质量:乙>丙>甲
D. 消耗硫酸的质量:甲>乙>丙
答案:
C
查看更多完整答案,请扫码查看


