第13页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
6. 实验室里有一瓶长期敞口放置的氢氧化钙粉末,小实为测定该瓶粉末是否变质及变质程度,进行如下实验操作:
步骤一:小实取2克样品放入烧杯中,加10克水,有固体未溶。
步骤二:过滤,取滤液加入无色酚酞,溶液变红。
步骤三:在滤渣中加入过量盐酸,有气泡生成。
(1)不能通过步骤一判断该瓶粉末已变质,理由是
(2)通过以上实验,可以得出的结论是
(3)若瓶内未变质前的氢氧化钙,与质量为$m_1$的HCl恰好完全反应,当氢氧化钙变质后,恰好完全反应需要消耗HCl的质量为$m_2,$则$m_2$
步骤一:小实取2克样品放入烧杯中,加10克水,有固体未溶。
步骤二:过滤,取滤液加入无色酚酞,溶液变红。
步骤三:在滤渣中加入过量盐酸,有气泡生成。
(1)不能通过步骤一判断该瓶粉末已变质,理由是
氢氧化钙微溶于水
。(2)通过以上实验,可以得出的结论是
氢氧化钙粉末部分变质
。(3)若瓶内未变质前的氢氧化钙,与质量为$m_1$的HCl恰好完全反应,当氢氧化钙变质后,恰好完全反应需要消耗HCl的质量为$m_2,$则$m_2$
=
$m_1($填“>”“<”或“=”)。
答案:
答案 (1)氢氧化钙微溶于水 (2)氢氧化钙粉末部分变质 (3)=
解析 (1)氢氧化钙微溶于水,未溶物可能是氢氧化钙。(2)滤液中加入无色酚酞,溶液变红,说明溶液中含有氢氧化钙。在滤渣中加入过量盐酸,有气泡生成,说明其中含有碳酸钙。通过以上实验,可以得出氢氧化钙粉末部分变质。
解析 (1)氢氧化钙微溶于水,未溶物可能是氢氧化钙。(2)滤液中加入无色酚酞,溶液变红,说明溶液中含有氢氧化钙。在滤渣中加入过量盐酸,有气泡生成,说明其中含有碳酸钙。通过以上实验,可以得出氢氧化钙粉末部分变质。
7. 「2024山东滨州滨城一模」研究性学习小组测定实验室里一瓶久置的NaOH固体是否变质。
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是
猜想3:部分变质,既含有NaOH,又含有$Na_2CO_3。$
【设计方案并进行实验】请你与他们一起完成,并回答所给问题。
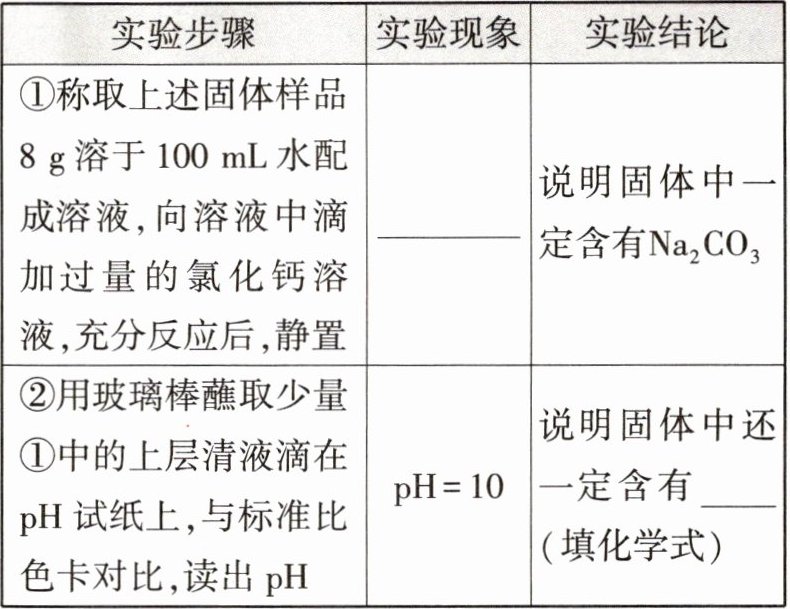
上述步骤①中,滴加过量氯化钙溶液的目的是
【实验结论】通过实验,说明猜想
【拓展】要除去氢氧化钠中含有的碳酸钠,所用的方法是
【提出问题】NaOH固体是否变质?
【猜想与假设】猜想1:没变质,全部是NaOH;
猜想2:全变质,全部是
Na₂CO₃
;猜想3:部分变质,既含有NaOH,又含有$Na_2CO_3。$
【设计方案并进行实验】请你与他们一起完成,并回答所给问题。

上述步骤①中,滴加过量氯化钙溶液的目的是
检验Na₂CO₃并使样品中的Na₂CO₃完全反应
。【实验结论】通过实验,说明猜想
3
正确。【拓展】要除去氢氧化钠中含有的碳酸钠,所用的方法是
Na₂CO₃+Ca(OH)₂=CaCO₃↓+2NaOH
(用化学方程式表示)。
答案:
答案 【猜想与假设】Na₂CO₃ 【设计方案并进行实验】产生白色沉淀 NaOH 检验Na₂CO₃并使样品中的Na₂CO₃完全反应 【实验结论】3
【拓展】Na₂CO₃+Ca(OH)₂=CaCO₃↓+2NaOH(合理即可)
解析 【设计方案并进行实验】由实验结论为含有碳酸钠可知,现象为产生白色沉淀。步骤①中滴加过量CaCl₂溶液,目的是检验Na₂CO₃并使碳酸钠完全反应。滴入过量的CaCl₂溶液后,测得溶液的pH=10,则说明原固体中含有NaOH。【拓展】碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,可用适量氢氧化钙溶液除去氢氧化钠中含有的碳酸钠。
【拓展】Na₂CO₃+Ca(OH)₂=CaCO₃↓+2NaOH(合理即可)
解析 【设计方案并进行实验】由实验结论为含有碳酸钠可知,现象为产生白色沉淀。步骤①中滴加过量CaCl₂溶液,目的是检验Na₂CO₃并使碳酸钠完全反应。滴入过量的CaCl₂溶液后,测得溶液的pH=10,则说明原固体中含有NaOH。【拓展】碳酸钠能和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,可用适量氢氧化钙溶液除去氢氧化钠中含有的碳酸钠。
8. 「2025杭州采荷中学期中」实验室有一瓶敞口放置一段时间的氢氧化钠固体(不考虑水分),为测定这瓶样品中氢氧化钠的质量分数,做如下实验:现取m克样品放入盛有足量水的烧杯中(充分溶解),向烧杯中逐滴加入300克一定溶质质量分数的稀盐酸。实验数据如图所示。试分析并计算回答:
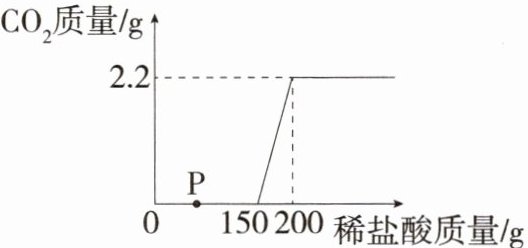
(1)氢氧化钠变质的化学方程式为
(2)P点对应的溶液中溶质是
(3)m克样品中氢氧化钠的质量分数是多少?(精确到0.1%)

(1)氢氧化钠变质的化学方程式为
2NaOH+CO₂=Na₂CO₃+H₂O
;由图得,加入的稀盐酸与样品充分反应时,产生气体的质量是2.2
克。(2)P点对应的溶液中溶质是
NaOH、Na₂CO₃、NaCl
。(3)m克样品中氢氧化钠的质量分数是多少?(精确到0.1%)
答案:
答案 (1)2NaOH+CO₂=Na₂CO₃+H₂O 2.2 (2)NaOH、Na₂CO₃、NaCl
(3)解:与碳酸钠反应的稀盐酸质量为200g - 150g = 50g。
设m g样品中碳酸钠的质量为x,稀盐酸的溶质质量分数为y。
Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
106 73 44
x 50g×y 2.2g
$\frac{106}{44}=\frac{x}{2.2g}$ x = 5.3g
$\frac{73}{44}=\frac{50g×y}{2.2g}$ y = 7.3%
设m g样品中氢氧化钠的质量为z。
NaOH+HCl=NaCl+H₂O
40 36.5
z 150g×7.3%
$\frac{40}{36.5}=\frac{z}{150g×7.3%}$ z = 12g
所以m克样品中氢氧化钠的质量分数为
$\frac{12g}{12g + 5.3g}×100\%≈69.4\%$。
答:m克样品中氢氧化钠的质量分数约是69.4%。
解析 (1)氢氧化钠在空气中变质,是因为氢氧化钠和二氧化碳反应生成碳酸钠和水,反应的化学方程式为2NaOH+CO₂=Na₂CO₃+H₂O。由题图可知,加入的稀盐酸与样品充分反应时,产生气体的质量是2.2g。(2)氢氧化钠和碳酸钠的混合溶液中加入稀盐酸,盐酸优先与氢氧化钠反应,此时没有气体生成;一直到加入150g稀盐酸时才开始有气体生成,说明此时氢氧化钠刚好完全反应,碳酸钠与稀盐酸开始反应,所以P点对应的溶液中溶质是剩余的NaOH、尚未参加反应的Na₂CO₃以及生成的NaCl。
(3)解:与碳酸钠反应的稀盐酸质量为200g - 150g = 50g。
设m g样品中碳酸钠的质量为x,稀盐酸的溶质质量分数为y。
Na₂CO₃+2HCl=2NaCl+H₂O+CO₂↑
106 73 44
x 50g×y 2.2g
$\frac{106}{44}=\frac{x}{2.2g}$ x = 5.3g
$\frac{73}{44}=\frac{50g×y}{2.2g}$ y = 7.3%
设m g样品中氢氧化钠的质量为z。
NaOH+HCl=NaCl+H₂O
40 36.5
z 150g×7.3%
$\frac{40}{36.5}=\frac{z}{150g×7.3%}$ z = 12g
所以m克样品中氢氧化钠的质量分数为
$\frac{12g}{12g + 5.3g}×100\%≈69.4\%$。
答:m克样品中氢氧化钠的质量分数约是69.4%。
解析 (1)氢氧化钠在空气中变质,是因为氢氧化钠和二氧化碳反应生成碳酸钠和水,反应的化学方程式为2NaOH+CO₂=Na₂CO₃+H₂O。由题图可知,加入的稀盐酸与样品充分反应时,产生气体的质量是2.2g。(2)氢氧化钠和碳酸钠的混合溶液中加入稀盐酸,盐酸优先与氢氧化钠反应,此时没有气体生成;一直到加入150g稀盐酸时才开始有气体生成,说明此时氢氧化钠刚好完全反应,碳酸钠与稀盐酸开始反应,所以P点对应的溶液中溶质是剩余的NaOH、尚未参加反应的Na₂CO₃以及生成的NaCl。
查看更多完整答案,请扫码查看


