第97页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
13. (10分)(2025·无锡期中)将二氧化碳转化为有机物是实现“碳中和”的途径之一,我国科学家研制出了全球首套捕集二氧化碳合成甲醇$(CH_3OH)$的装置,有利于实现“碳中和”。以下是将二氧化碳在一定条件下转化成$CH_3OH$的工艺流程图。
查阅资料:甲醇常温下是一种无色液体,易溶于水,熔点:-97.8℃,沸点:64.7℃。
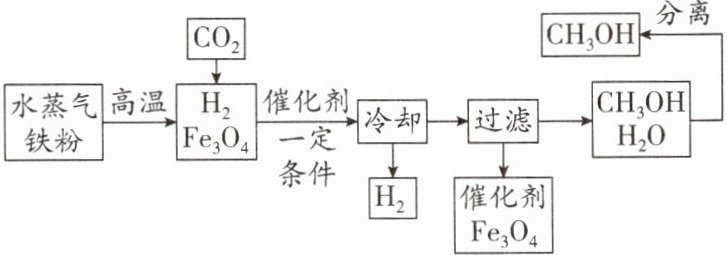
(1)二氧化碳和甲醇中都含碳____(填“单质”或“元素”)。
(2)自然界中消耗二氧化碳的主要途径是______。
(3)小明在实验室进行过滤操作时,发现所得滤液仍然浑浊了,经检查滤纸和其他仪器均正常,失败的原因可能是______。
(4)请写出铁和水蒸气发生反应的化学方程式:______。
(5)根据资料,请你设计分离出$CH_3OH$的一种方案:______。
查阅资料:甲醇常温下是一种无色液体,易溶于水,熔点:-97.8℃,沸点:64.7℃。

(1)二氧化碳和甲醇中都含碳____(填“单质”或“元素”)。
(2)自然界中消耗二氧化碳的主要途径是______。
(3)小明在实验室进行过滤操作时,发现所得滤液仍然浑浊了,经检查滤纸和其他仪器均正常,失败的原因可能是______。
(4)请写出铁和水蒸气发生反应的化学方程式:______。
(5)根据资料,请你设计分离出$CH_3OH$的一种方案:______。
答案:
(1)元素
(2)光合作用
(3)液面高于滤纸边缘或盛接滤液的烧杯不干净等
(4)$3Fe+4H_{2}O\xlongequal {高温}Fe_{3}O_{4}+4H_{2}$
(5)蒸馏,将混合物加热到64.7℃(合理即可)
解析:
(4)由流程图可知,水蒸气与铁高温条件下生成氢气和四氧化三铁。
(5)根据资料:甲醇常温下是一种无色液体,易溶于水,熔点:-97.8℃,沸点:64.7℃。水的沸点是100℃,可利用水和甲醇的沸点不同进行分离。
(1)元素
(2)光合作用
(3)液面高于滤纸边缘或盛接滤液的烧杯不干净等
(4)$3Fe+4H_{2}O\xlongequal {高温}Fe_{3}O_{4}+4H_{2}$
(5)蒸馏,将混合物加热到64.7℃(合理即可)
解析:
(4)由流程图可知,水蒸气与铁高温条件下生成氢气和四氧化三铁。
(5)根据资料:甲醇常温下是一种无色液体,易溶于水,熔点:-97.8℃,沸点:64.7℃。水的沸点是100℃,可利用水和甲醇的沸点不同进行分离。
14. (10分)(2024·邯郸二模)A~H是初中化学常见的物质,其中A、B、C、E均为气体,且E有毒。它们之间的转化关系如图所示(反应条件已略去),请回答下列问题。
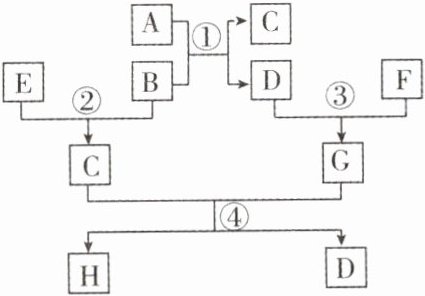
(1)E的化学式为____。
(2)反应④的化学方程式为______。
(3)B的一种用途为______。

(1)E的化学式为____。
(2)反应④的化学方程式为______。
(3)B的一种用途为______。
答案:
(1)CO
(2)$CO_{2}+Ca(OH)_{2}=CaCO_{3}\downarrow +H_{2}O$
(3)供给呼吸(合理即可)
解析:E有毒,则E是一氧化碳;A和B反应得到C和D,且A、B、C、E均为气体,则A是甲烷,B是氧气,C是二氧化碳,D是水;C和G反应得到H和D,D和F反应得到G,则F是氧化钙,G是氢氧化钙,H是碳酸钙。据此分析解答。
(1)CO
(2)$CO_{2}+Ca(OH)_{2}=CaCO_{3}\downarrow +H_{2}O$
(3)供给呼吸(合理即可)
解析:E有毒,则E是一氧化碳;A和B反应得到C和D,且A、B、C、E均为气体,则A是甲烷,B是氧气,C是二氧化碳,D是水;C和G反应得到H和D,D和F反应得到G,则F是氧化钙,G是氢氧化钙,H是碳酸钙。据此分析解答。
15. (18分)实验室现有高锰酸钾、块状石灰石、稀硫酸、稀盐酸、浓盐酸、棉花以及下列仪器及装置。

请回答下列问题:
(1)仪器①的名称是____。
(2)利用上述仪器和试剂制取氧气,反应的化学方程式为______,利用装置A制氧气还需改进的地方是______。在上述收集气体的装置中,不能用于收集氧气的是____(填字母)。
(3)实验室常用装置B和____(填试剂名称)制取$CO_2,$其反应的化学方程式为______。若使用装置F作为制取$CO_2$的发生装置。与装置B比较,除了利用废物的优点外,请写出另外一个优点:______。
(4)选用C装置收集二氧化碳的原因是:在相同条件下,二氧化碳的密度比空气的密度____(填“大”或“小”)。
(5)若用装置G来干燥制取的二氧化碳,则气体应从____(填“a”或“b”)管口进入。

请回答下列问题:
(1)仪器①的名称是____。
(2)利用上述仪器和试剂制取氧气,反应的化学方程式为______,利用装置A制氧气还需改进的地方是______。在上述收集气体的装置中,不能用于收集氧气的是____(填字母)。
(3)实验室常用装置B和____(填试剂名称)制取$CO_2,$其反应的化学方程式为______。若使用装置F作为制取$CO_2$的发生装置。与装置B比较,除了利用废物的优点外,请写出另外一个优点:______。
(4)选用C装置收集二氧化碳的原因是:在相同条件下,二氧化碳的密度比空气的密度____(填“大”或“小”)。
(5)若用装置G来干燥制取的二氧化碳,则气体应从____(填“a”或“b”)管口进入。
答案:
(1)长颈漏斗
(2)$2KMnO_{4}\xlongequal {△}K_{2}MnO_{4}+MnO_{2}+O_{2}\uparrow$在试管口塞一团棉花 D
(3)块状石灰、稀盐酸$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow$可以控制反应的发生和停止
(4)大
(5)b
(1)长颈漏斗
(2)$2KMnO_{4}\xlongequal {△}K_{2}MnO_{4}+MnO_{2}+O_{2}\uparrow$在试管口塞一团棉花 D
(3)块状石灰、稀盐酸$CaCO_{3}+2HCl=CaCl_{2}+H_{2}O+CO_{2}\uparrow$可以控制反应的发生和停止
(4)大
(5)b
16. (16分)新趋势 项目式探究 (2024·淮安期中)用实验的方法研究$CO_2$的制取和性质是初中化学重要的学习内容。
【活动一】探究$CO_2$的实验室制法
(1)在实验室不利用碳的燃烧来制取$CO_2,$其主要原因是______(答出1条)。
(2)二氧化碳密度大于空气且不与空气反应,通常采用______收集。
【活动二】探究$CO_2$在水中的溶解
(3)探究溶解速率:该小组用排水法收集$CO_2($如图1),待收集到$100mL CO_2$后,移出导管。每隔一段时间观察并记录量筒内$CO_2$体积。重复实验,所测数据平均值如下表。

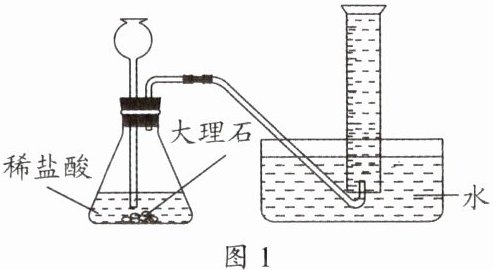
分析上表数据,得出也能用排水法收集$CO_2,$写出你的判断依据______。
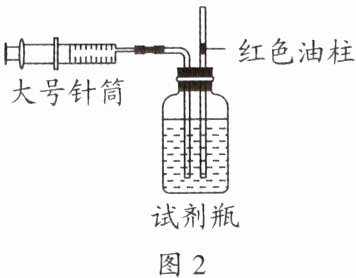
(4)探究溶解能力:如图2,用大号针筒抽取200mL二氧化碳气体,试剂瓶中加入200mL水(恰好加满),塞紧双孔橡皮塞,连接大号针筒和试剂瓶,缓慢推动活塞,将二氧化碳注入水中。当向水中注入$CO_2$气体体积达到120mL时,红色油柱开始向上移动,实验表明在该条件下,1体积水中能溶解____体积二氧化碳。
【活动三】探究$CO_2$的重要性质
(5)将二氧化碳气体缓慢通入如图3所示装置,并观察实验现象。

①实验中观察到______,能得出$“CO_2$与水发生反应”的结论。
②通入二氧化碳一段时间后,三个烧杯中蜡烛均熄灭,能证明$“CO_2$密度大于空气”的是烧杯____(填“A”“B”或“C”)。
【活动一】探究$CO_2$的实验室制法
(1)在实验室不利用碳的燃烧来制取$CO_2,$其主要原因是______(答出1条)。
(2)二氧化碳密度大于空气且不与空气反应,通常采用______收集。
【活动二】探究$CO_2$在水中的溶解
(3)探究溶解速率:该小组用排水法收集$CO_2($如图1),待收集到$100mL CO_2$后,移出导管。每隔一段时间观察并记录量筒内$CO_2$体积。重复实验,所测数据平均值如下表。


分析上表数据,得出也能用排水法收集$CO_2,$写出你的判断依据______。
(4)探究溶解能力:如图2,用大号针筒抽取200mL二氧化碳气体,试剂瓶中加入200mL水(恰好加满),塞紧双孔橡皮塞,连接大号针筒和试剂瓶,缓慢推动活塞,将二氧化碳注入水中。当向水中注入$CO_2$气体体积达到120mL时,红色油柱开始向上移动,实验表明在该条件下,1体积水中能溶解____体积二氧化碳。

【活动三】探究$CO_2$的重要性质
(5)将二氧化碳气体缓慢通入如图3所示装置,并观察实验现象。

①实验中观察到______,能得出$“CO_2$与水发生反应”的结论。
②通入二氧化碳一段时间后,三个烧杯中蜡烛均熄灭,能证明$“CO_2$密度大于空气”的是烧杯____(填“A”“B”或“C”)。
答案:
(1)用碳的燃烧来制取CO₂时,反应物中有氧气参加,氧气的量不易控制,氧气过量,收集的气体是二氧化碳和氧气的混合物,氧气不足,收集的气体是一氧化碳和二氧化碳的混合物(合理即可)
(2)向上排空气法
(3)二氧化碳溶于水的速率远小于二氧化碳逸出的速率
(4)0.6
(5)①干燥的紫色石蕊试纸不变红,湿润的紫色石蕊试纸变红 ②A
解析:
(2)二氧化碳密度大于空气且不与空气反应,通常采用向上排空气法收集。
(3)由表中数据可知,二氧化碳溶于水的速率较慢。12h才溶解了23mL,所以可用排水法收集二氧化碳的理由是二氧化碳溶于水的速率远小于二氧化碳逸出的速率。
(4)当向水中注入CO₂气体体积达到120mL时,红色油柱开始向上移动,说明200mL水中最多能溶解120mL二氧化碳,实验表明在该条件下,1体积水中能溶解二氧化碳的体积是$\frac {120mL}{200mL}=0.6$。
(5)①紫色石蕊遇酸性物质变红,二氧化碳通入装置中时,干燥的紫色石蕊试纸不变红;二氧化碳与湿润的紫色石蕊试纸中的水反应生成碳酸,碳酸使湿润的紫色石蕊试纸变红;因此证明CO₂与水发生了反应的实验现象为干燥的紫色石蕊试纸不变红,湿润的紫色石蕊试纸变红。②A中导管口在烧杯口处,B、C中导管口接近烧杯底部,而A烧杯中蜡烛由下至上依次熄灭,说明二氧化碳沿着烧杯壁进入烧杯的底部,由此证明二氧化碳的密度比空气的大。
(1)用碳的燃烧来制取CO₂时,反应物中有氧气参加,氧气的量不易控制,氧气过量,收集的气体是二氧化碳和氧气的混合物,氧气不足,收集的气体是一氧化碳和二氧化碳的混合物(合理即可)
(2)向上排空气法
(3)二氧化碳溶于水的速率远小于二氧化碳逸出的速率
(4)0.6
(5)①干燥的紫色石蕊试纸不变红,湿润的紫色石蕊试纸变红 ②A
解析:
(2)二氧化碳密度大于空气且不与空气反应,通常采用向上排空气法收集。
(3)由表中数据可知,二氧化碳溶于水的速率较慢。12h才溶解了23mL,所以可用排水法收集二氧化碳的理由是二氧化碳溶于水的速率远小于二氧化碳逸出的速率。
(4)当向水中注入CO₂气体体积达到120mL时,红色油柱开始向上移动,说明200mL水中最多能溶解120mL二氧化碳,实验表明在该条件下,1体积水中能溶解二氧化碳的体积是$\frac {120mL}{200mL}=0.6$。
(5)①紫色石蕊遇酸性物质变红,二氧化碳通入装置中时,干燥的紫色石蕊试纸不变红;二氧化碳与湿润的紫色石蕊试纸中的水反应生成碳酸,碳酸使湿润的紫色石蕊试纸变红;因此证明CO₂与水发生了反应的实验现象为干燥的紫色石蕊试纸不变红,湿润的紫色石蕊试纸变红。②A中导管口在烧杯口处,B、C中导管口接近烧杯底部,而A烧杯中蜡烛由下至上依次熄灭,说明二氧化碳沿着烧杯壁进入烧杯的底部,由此证明二氧化碳的密度比空气的大。
查看更多完整答案,请扫码查看


