第54页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
9. (2025·荆州期中)同学们对含有$Na_{2}SO_{4}$、$Na_{2}SO_{3}$、$Na_{2}S$的混合物中各元素含量进行探究,经测定其中氧元素的质量分数为22%,则含钠元素的质量分数为 ()
A. 46%
B. 64%
C. 23%
D. 32%
A. 46%
B. 64%
C. 23%
D. 32%
答案:
A 解析:$Na_{2}SO_{4}$、$Na_{2}SO_{3}$、$Na_{2}S$的混合物中含硫、钠和氧三种元素,$Na$、$S$个数比$=2:1$,$Na$、$S$元素质量比$=(23×2):(32×1)=23:16$,经测定其中氧元素的质量分数为22%,钠元素、硫元素的质量分数$=1-22\%=78\%$,含钠元素的质量分数$=78\%×(\frac{23}{23+16}×100\%)=46\%$。
10. (2024·扬州期中)元素钴(Co)有多种化合价,将9.3 g $Co(OH)_{2}$在隔绝空气的条件下加热至刚好完全脱水,得到7.5 g钴的氧化物,该氧化物的化学式为 ()
A. $Co_{2}O_{3}$
B. $CoO_{3}$
C. CoO
D. $Co_{3}O_{4}$
A. $Co_{2}O_{3}$
B. $CoO_{3}$
C. CoO
D. $Co_{3}O_{4}$
答案:
C 解析:9.3g$Co(OH)_{2}$中$Co$元素的质量为$9.3g×\frac{59}{59+(16+1)×2}×100\%=5.9g$,则7.5g$Co$的氧化物中$Co$元素的质量也为5.9g,氧元素的质量为$7.5g-5.9g=1.6g$,设该氧化物的化学式为$Co_{x}O_{y}$,则有$\frac{5.9g}{59x}=\frac{1.6g}{16y}$,解得$x:y=1:1$,则其化学式为$CoO$。
11. 含有杂质的$NH_{4}NO_{3}$化肥样品,经测定其含氮量为38%,则其中含有的杂质可能为 ()
A. $NH_{4}HCO_{3}$
B. $(NH_{4})_{2}SO_{4}$
C. $NH_{4}Cl$
D. $CO(NH_{2})_{2}$
A. $NH_{4}HCO_{3}$
B. $(NH_{4})_{2}SO_{4}$
C. $NH_{4}Cl$
D. $CO(NH_{2})_{2}$
答案:
D 解析:$NH_{4}NO_{3}$的含氮量为$\frac{14×2}{14×2+1×4+16×3}×100\%=35\%$;含有杂质的硝酸铵的含氮量为38%,说明杂质的含氮量高于38%。碳酸氢铵的含氮量为$\frac{14}{14+1×5+12+16×3}×100\%≈18\%$;硫酸铵的含氮量为$\frac{14×2}{14×2+1×8+32+16×4}×100\%≈21\%$;氯化铵的含氮量为$\frac{14}{14+1×4+35.5}×100\%≈26\%$;尿素的含氮量为$\frac{14×2}{12+16+(14+1×2)×2}×100\%≈47\%$;故选D。
12. (2024·南京期中)由铁的氧化物组成的某固体样品共29 g,经测定其中含铁元素21 g。已知铁的氧化物有FeO、$Fe_{2}O_{3}和Fe_{3}O_{4}$三种,则下列说法正确的是 ()
A. 固体样品一定是$Fe_{3}O_{4}$
B. 固体样品不可能是$Fe_{2}O_{3}和Fe_{3}O_{4}$的混合物
C. 固体样品的组成只有2种情况
D. 若固体样品由两种氧化物组成,则两种氧化物的质量比为1:1
A. 固体样品一定是$Fe_{3}O_{4}$
B. 固体样品不可能是$Fe_{2}O_{3}和Fe_{3}O_{4}$的混合物
C. 固体样品的组成只有2种情况
D. 若固体样品由两种氧化物组成,则两种氧化物的质量比为1:1
答案:
B 解析:由铁的氧化物组成的某固体样品共29g,经测定其中含铁元素21g,则氧元素的质量为$29g-21g=8g$,则该固体中铁、氧元素的质量比为$21g:8g=21:8$,$FeO$中$Fe$、$O$元素的质量比为$56:16=7:2=21:6$,氧化铁中铁、氧元素的质量比为$(56×2):(16×3)=7:3=21:9$,四氧化三铁中铁、氧元素的质量比为$(56×3):(16×4)=21:8$,故该固体样品可能是四氧化三铁,也可能是$FeO$和氧化铁的混合物,也可能是氧化亚铁、氧化铁、四氧化三铁的混合物。由分析可知,A、C错误,B正确;若固体样品由两种氧化物组成,则这两种氧化物为$FeO$和$Fe_{2}O_{3}$,设氧化铁的质量为$x$,则氧化亚铁的质量为$29g-x$,则$x×\frac{56×2}{56×2+16×3}×100\%+(29g-x)×\frac{56}{56+16}×100\%=21g$,解得$x=20g$,则氧化亚铁的质量为$29g-20g=9g$,则氧化铁和氧化亚铁的质量比为$20g:9g=20:9$,D错误。
13. $\alpha$-丙氨酸是组成人体蛋白质的氨基酸之一,其分子结构如图所示(注:“●”表示氮原子,“○”表示碳原子,“●”表示氧原子,“○”表示氢原子,“—”表示原子之间的相互连接)。计算:
(1) 写出$\alpha$-丙氨酸的化学式:____。
(2) $\alpha$-丙氨酸中各原子个数比为C:H:O:N= ____(填最简整数比)。
(3) $\alpha$-丙氨酸中氮元素的质量分数为____(精确到0.1%)。

(1) 写出$\alpha$-丙氨酸的化学式:____。
(2) $\alpha$-丙氨酸中各原子个数比为C:H:O:N= ____(填最简整数比)。
(3) $\alpha$-丙氨酸中氮元素的质量分数为____(精确到0.1%)。

答案:
(1)$C_{3}H_{7}O_{2}N$
(2)$3:7:2:1$
(3)15.7%
解析:
(1)由图可知,每个$\alpha$-丙氨酸分子由3个碳原子、7个氢原子、1个氮原子、2个氧原子构成,化学式为$C_{3}H_{7}O_{2}N$。
(2)元素符号右下角的数字表示原子的个数,$\alpha$-丙氨酸中各原子个数比为$C:H:O:N=3:7:2:1$。
(3)$\alpha$-丙氨酸中氮元素的质量分数为$\frac{14}{12×3+1×7+16×2+14}×100\%≈15.7\%$。
(1)$C_{3}H_{7}O_{2}N$
(2)$3:7:2:1$
(3)15.7%
解析:
(1)由图可知,每个$\alpha$-丙氨酸分子由3个碳原子、7个氢原子、1个氮原子、2个氧原子构成,化学式为$C_{3}H_{7}O_{2}N$。
(2)元素符号右下角的数字表示原子的个数,$\alpha$-丙氨酸中各原子个数比为$C:H:O:N=3:7:2:1$。
(3)$\alpha$-丙氨酸中氮元素的质量分数为$\frac{14}{12×3+1×7+16×2+14}×100\%≈15.7\%$。
14. (2025·贵阳期中)如图是超市销售的某种碘盐部分标签。
(1) 该碘盐属于____(填“纯净物”或“混合物”)。
(2) $KIO_{3}$中K、I、O三种元素的质量比为____。中国营养学会推荐:一个普通成人每天摄入“碘”的质量为0.15 mg,假设碘的来源仅靠该碘盐,则一个普通成人每天需摄入这种碘盐____g。
(3) 这一袋碘盐中$KIO_{3}$的质量为____mg(结果保留到0.1 mg)。

(1) 该碘盐属于____(填“纯净物”或“混合物”)。
(2) $KIO_{3}$中K、I、O三种元素的质量比为____。中国营养学会推荐:一个普通成人每天摄入“碘”的质量为0.15 mg,假设碘的来源仅靠该碘盐,则一个普通成人每天需摄入这种碘盐____g。
(3) 这一袋碘盐中$KIO_{3}$的质量为____mg(结果保留到0.1 mg)。

答案:
(1)混合物
(2)$39:127:48$ 7.5
(3)16.9
解析:
(1)该碘盐中含有氯化钠、碘酸钾等物质,属于混合物。
(2)$KIO_{3}$中$K$、$I$、$O$三种元素的质量比为$39:127:(16×3)=39:127:48$;摄入“碘”的质量为0.15mg,由图可知,每100g食盐中含碘的质量为2mg,则一个普通成人每天需摄入这种碘盐的质量为$0.15mg÷\frac{2mg}{100g}=7.5g$。
(3)该食盐中含有碘的质量为$500g×2mg/100g=10mg$,则含有碘酸钾的质量为$10mg÷(\frac{127}{39+127+16×3}×100\%)≈16.9mg$。
(1)混合物
(2)$39:127:48$ 7.5
(3)16.9
解析:
(1)该碘盐中含有氯化钠、碘酸钾等物质,属于混合物。
(2)$KIO_{3}$中$K$、$I$、$O$三种元素的质量比为$39:127:(16×3)=39:127:48$;摄入“碘”的质量为0.15mg,由图可知,每100g食盐中含碘的质量为2mg,则一个普通成人每天需摄入这种碘盐的质量为$0.15mg÷\frac{2mg}{100g}=7.5g$。
(3)该食盐中含有碘的质量为$500g×2mg/100g=10mg$,则含有碘酸钾的质量为$10mg÷(\frac{127}{39+127+16×3}×100\%)≈16.9mg$。
15. 某地化肥市场价格如下:
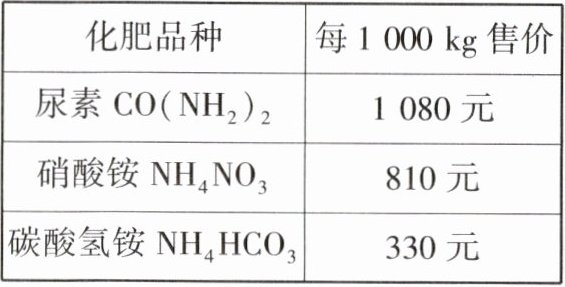
(1) 尿素的相对分子质量为____。
(2) 碳酸氢铵中碳、氢两种元素的质量比为____。
(3) 上述三种化肥中氮元素质量分数最大的是____(填化肥名称),求该化肥中氮元素的质量分数是____(计算结果精确到0.1%)。
(4) 分别用10000元采购上述化肥,则购得化肥中含氮元素最多的是哪种化肥____(填化学式),求购得这种化肥含氮元素的质量为____kg(计算结果保留一位小数)。

(1) 尿素的相对分子质量为____。
(2) 碳酸氢铵中碳、氢两种元素的质量比为____。
(3) 上述三种化肥中氮元素质量分数最大的是____(填化肥名称),求该化肥中氮元素的质量分数是____(计算结果精确到0.1%)。
(4) 分别用10000元采购上述化肥,则购得化肥中含氮元素最多的是哪种化肥____(填化学式),求购得这种化肥含氮元素的质量为____kg(计算结果保留一位小数)。
答案:
(1)60
(2)$12:5$
(3)尿素 46.7%
(4)$NH_{4}HCO_{3}$ 5370.2
解析:
(1)$CO(NH_{2})_{2}$的相对分子质量$=12+16+(14+1×2)×2=60$。
(2)碳酸氢铵$(NH_{4}HCO_{3})$中碳、氢两种元素的质量比为$12:(1×5)=12:5$。
(3)尿素中氮元素的质量分数为$\frac{14×2}{60}×100\%≈46.7\%$;硝酸铵$(NH_{4}NO_{3})$中氮元素的质量分数为$\frac{14×2}{14×2+1×4+16×3}×100\%=35\%$;碳酸氢铵$(NH_{4}HCO_{3})$中氮元素的质量分数为$\frac{14}{14+1×5+12+16×3}×100\%≈17.7\%$;根据以上计算可知,化肥中氮元素质量分数最大的是尿素。
(4)10000元购买的尿素中氮元素的质量为$10000元÷\frac{1080元}{1000kg}×\frac{14×2}{60}≈4321.0kg$;10000元购买的硝酸铵中氮元素的质量为$10000元÷\frac{810元}{1000kg}×\frac{14×2}{80}≈4321.0kg$;10000元购买的碳酸氢铵中氮元素的质量为$10000元÷\frac{330元}{1000kg}×\frac{14}{79}≈5370.2kg$;故购得含氮元素最多的是$NH_{4}HCO_{3}$,购得这种化肥含氮元素的质量为5370.2kg。
(1)60
(2)$12:5$
(3)尿素 46.7%
(4)$NH_{4}HCO_{3}$ 5370.2
解析:
(1)$CO(NH_{2})_{2}$的相对分子质量$=12+16+(14+1×2)×2=60$。
(2)碳酸氢铵$(NH_{4}HCO_{3})$中碳、氢两种元素的质量比为$12:(1×5)=12:5$。
(3)尿素中氮元素的质量分数为$\frac{14×2}{60}×100\%≈46.7\%$;硝酸铵$(NH_{4}NO_{3})$中氮元素的质量分数为$\frac{14×2}{14×2+1×4+16×3}×100\%=35\%$;碳酸氢铵$(NH_{4}HCO_{3})$中氮元素的质量分数为$\frac{14}{14+1×5+12+16×3}×100\%≈17.7\%$;根据以上计算可知,化肥中氮元素质量分数最大的是尿素。
(4)10000元购买的尿素中氮元素的质量为$10000元÷\frac{1080元}{1000kg}×\frac{14×2}{60}≈4321.0kg$;10000元购买的硝酸铵中氮元素的质量为$10000元÷\frac{810元}{1000kg}×\frac{14×2}{80}≈4321.0kg$;10000元购买的碳酸氢铵中氮元素的质量为$10000元÷\frac{330元}{1000kg}×\frac{14}{79}≈5370.2kg$;故购得含氮元素最多的是$NH_{4}HCO_{3}$,购得这种化肥含氮元素的质量为5370.2kg。
查看更多完整答案,请扫码查看


