第78页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
例1 (2023·贵州中考)探索燃烧的利用和控制,能更好地为人类服务。下列关于燃烧的说法错误的是 ()
A. 燃烧属于化学变化,产生的能量被广泛应用
B. 把煤块粉碎成煤粉使用,可以使煤充分燃烧
C. 炒菜油锅着火时,立刻盖上锅盖可以灭火
D. 把蜡烛伸入装有氧气的集气瓶中,蜡烛能立刻燃烧
A. 燃烧属于化学变化,产生的能量被广泛应用
B. 把煤块粉碎成煤粉使用,可以使煤充分燃烧
C. 炒菜油锅着火时,立刻盖上锅盖可以灭火
D. 把蜡烛伸入装有氧气的集气瓶中,蜡烛能立刻燃烧
答案:
D
1. (2024·连云港模拟)白磷的着火点是40℃,红磷的着火点是240℃。某同学用足量的白磷和红磷探究燃烧的条件,实验装置如图1所示。实验中测得试管②中氧气的体积分数随时间的变化曲线如图2所示。下列说法正确的是 (
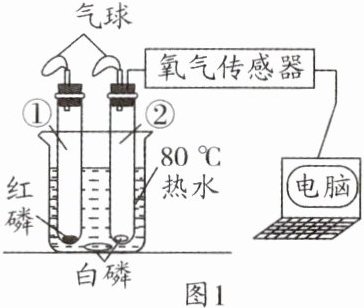
)
A. 烧杯底部的白磷可以燃烧
B. 实验过程中试管①的气球先变小后变大
C. 通过试管中白磷燃烧、红磷不燃烧的现象得出结论:燃烧需要氧气
D. 物质燃烧时氧气必须达到一定的体积分数

)
A. 烧杯底部的白磷可以燃烧
B. 实验过程中试管①的气球先变小后变大
C. 通过试管中白磷燃烧、红磷不燃烧的现象得出结论:燃烧需要氧气
D. 物质燃烧时氧气必须达到一定的体积分数
答案:
D
例2 (2024·广东中考)我国科学家利用光催化技术实现了绿色制取$H_2O_2,$反应的微观示意图如图所示。下列说法正确的是 ()
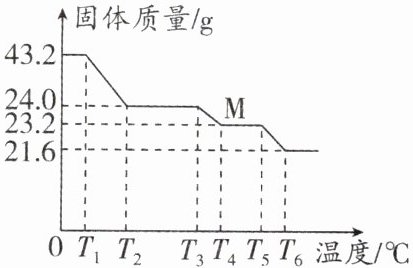
A. 反应后氧原子个数减少
B. 反应后催化剂的质量增加
C. b的化学式为$H_2O$
D. 参加反应的a、b分子个数比为1:1


A. 反应后氧原子个数减少
B. 反应后催化剂的质量增加
C. b的化学式为$H_2O$
D. 参加反应的a、b分子个数比为1:1
答案:
C 解析:根据质量守恒定律,反应前后原子种类和数目不变,A错误;反应后催化剂的质量不变,B错误;由题图可知,一个b分子是由1个氧原子和2个氢原子构成的,则b的化学式为H₂O,C正确;由题图可知,氧气和水在催化剂的作用下反应生成过氧化氢,化学方程式为$O₂ + 2H₂O\xlongequal{催化剂}2H₂O₂,$则参加反应的a、b分子个数比为1:2,D错误。
2. (2024·宜宾中考)一定条件下,X、Y、Z、W四种物质在密闭容器中充分反应,测得反应前后各物质质量如下表。
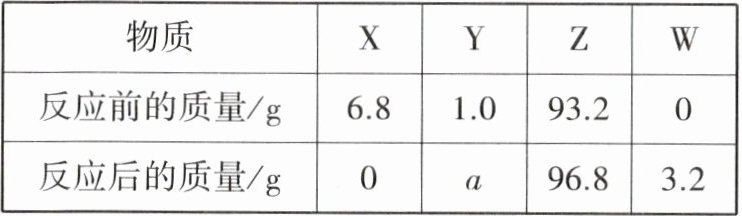
下列说法正确的是 ()
A. a= 1.0,Y一定是该反应的催化剂
B. 该反应一定为化合反应
C. X与W相对分子质量之比一定为17:8
D. Z与W质量变化量之比一定为9:8

下列说法正确的是 ()
A. a= 1.0,Y一定是该反应的催化剂
B. 该反应一定为化合反应
C. X与W相对分子质量之比一定为17:8
D. Z与W质量变化量之比一定为9:8
答案:
D 解析:一定条件下,X、Y、Z、W四种物质在密闭容器中充分反应,根据质量守恒定律,则有6.8g + 1.0g + 93.2g + 0g = 0g + a g + 96.8g + 3.2g,a = 1.0;反应后X的质量减少了6.8g - 0g = 6.8g,则X为反应物;反应后Z的质量增加了96.8g - 93.2g = 3.6g,则Z为生成物;反应后W的质量增加了3.2g - 0g = 3.2g,则W为生成物;反应前后Y的质量不变,则Y可能是该反应的催化剂,也可能是没有参与反应的杂质;故该反应为X在一定条件下生成Z和W,属于分解反应。由分析可知,A、B错误;由分析可知,X与W的质量变化量之比为(6.8g - 0g):(3.2g - 0g) = 6.8g:3.2g = 17:8,但因为反应式中X与W的化学计量数之比未知,故无法判断其相对分子质量之比,C错误;由分析可知,Z与W质量变化量之比一定为(96.8g - 93.2g):(3.2g - 0g) = 3.6g:3.2g = 9:8,D正确。
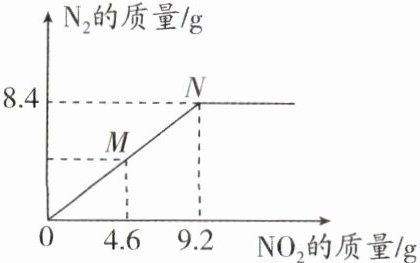
例3 肼又称联氨,无色油状液体,是一种常见的燃料,它与二氧化氮反应的化学方程式为aNₓHᵧ + bNO_2 $\xlongequal{点燃}$ cN_2 + dH_2O。不同质量的二氧化氮与一定质量的肼反应,生成N_2的质量随参加反应的NO_2的质量变化如图所示。下列说法不正确的是 ()
A. 化学计量数2b= d
B. NₓHᵧ中x:y= 1:2
C. N点时生成水的质量为3.6g
D. M点时消耗肼的质量为3.2g

A. 化学计量数2b= d
B. NₓHᵧ中x:y= 1:2
C. N点时生成水的质量为3.6g
D. M点时消耗肼的质量为3.2g
答案:
C 解析:反应前有2b个氧原子,反应后有d个氧原子,反应前后氧原子个数不变,故化学计量数2b = d,A正确;由反应前后氮原子个数不变有ax + b = 2c,则x = $\frac{2c - b}{a}$,由反应前后氢原子个数不变有y = $\frac{2d}{a}$,故x:y = (2c - b):2d;由图知9.2g二氧化氮反应时,生成8.4g氮气,则
aNₓHᵧ + bNO₂\xlongequal{点燃}cN₂ + dH₂O
46b 28c
9.2g 8.4g
$\frac{46b}{28c} = \frac{9.2g}{8.4g}$,$\frac{b}{c} = \frac{2}{3}$,c = $\frac{3b}{2}$
代入,则x:y = (2c - b):2d = 2b:2d,已知2b = d,则x:y = 2b:2d = d:2d = 1:2,B正确;N点时消耗二氧化氮的质量为9.2g,则生成水的质量 = 9.2g×$\frac{32}{46}$÷$\frac{16}{18}$ = 7.2g,C错误;反应的二氧化氮和生成水的质量比 = 46b:18d = 23:18;反应的二氧化氮和生成氮气的质量比为9.2g:8.4g = 23:21,所以当消耗4.6g二氧化氮时,生成水的质量 = 4.6g×$\frac{18}{23}$ = 3.6g,生成氮气的质量 = 4.6g×$\frac{21}{23}$ = 4.2g,则M点时消耗肼的质量 = 3.6g + 4.2g - 4.6g = 3.2g,D正确。
aNₓHᵧ + bNO₂\xlongequal{点燃}cN₂ + dH₂O
46b 28c
9.2g 8.4g
$\frac{46b}{28c} = \frac{9.2g}{8.4g}$,$\frac{b}{c} = \frac{2}{3}$,c = $\frac{3b}{2}$
代入,则x:y = (2c - b):2d = 2b:2d,已知2b = d,则x:y = 2b:2d = d:2d = 1:2,B正确;N点时消耗二氧化氮的质量为9.2g,则生成水的质量 = 9.2g×$\frac{32}{46}$÷$\frac{16}{18}$ = 7.2g,C错误;反应的二氧化氮和生成水的质量比 = 46b:18d = 23:18;反应的二氧化氮和生成氮气的质量比为9.2g:8.4g = 23:21,所以当消耗4.6g二氧化氮时,生成水的质量 = 4.6g×$\frac{18}{23}$ = 3.6g,生成氮气的质量 = 4.6g×$\frac{21}{23}$ = 4.2g,则M点时消耗肼的质量 = 3.6g + 4.2g - 4.6g = 3.2g,D正确。
查看更多完整答案,请扫码查看


