2025年资源与评价黑龙江教育出版社高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年资源与评价黑龙江教育出版社高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第9页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
1.硫酸根离子检验的实验探究
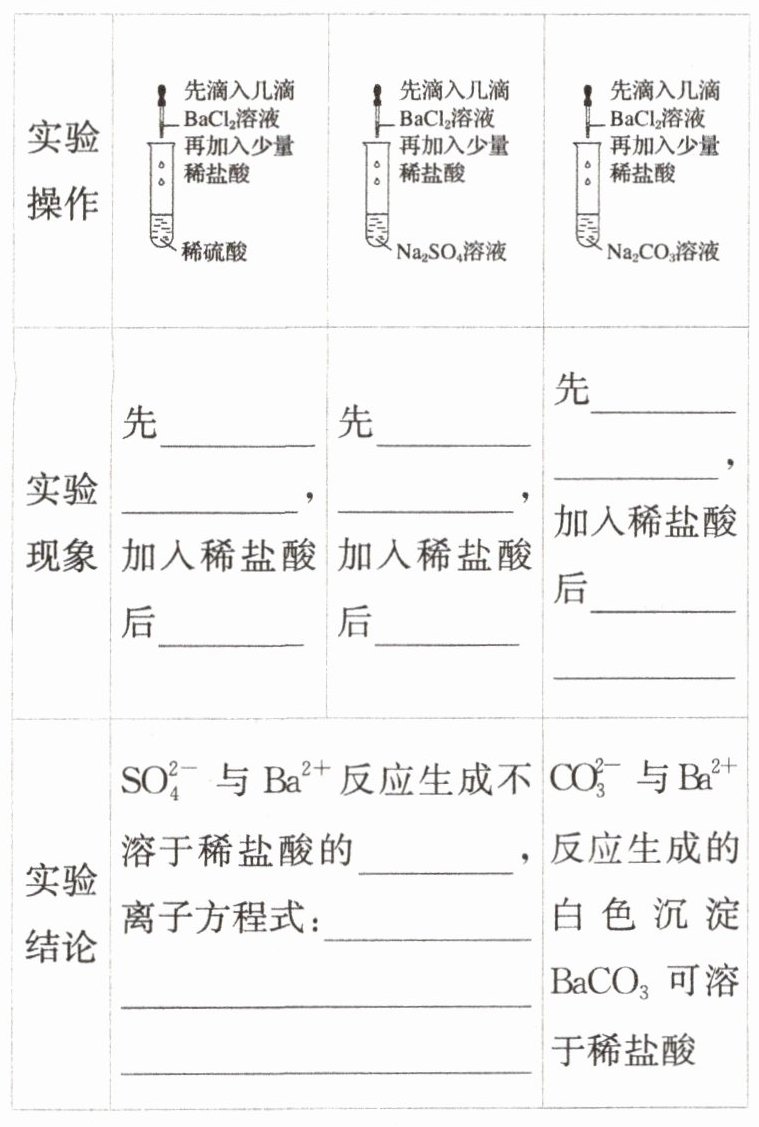

答案:
生成白色沉淀 沉淀不溶解 生成白色沉淀 沉淀不溶解 生成白色沉淀 沉淀溶解,且有气泡产生 白色沉淀 SO₄²⁻+Ba²⁺==BaSO₄↓
2.检验$SO_{4}^{2-}$的正确操作及解释
(1)
待测液$\xrightarrow{稀盐酸酸化}$无明显现象$\xrightarrow{BaCl_{2}溶液}$出现______沉淀,即可确定存在$SO_{4}^{2-}$。
(2)
理论解释
①先加稀盐酸的目的是排除______、______、______等离子的干扰。
②再加入$BaCl_{2}$溶液,若存在$SO_{4}^{2-}$,发生反应的离子方程式为______。
(1)
待测液$\xrightarrow{稀盐酸酸化}$无明显现象$\xrightarrow{BaCl_{2}溶液}$出现______沉淀,即可确定存在$SO_{4}^{2-}$。
(2)
理论解释
①先加稀盐酸的目的是排除______、______、______等离子的干扰。
②再加入$BaCl_{2}$溶液,若存在$SO_{4}^{2-}$,发生反应的离子方程式为______。
答案:
白色
@@①Ag⁺ CO₃²⁻ SO₃²⁻ ②Ba²⁺+SO₄²⁻==BaSO₄↓
@@①Ag⁺ CO₃²⁻ SO₃²⁻ ②Ba²⁺+SO₄²⁻==BaSO₄↓
3.$SO_{4}^{2-}$检验应用——粗盐除杂
(1)
若除去粗盐中杂质(硫酸盐、$CaCl_{2}$、$MgCl_{2}$),将选用的试剂及反应的离子方程式填入下表:
|杂质|加入的试剂|离子方程式|
|----|----|----|
|硫酸盐| | |
|$CaCl_{2}$| | |
|$MgCl_{2}$| | |
(2)
试剂加入的顺序
为使杂质离子完全除去,通常加入试剂及顺序有如下三种:
①$BaCl_{2}$溶液→______→______→盐酸
②$NaOH$溶液→______→______→盐酸;
③______→______→______→盐酸。
总结:为保障杂质离子完全除去,只要______在______之后加入即可。
(1)
若除去粗盐中杂质(硫酸盐、$CaCl_{2}$、$MgCl_{2}$),将选用的试剂及反应的离子方程式填入下表:
|杂质|加入的试剂|离子方程式|
|----|----|----|
|硫酸盐| | |
|$CaCl_{2}$| | |
|$MgCl_{2}$| | |
(2)
试剂加入的顺序
为使杂质离子完全除去,通常加入试剂及顺序有如下三种:
①$BaCl_{2}$溶液→______→______→盐酸
②$NaOH$溶液→______→______→盐酸;
③______→______→______→盐酸。
总结:为保障杂质离子完全除去,只要______在______之后加入即可。
答案:
氯化钡溶液 Ba²⁺+SO₄²⁻==BaSO₄↓ 碳酸钠溶液 Ca²⁺+CO₃²⁻==CaCO₃↓ 烧碱溶液 Mg²⁺+2OH⁻==Mg(OH)₂↓
@@①NaOH溶液 Na₂CO₃溶液 ②BaCl₂溶液 Na₂CO₃溶液 ③BaCl₂溶液 Na₂CO₃溶液 NaOH溶液 碳酸钠溶液 氯化钡溶液
@@①NaOH溶液 Na₂CO₃溶液 ②BaCl₂溶液 Na₂CO₃溶液 ③BaCl₂溶液 Na₂CO₃溶液 NaOH溶液 碳酸钠溶液 氯化钡溶液
「判断正误」
(1)取少量试样溶液,加入用稀盐酸酸化的$BaCl_{2}$溶液,有白色沉淀生成,则溶液中一定含有$SO_{4}^{2-}$( )
(2)取少量试样溶液,先加入$BaCl_{2}$溶液,有白色沉淀生成,再加稀$HNO_{3}$,沉淀不溶解,则溶液中一定含有$SO_{4}^{2-}$( )
(3)取少量试样溶液,先加入稀硫酸,无现象,再加入$BaCl_{2}$,有白色沉淀生成,则溶液中一定含有$SO_{4}^{2-}$( )
(4)为除去粗盐水中少量的$CO_{3}^{2-}$,可向溶液中加入过量的$K_{2}CO_{3}$溶液,然后过滤( )
(5)为除去粗盐中的$Mg^{2+}$、$Ca^{2+}$、$SO_{4}^{2-}$,可依次加入稍过量的$NaOH$、$BaCl_{2}$、$Na_{2}CO_{3}$溶液,过滤后加入稀盐酸调节溶液为中性( )
(1)取少量试样溶液,加入用稀盐酸酸化的$BaCl_{2}$溶液,有白色沉淀生成,则溶液中一定含有$SO_{4}^{2-}$( )
(2)取少量试样溶液,先加入$BaCl_{2}$溶液,有白色沉淀生成,再加稀$HNO_{3}$,沉淀不溶解,则溶液中一定含有$SO_{4}^{2-}$( )
(3)取少量试样溶液,先加入稀硫酸,无现象,再加入$BaCl_{2}$,有白色沉淀生成,则溶液中一定含有$SO_{4}^{2-}$( )
(4)为除去粗盐水中少量的$CO_{3}^{2-}$,可向溶液中加入过量的$K_{2}CO_{3}$溶液,然后过滤( )
(5)为除去粗盐中的$Mg^{2+}$、$Ca^{2+}$、$SO_{4}^{2-}$,可依次加入稍过量的$NaOH$、$BaCl_{2}$、$Na_{2}CO_{3}$溶液,过滤后加入稀盐酸调节溶液为中性( )
答案:
(1)×
(2)×
(3)×
(4)×
(5)√
(1)×
(2)×
(3)×
(4)×
(5)√
「深度思考」
1.为检验某种阳离子为$Na^{+}$的溶液中含有的阴离子是$SO_{4}^{2-}$、$CO_{3}^{2-}$还是$OH^{-}$、$Cl^{-}$,下列设计的方案合理的是______。
方案一:检验$CO_{3}^{2-}$:向待测液中加入足量的稀盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
方案二:检验$SO_{4}^{2-}$:先向待测液中加入稀盐酸至溶液呈酸性,未见沉淀或气体生成,再加入$BaCl_{2}$溶液出现白色沉淀
方案三:检验$OH^{-}$:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验$Cl^{-}$:向待测溶液中依次加入稀盐酸和$AgNO_{3}$溶液,有白色沉淀生成
1.为检验某种阳离子为$Na^{+}$的溶液中含有的阴离子是$SO_{4}^{2-}$、$CO_{3}^{2-}$还是$OH^{-}$、$Cl^{-}$,下列设计的方案合理的是______。
方案一:检验$CO_{3}^{2-}$:向待测液中加入足量的稀盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
方案二:检验$SO_{4}^{2-}$:先向待测液中加入稀盐酸至溶液呈酸性,未见沉淀或气体生成,再加入$BaCl_{2}$溶液出现白色沉淀
方案三:检验$OH^{-}$:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验$Cl^{-}$:向待测溶液中依次加入稀盐酸和$AgNO_{3}$溶液,有白色沉淀生成
答案:
方案二、方案三
解析 与稀盐酸反应的离子不一定是CO₃²⁻,还可能是HCO₃⁻或SO₃²⁻等,故方案一不合理;先在待测液中加入稀盐酸,可排除CO₃²⁻、SO₃²⁻及Ag⁺等的干扰,再用BaCl₂溶液检验SO₄²⁻的存在,故方案二合理;溶液中若有OH⁻,OH⁻会使石蕊溶液变成蓝色,故方案三合理;AgNO₃溶液和稀盐酸混合就有白色浑浊出现,不能证明原溶液中含有Cl⁻,故方案四不合理。
解析 与稀盐酸反应的离子不一定是CO₃²⁻,还可能是HCO₃⁻或SO₃²⁻等,故方案一不合理;先在待测液中加入稀盐酸,可排除CO₃²⁻、SO₃²⁻及Ag⁺等的干扰,再用BaCl₂溶液检验SO₄²⁻的存在,故方案二合理;溶液中若有OH⁻,OH⁻会使石蕊溶液变成蓝色,故方案三合理;AgNO₃溶液和稀盐酸混合就有白色浑浊出现,不能证明原溶液中含有Cl⁻,故方案四不合理。
查看更多完整答案,请扫码查看


