2025年资源与评价黑龙江教育出版社高中化学必修第二册人教版
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年资源与评价黑龙江教育出版社高中化学必修第二册人教版 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
第24页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
3.工业制备原理
工业制备原理
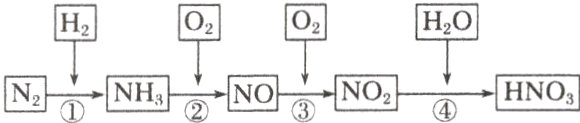
写出上述转化的化学方程式,并指出含氮物质发生的是氧化反应还是还原反应:
①______________________________,N发生________反应。
②______________________________,NH发生________反应。
③______________________________,NO 发生________反应。
④______________________________,NO2 既发生________反应,又发生______反应。
工业制备原理

写出上述转化的化学方程式,并指出含氮物质发生的是氧化反应还是还原反应:
①______________________________,N发生________反应。
②______________________________,NH发生________反应。
③______________________________,NO 发生________反应。
④______________________________,NO2 既发生________反应,又发生______反应。
答案:
①$N_{2}+3H_{2}\underset{\text{催化剂}}{\overset{\text{高温、高压}}{\rightleftharpoons }}2NH_{3}$ 还原 ②$4NH_{3}+5O_{2}\underset{\triangle }{\overset{\text{催化剂}}{\xlongequal{\;\;}}}4NO + 6H_{2}O$ 氧化 ③$2NO + O_{2}\xlongequal{\;\;}2NO_{2}$ 氧化 ④$3NO_{2}+H_{2}O\xlongequal{\;\;}2HNO_{3}+NO$ 氧化 还原
判断正误
(1)硝酸和活泼金属反应生成氢气和相应的硝酸盐 ( )
(2)硝酸的浓度越大,其氧化性越强 ( )
(3)稀硝酸可溶解Fe(OH)2生成Fe(NO3)2和水 ( )
(4)碳、铜与浓硝酸反应时,浓硝酸只表现强氧化性 ( )
(5)过量的铜和一定量浓硝酸反应,生成的气体只有二氧化氮 ( )
(6)常温下,将铝片放入浓硝酸,无明显现象,是因为铝和浓硝酸不反应 ( )
(7)王水是浓硝酸和浓盐酸体积比为1:3的混合物,能溶解金和铂 ( )
(8)实验室可以用铜和稀硝酸制备少量的NO气体 ( )
(9)浓硝酸氧化性很强,常温下就可以和碳发生反应 ( )
(1)硝酸和活泼金属反应生成氢气和相应的硝酸盐 ( )
(2)硝酸的浓度越大,其氧化性越强 ( )
(3)稀硝酸可溶解Fe(OH)2生成Fe(NO3)2和水 ( )
(4)碳、铜与浓硝酸反应时,浓硝酸只表现强氧化性 ( )
(5)过量的铜和一定量浓硝酸反应,生成的气体只有二氧化氮 ( )
(6)常温下,将铝片放入浓硝酸,无明显现象,是因为铝和浓硝酸不反应 ( )
(7)王水是浓硝酸和浓盐酸体积比为1:3的混合物,能溶解金和铂 ( )
(8)实验室可以用铜和稀硝酸制备少量的NO气体 ( )
(9)浓硝酸氧化性很强,常温下就可以和碳发生反应 ( )
答案:
(1)×
(2)√
(3)×
(4)×
(5)×
(6)×
(7)√
(8)√
(9)×
(1)×
(2)√
(3)×
(4)×
(5)×
(6)×
(7)√
(8)√
(9)×
1. (1)将铁粉溶于稀硝酸,铁元素的存在形式可能为①__________、②__________、③________。
(2)其原因为______________________________。
(2)其原因为______________________________。
答案:
(1)①$Fe(NO_{3})_{3}$ ②$Fe(NO_{3})_{2}$ ③$Fe(NO_{3})_{3}$和$Fe(NO_{3})_{2}$
(2)硝酸与变价金属(如$Fe$)反应,根据硝酸量的多少分别得到高价、低价或两种价态共存的混合物。$Fe(\text{少量})+4HNO_{3}(\text{稀})\xlongequal{\;\;}Fe(NO_{3})_{3}+NO\uparrow +2H_{2}O$;$3Fe(\text{过量})+8HNO_{3}(\text{稀})\xlongequal{\;\;}3Fe(NO_{3})_{2}+2NO\uparrow +4H_{2}O$
(1)①$Fe(NO_{3})_{3}$ ②$Fe(NO_{3})_{2}$ ③$Fe(NO_{3})_{3}$和$Fe(NO_{3})_{2}$
(2)硝酸与变价金属(如$Fe$)反应,根据硝酸量的多少分别得到高价、低价或两种价态共存的混合物。$Fe(\text{少量})+4HNO_{3}(\text{稀})\xlongequal{\;\;}Fe(NO_{3})_{3}+NO\uparrow +2H_{2}O$;$3Fe(\text{过量})+8HNO_{3}(\text{稀})\xlongequal{\;\;}3Fe(NO_{3})_{2}+2NO\uparrow +4H_{2}O$
2.
某研究小组为了探究硝酸的性质,进行如下实验操作。
(1)从试剂柜中取一瓶浓硝酸,发现其保存在____色试剂瓶中,取少量浓硝酸于试管中,发现其溶液呈"黄色",其原因是________________(用化学方程式和适当文字描述)。
该研究小组尝试将显"黄色"的浓硝酸恢复到原本的无色。下列措施合理的是______(填字母)。
a.向浓硝酸中加水
b.向浓硝酸中通入适量空气
c.加热浓硝酸
d.向浓硝酸中加入适量的NaOH固体
(2)向浓硝酸中加入稍过量铜片,该小组同学发现,生成的气体开始呈红棕色后逐渐变浅,最终气体变为无色,试写出上述反应的化学方程式:______________________________,在上述反应中,硝酸体现的性质为__________。
(3)当实验完毕,该小组同学向试管中滴入少量稀H2SO4,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:________。
(4)该小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:
______________________________,在该反应中硝酸体现的性质为______________。
某研究小组为了探究硝酸的性质,进行如下实验操作。
(1)从试剂柜中取一瓶浓硝酸,发现其保存在____色试剂瓶中,取少量浓硝酸于试管中,发现其溶液呈"黄色",其原因是________________(用化学方程式和适当文字描述)。
该研究小组尝试将显"黄色"的浓硝酸恢复到原本的无色。下列措施合理的是______(填字母)。
a.向浓硝酸中加水
b.向浓硝酸中通入适量空气
c.加热浓硝酸
d.向浓硝酸中加入适量的NaOH固体
(2)向浓硝酸中加入稍过量铜片,该小组同学发现,生成的气体开始呈红棕色后逐渐变浅,最终气体变为无色,试写出上述反应的化学方程式:______________________________,在上述反应中,硝酸体现的性质为__________。
(3)当实验完毕,该小组同学向试管中滴入少量稀H2SO4,发现铜片又逐渐溶解,产生无色气体,试写出上述反应的离子方程式:________。
(4)该小组同学向浓硝酸中加入少量碳粉,无明显现象,缓慢加热,发现碳粉逐渐溶解,产生红棕色气体,试写出上述反应的化学方程式:
______________________________,在该反应中硝酸体现的性质为______________。
答案:
(1)棕 浓硝酸不稳定,见光或受热易分解,$4HNO_{3}\xlongequal[\text{或光照}]{\triangle }4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O$,$NO_{2}$溶于浓$HNO_{3}$使溶液呈黄色 b
(2)$Cu + 4HNO_{3}(\text{浓})\xlongequal{\;\;}Cu(NO_{3})_{2}+2NO_{2}\uparrow +2H_{2}O$、$3Cu + 8HNO_{3}(\text{稀})\xlongequal{\;\;}3Cu(NO_{3})_{2}+2NO\uparrow +4H_{2}O$ 强氧化性和酸性
(3)$3Cu + 8H^{+}+2NO_{3}^{-}\xlongequal{\;\;}3Cu^{2+}+2NO\uparrow +4H_{2}O$
(4)$C + 4HNO_{3}(\text{浓})\xlongequal{\triangle }CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O$ 强氧化性
(1)棕 浓硝酸不稳定,见光或受热易分解,$4HNO_{3}\xlongequal[\text{或光照}]{\triangle }4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O$,$NO_{2}$溶于浓$HNO_{3}$使溶液呈黄色 b
(2)$Cu + 4HNO_{3}(\text{浓})\xlongequal{\;\;}Cu(NO_{3})_{2}+2NO_{2}\uparrow +2H_{2}O$、$3Cu + 8HNO_{3}(\text{稀})\xlongequal{\;\;}3Cu(NO_{3})_{2}+2NO\uparrow +4H_{2}O$ 强氧化性和酸性
(3)$3Cu + 8H^{+}+2NO_{3}^{-}\xlongequal{\;\;}3Cu^{2+}+2NO\uparrow +4H_{2}O$
(4)$C + 4HNO_{3}(\text{浓})\xlongequal{\triangle }CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O$ 强氧化性
3.
将1.92g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体1.12L(标准状况下)。则所消耗硝酸的物质的量是______________。
将1.92g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体1.12L(标准状况下)。则所消耗硝酸的物质的量是______________。
答案:
0.11 mol
查看更多完整答案,请扫码查看


