第151页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
7. 目前世界生产的镁大多数来自海水。利用海水提取镁的工业流程如图所示。下列说法错误的是( )。
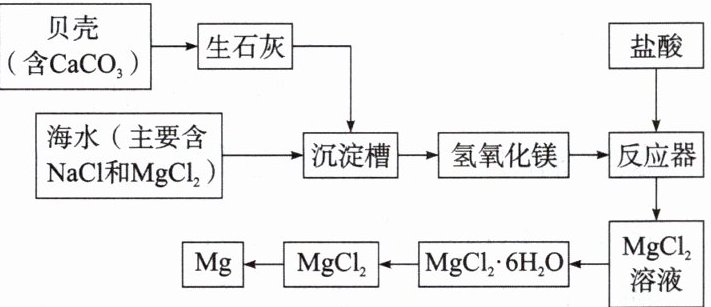
A.沉淀槽中总的化学方程式为MgCl₂ + CaO + H₂O = Mg(OH)₂↓ + CaCl₂
B.在上述流程中,元素的化合价均没有发生变化
C.反应器中发生的化学反应类型为中和反应
D.由贝壳制取生石灰的反应条件是高温

A.沉淀槽中总的化学方程式为MgCl₂ + CaO + H₂O = Mg(OH)₂↓ + CaCl₂
B.在上述流程中,元素的化合价均没有发生变化
C.反应器中发生的化学反应类型为中和反应
D.由贝壳制取生石灰的反应条件是高温
答案:
7.B
8. 海洋是人类巨大的资源宝库,下图为从海水中提取金属镁的简易流程图。
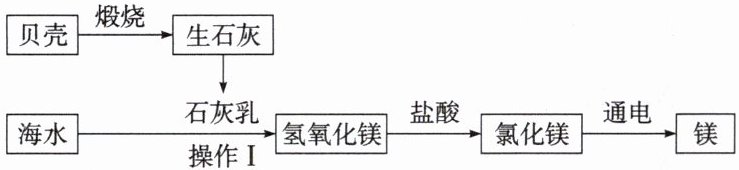
(1) 海洋中含量最多的物质是________。
(2) 实验室中进行操作Ⅰ时,玻璃棒的作用是________。
(3) 生石灰转化为石灰乳的反应是________(填“吸热”或“放热”)反应。
(4) 写出用氯化镁制取金属镁的化学方程式:________。
(5) 上述流程中涉及的基本反应类型有________种。

(1) 海洋中含量最多的物质是________。
(2) 实验室中进行操作Ⅰ时,玻璃棒的作用是________。
(3) 生石灰转化为石灰乳的反应是________(填“吸热”或“放热”)反应。
(4) 写出用氯化镁制取金属镁的化学方程式:________。
(5) 上述流程中涉及的基本反应类型有________种。
答案:
8.
(1)水
(2)引流
(3)放热
$(4)MgCl₂ \xlongequal{通电} Mg + Cl₂↑$
(5)3
(1)水
(2)引流
(3)放热
$(4)MgCl₂ \xlongequal{通电} Mg + Cl₂↑$
(5)3
9. 如图是粗盐提纯的部分实验操作。下列有关叙述错误的是( )。
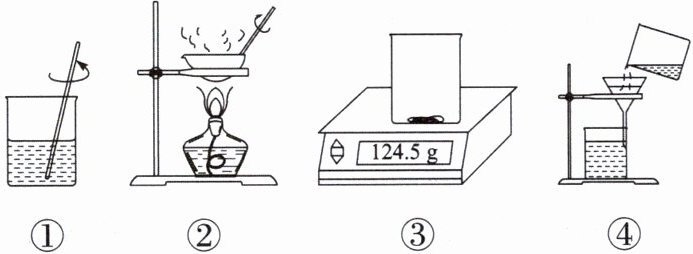
A.上述操作顺序为③①②④
B.①中水的质量可以由食盐的溶解度计算得出
C.④中缺少玻璃棒引流溶液
D.当②中蒸发皿内出现较多固体时应停止加热

A.上述操作顺序为③①②④
B.①中水的质量可以由食盐的溶解度计算得出
C.④中缺少玻璃棒引流溶液
D.当②中蒸发皿内出现较多固体时应停止加热
答案:
9.A
10. 某粗盐中含有泥沙、硫酸钠、氯化镁和氯化钙等杂质。实验小组按照下列流程对该粗盐进行提纯。
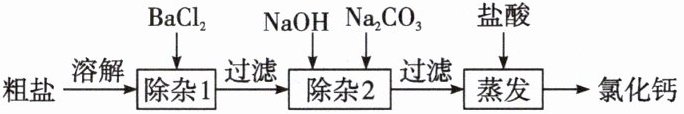
(1) 实验过程中需要配制下列规格的溶液:
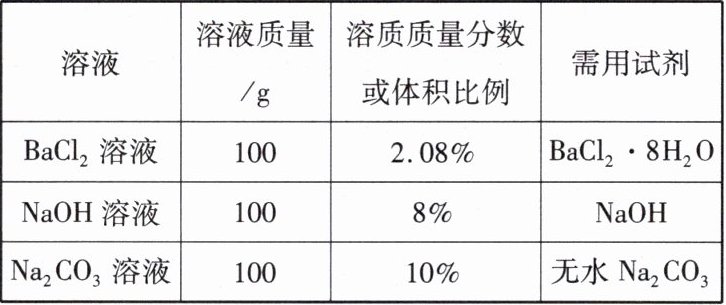
(2) ①配制100g 2.08% BaCl₂的溶液,需要BaCl₂·8H₂O晶体的质量是________g。
②准确称量8g NaOH,用92mL水充分溶解,所得溶液中NaOH的质量分数略小于8%。若不考虑操作误差,则造成NaOH质量分数偏低的原因是________。
(3) 除杂时,滴加试剂须过量,将杂质离子充分沉淀完全,再过滤除去。
①除杂2所得的沉淀的成分是________(填化学式)。
②判断滴加盐酸过量的实验方法:用玻璃棒蘸取溶液点在一片pH试纸上,________。
(4) 实验室常用“得盐率”衡量粗盐提纯的效率。已知:得盐率 = $\frac{精盐质量}{粗盐质量}$ × 100%。上述粗盐提纯中,实际得盐率均比理论值偏高,原因是________。

(1) 实验过程中需要配制下列规格的溶液:

(2) ①配制100g 2.08% BaCl₂的溶液,需要BaCl₂·8H₂O晶体的质量是________g。
②准确称量8g NaOH,用92mL水充分溶解,所得溶液中NaOH的质量分数略小于8%。若不考虑操作误差,则造成NaOH质量分数偏低的原因是________。
(3) 除杂时,滴加试剂须过量,将杂质离子充分沉淀完全,再过滤除去。
①除杂2所得的沉淀的成分是________(填化学式)。
②判断滴加盐酸过量的实验方法:用玻璃棒蘸取溶液点在一片pH试纸上,________。
(4) 实验室常用“得盐率”衡量粗盐提纯的效率。已知:得盐率 = $\frac{精盐质量}{粗盐质量}$ × 100%。上述粗盐提纯中,实际得盐率均比理论值偏高,原因是________。
答案:
10.
(1)3.52 NaOH固体易吸收空气中的水分而潮解,称量的NaOH中含有一定量的水分,导致实际的NaOH质量小于8g
(2)CaCO₃、BaCO₃ 将试纸显示的颜色与标准比色卡对照,若pH<7,则说明滴加盐酸过量
(3)在除杂过程中生成了氯化钠,导致得到的精盐质量增加
(1)3.52 NaOH固体易吸收空气中的水分而潮解,称量的NaOH中含有一定量的水分,导致实际的NaOH质量小于8g
(2)CaCO₃、BaCO₃ 将试纸显示的颜色与标准比色卡对照,若pH<7,则说明滴加盐酸过量
(3)在除杂过程中生成了氯化钠,导致得到的精盐质量增加
查看更多完整答案,请扫码查看


