第147页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
- 第115页
- 第116页
- 第117页
- 第118页
- 第119页
- 第120页
- 第121页
- 第122页
- 第123页
- 第124页
- 第125页
- 第126页
- 第127页
- 第128页
- 第129页
- 第130页
- 第131页
- 第132页
- 第133页
- 第134页
- 第135页
- 第136页
- 第137页
- 第138页
- 第139页
- 第140页
- 第141页
- 第142页
- 第143页
- 第144页
- 第145页
- 第146页
- 第147页
- 第148页
- 第149页
- 第150页
- 第151页
- 第152页
- 第153页
- 第154页
- 第155页
- 第156页
- 第157页
- 第158页
- 第159页
- 第160页
- 第161页
- 第162页
- 第163页
- 第164页
- 第165页
- 第166页
- 第167页
- 第168页
- 第169页
- 第170页
- 第171页
- 第172页
- 第173页
- 第174页
- 第175页
- 第176页
- 第177页
- 第178页
- 第179页
- 第180页
- 第181页
- 第182页
- 第183页
- 第184页
- 第185页
- 第186页
- 第187页
- 第188页
3. (2024·佛山模拟)将 X、Z 两种金属分别放入 Y(NO₃)₂的溶液中,仅 X 的表面有 Y 单质析出,则 X、Y、Z 三种金属的活动性顺序是(
A.Z>X>Y
B.X>Y>Z
C.X>Z>Y
D.Y>X>Z
B
)A.Z>X>Y
B.X>Y>Z
C.X>Z>Y
D.Y>X>Z
答案:
B
4. (2023·甘肃)现有 X、Y、Z 三种金属,如果把 Y 和 Z 分别放入硝酸银溶液中,过一会儿,在 Y 表面有银析出,而 Z 没有变化;如果把 X 和 Y 分别放入稀硫酸中,X 溶解并产生气泡,Y 不反应。根据以上实验事实,判断这三种金属的活动性由强到弱的顺序为(
A.Z、Y、X
B.X、Z、Y
C.X、Y、Z
D.Y、X、Z
C
)A.Z、Y、X
B.X、Z、Y
C.X、Y、Z
D.Y、X、Z
答案:
C
5. 常见金属 M 与硝酸银溶液反应的化学方程式为 2AgNO₃ + M = 2Ag + M(NO₃)₂。下列有关该反应的说法,错误的是(
A.该反应是置换反应
B.金属活动性 M>Ag
C.M 可能是铝
D.M 表面有固体析出
C
)A.该反应是置换反应
B.金属活动性 M>Ag
C.M 可能是铝
D.M 表面有固体析出
答案:
C
6. 某兴趣小组为探究 Zn、Fe、Cu 的活动性,进行如图所示探究实验,下列说法不正确的是(
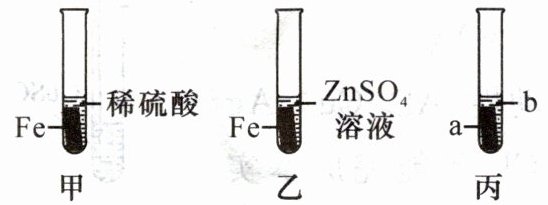
A.甲实验发生的基本反应类型为置换反应
B.通过乙实验可以比较 Zn 与 Fe 的金属活动性强弱
C.若 a 是 Zn,b 是 CuSO₄溶液,即可达到实验目的
D.若 a 是 Fe,b 是 CuSO₄溶液,则无需甲实验也能达到实验目的
C
)
A.甲实验发生的基本反应类型为置换反应
B.通过乙实验可以比较 Zn 与 Fe 的金属活动性强弱
C.若 a 是 Zn,b 是 CuSO₄溶液,即可达到实验目的
D.若 a 是 Fe,b 是 CuSO₄溶液,则无需甲实验也能达到实验目的
答案:
C
写出下列反应的化学方程式:
铁分别与稀盐酸、稀硫酸反应
锌分别与稀盐酸、稀硫酸反应
铁分别与稀盐酸、稀硫酸反应
锌分别与稀盐酸、稀硫酸反应
答案:
1. 铁与稀盐酸反应:
解:铁与稀盐酸反应生成氯化亚铁和氢气,化学方程式为$Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$。
2. 铁与稀硫酸反应:
解:铁与稀硫酸反应生成硫酸亚铁和氢气,化学方程式为$Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$。
3. 锌与稀盐酸反应:
解:锌与稀盐酸反应生成氯化锌和氢气,化学方程式为$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$。
4. 锌与稀硫酸反应:
解:锌与稀硫酸反应生成硫酸锌和氢气,化学方程式为$Zn + H_{2}SO_{4}=ZnSO_{4}+H_{2}\uparrow$。
故答案依次为:$Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$;$Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$;$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$;$Zn + H_{2}SO_{4}=ZnSO_{4}+H_{2}\uparrow$。
解:铁与稀盐酸反应生成氯化亚铁和氢气,化学方程式为$Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$。
2. 铁与稀硫酸反应:
解:铁与稀硫酸反应生成硫酸亚铁和氢气,化学方程式为$Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$。
3. 锌与稀盐酸反应:
解:锌与稀盐酸反应生成氯化锌和氢气,化学方程式为$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$。
4. 锌与稀硫酸反应:
解:锌与稀硫酸反应生成硫酸锌和氢气,化学方程式为$Zn + H_{2}SO_{4}=ZnSO_{4}+H_{2}\uparrow$。
故答案依次为:$Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$;$Fe + H_{2}SO_{4}=FeSO_{4}+H_{2}\uparrow$;$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$;$Zn + H_{2}SO_{4}=ZnSO_{4}+H_{2}\uparrow$。
查看更多完整答案,请扫码查看


