1 [2024南充中考]下列物质的俗名、化学式、分类完全正确的是 ( )
A. 水银、Hg、单质
B. 熟石灰、CaO、氧化物
C. 苛性钠、NaOH、盐
D. 纯碱、$Na_{2}CO_{3}$、碱
A. 水银、Hg、单质
B. 熟石灰、CaO、氧化物
C. 苛性钠、NaOH、盐
D. 纯碱、$Na_{2}CO_{3}$、碱
答案:
1 A 生石灰是氧化钙(CaO),熟石灰是氢氧化钙[Ca(OH)₂];NaOH属于碱;Na₂CO₃属于盐。
2 [2024重庆中考B卷]盐酸、硫酸是常见的酸。下列关于它们的说法不正确的是 ( )
A. 两者的水溶液都能导电
B. 两者的水溶液都能使紫色石蕊溶液变红
C. 将水沿烧杯内壁缓慢注入浓硫酸中进行稀释
D. 打开浓盐酸瓶盖观察到的白雾是盐酸小液滴
A. 两者的水溶液都能导电
B. 两者的水溶液都能使紫色石蕊溶液变红
C. 将水沿烧杯内壁缓慢注入浓硫酸中进行稀释
D. 打开浓盐酸瓶盖观察到的白雾是盐酸小液滴
答案:
2 C A(√):盐酸、硫酸在其水溶液中均能解离出自由移动的H⁺和酸根,故两者的水溶液都能导电。B(√):紫色石蕊溶液遇酸性溶液变红,盐酸、硫酸的水溶液都显酸性,都能使紫色石蕊溶液变红。C(×):稀释浓硫酸时,要把浓硫酸用玻璃棒引流(或沿烧杯内壁)缓慢注入水中,并用玻璃棒不断搅拌,以使热量及时扩散(如果将水注入浓硫酸,由于水的密度较小,水会浮在浓硫酸上面,浓硫酸与水混合时放出的热使水立刻沸腾,使硫酸液滴向四周飞溅)。D(√):浓盐酸易挥发,打开浓盐酸的瓶盖时,挥发出的氯化氢气体与空气中的水蒸气结合成盐酸小液滴,呈现白雾。
3 [2024成都中考]人体内一些液体的正常pH范围,如表。相关说法正确的是 ( )
人体内的一些液体的正常pH范围

A. 血浆和乳汁均显酸性
B. 胆汁比胰液的碱性强
C. 可将pH试纸放入口腔测唾液的pH
D. 饮用苏打水可以缓解胃酸过多症状
人体内的一些液体的正常pH范围

A. 血浆和乳汁均显酸性
B. 胆汁比胰液的碱性强
C. 可将pH试纸放入口腔测唾液的pH
D. 饮用苏打水可以缓解胃酸过多症状
答案:
3 D A(×):血浆的pH大于7,显碱性;乳汁的pH范围为6.6~7.6,酸性、中性、碱性都有可能。B(×):胰液的pH(7.5~8.0)大于胆汁的pH(7.1~7.3),所以胰液比胆汁的碱性强。C(×):用pH试纸测定未知溶液的pH时,正确的操作方法为:取一片pH试纸放在玻璃片或白瓷板上,用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡比较读数。不可以将pH试纸放入口腔测唾液的pH。
4 [2023怀化中考]下列各组物质在同一溶液中能大量共存,且溶液为无色的是 ( )
A. NaCl、$BaCl_{2}$、HCl
B. $CuCl_{2}$、KCl、$H_{2}SO_{4}$
C. $Ca(NO_{3})_{2}$、$Na_{2}CO_{3}$、KOH
D. HCl、NaOH、$Na_{2}SO_{4}$
A. NaCl、$BaCl_{2}$、HCl
B. $CuCl_{2}$、KCl、$H_{2}SO_{4}$
C. $Ca(NO_{3})_{2}$、$Na_{2}CO_{3}$、KOH
D. HCl、NaOH、$Na_{2}SO_{4}$
答案:
4 A A(√):三种物质相互之间不会产生沉淀、气体或水,即相互之间不会发生反应,可以在同一溶液中大量共存,且溶液为无色。B(×):氯化铜在溶液中呈蓝色。C(×):钙离子与碳酸根会结合生成碳酸钙沉淀,不能在同一溶液中大量共存。D(×):氢离子与氢氧根会结合生成水,不能在同一溶液中大量共存。
5 [2024陕西中考]关于铝、铁、银三种金属,下列有关说法正确的是 ( )
A. 三种金属在空气中均易锈蚀
B. 用稀硫酸可以区分三种金属
C. 用铁、银和硝酸铝溶液可以验证三种金属的活动性顺序
D. 三种金属均是生活中常用导线的制作材料
A. 三种金属在空气中均易锈蚀
B. 用稀硫酸可以区分三种金属
C. 用铁、银和硝酸铝溶液可以验证三种金属的活动性顺序
D. 三种金属均是生活中常用导线的制作材料
答案:
5 B A(×):铁能与空气中的水蒸气、氧气等发生反应,铁易锈蚀;铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,从而阻止铝进一步氧化;银化学性质不活泼,不易与氧气反应,铝和银均不易锈蚀。B(√):分别向三种金属中滴入稀硫酸,有气泡产生,溶液呈无色的是铝(硫酸铝溶液呈无色);有气泡产生,溶液呈浅绿色的是铁(硫酸亚铁溶液呈浅绿色);无明显现象的是银(银不与稀硫酸反应)。C(×):铁、银与硝酸铝溶液都不反应,能验证铝的金属活动性强于铁、银,但无法验证铁、银的活动性强弱。D(×):铝是生活中常用导线的制作材料,铁的导电性较差且易生锈,银的导电性良好但价格偏高,故铁、银均不是生活中常用导线的制作材料。
6 [2024滨州中考]分析推理是化学学习中常用的思维方法。下列分析推理正确的是 ( )
A. 中和反应有盐和水生成,则生成盐和水的反应一定是中和反应
B. 由金属阳离子和酸根构成的化合物属于盐,则盐中一定有金属元素
C. 化合物由不同种元素组成,则由不同种元素组成的纯净物一定是化合物
D. 活泼金属与盐酸反应有气泡产生,则与盐酸反应有气泡产生的物质一定是活泼金属
A. 中和反应有盐和水生成,则生成盐和水的反应一定是中和反应
B. 由金属阳离子和酸根构成的化合物属于盐,则盐中一定有金属元素
C. 化合物由不同种元素组成,则由不同种元素组成的纯净物一定是化合物
D. 活泼金属与盐酸反应有气泡产生,则与盐酸反应有气泡产生的物质一定是活泼金属
答案:
6 C A(×):酸和金属氧化物、碱和非金属氧化物反应同样会生成盐和水,但是这两种反应均不属于中和反应(中和反应特指酸和碱发生的反应)。B(×):由金属阳离子(或铵根)和酸根构成的化合物属于盐,盐中不一定有金属元素,如硝酸铵。D(×):与盐酸反应产生气泡的不一定是活泼金属,也可能是碳酸盐,例如碳酸钙和盐酸反应也会产生气泡。
7 [新趋势·跨学科试题][2024天津中考改编]下列劳动项目与所涉及的化学知识相符的是 ( )
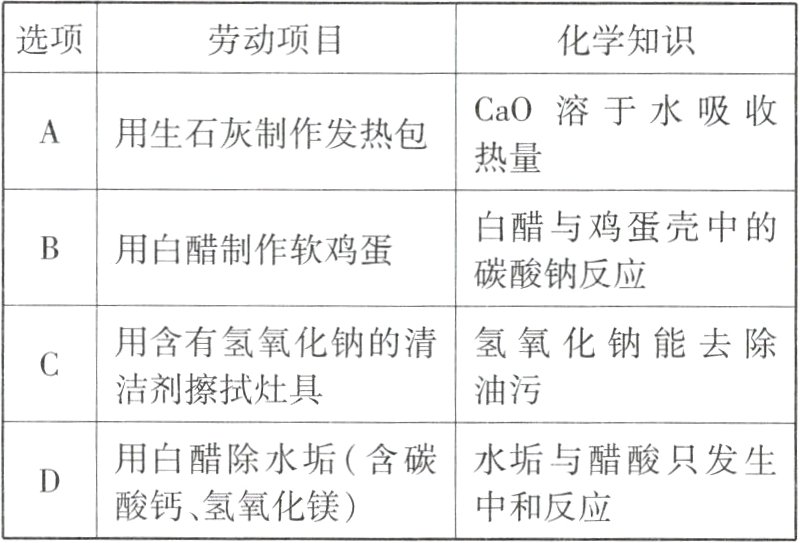

答案:
8 [创新实验][2024兰州中考]为测定某氢氧化钠固体是否变质,兴趣小组同学取一定量的样品配制成溶液,加入锥形瓶中,再逐滴加入稀盐酸至过量,并利用传感器测定$CO_{2}$的含量,如图所示,下列结论不正确的是 ( )
CO传感器
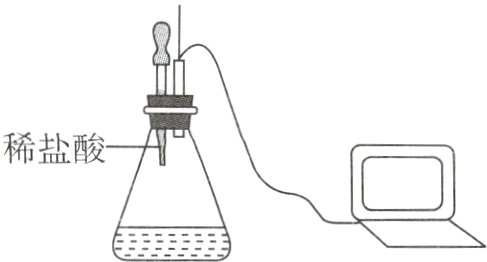

A. 氢氧化钠固体已变质
B. 0~50 s时段有中和反应发生
C. 100 s时溶液的pH>7
D. 200 s时溶液中的溶质只有一种
CO传感器


A. 氢氧化钠固体已变质
B. 0~50 s时段有中和反应发生
C. 100 s时溶液的pH>7
D. 200 s时溶液中的溶质只有一种
答案:
8 D 氢氧化钠变质实际上是氢氧化钠与空气中的二氧化碳反应生成碳酸钠和水,碳酸钠与稀盐酸反应生成氯化钠、二氧化碳和水。A(√):由题图可知,二氧化碳的体积分数逐渐增大,说明有二氧化碳气体生成,则氢氧化钠固体已变质。B(√):由题图可知,0~50 s时段有一段时间二氧化碳的体积分数没有增加,说明此时发生的反应是氢氧化钠与稀盐酸反应生成氯化钠和水,是中和反应。C(√):由题图可知,100 s时二氧化碳的体积分数还在增加,说明碳酸钠与稀盐酸的反应正在进行中,则此时溶液中含有氯化钠和碳酸钠,碳酸钠溶液显碱性,因此100 s时溶液的pH>7。D(×):由题图可知,200 s前二氧化碳的体积分数达到最大且不再变化,说明碳酸钠完全反应,由于加入的稀盐酸是过量的,所以此时溶液中的溶质有氯化钠和氯化氢。
查看更多完整答案,请扫码查看


