1 [2024 湖南中考改编]下列有关物质的性质或用途说法正确的是 ( )
A. 生石灰不能与水反应
B. 浓硫酸有挥发性
C. $Na_{2}CO_{3}$溶液能使紫色石蕊溶液变红
D. 熟石灰可用来改良酸性土壤
A. 生石灰不能与水反应
B. 浓硫酸有挥发性
C. $Na_{2}CO_{3}$溶液能使紫色石蕊溶液变红
D. 熟石灰可用来改良酸性土壤
答案:
1 D
选项正误 分析
A × 生石灰是氧化钙的俗称,氧化钙能与水反应生成氢氧化钙
B × 浓硫酸具有吸水性,浓盐酸具有挥发性
续表
选项正误 分析
C × $Na_{2}CO_{3}$溶液呈碱性,能使紫色石蕊溶液变蓝
D √ 熟石灰显碱性,能与酸性物质反应,可用于改良酸性土壤
选项正误 分析
A × 生石灰是氧化钙的俗称,氧化钙能与水反应生成氢氧化钙
B × 浓硫酸具有吸水性,浓盐酸具有挥发性
续表
选项正误 分析
C × $Na_{2}CO_{3}$溶液呈碱性,能使紫色石蕊溶液变蓝
D √ 熟石灰显碱性,能与酸性物质反应,可用于改良酸性土壤
2 [新考法][2023 聊城中考]下列有关酸、碱、盐的认识正确的是 ( )
A. 宏观:复分解反应一定有气体、沉淀和水生成
B. 微观:盐的溶液中一定含有金属阳离子
C. 变化:等质量的稀盐酸和氢氧化钠溶液充分反应,所得溶液一定呈中性
D. 实验:用湿润的 pH 试纸测定氢氧化钠溶液的 pH,结果会偏小
A. 宏观:复分解反应一定有气体、沉淀和水生成
B. 微观:盐的溶液中一定含有金属阳离子
C. 变化:等质量的稀盐酸和氢氧化钠溶液充分反应,所得溶液一定呈中性
D. 实验:用湿润的 pH 试纸测定氢氧化钠溶液的 pH,结果会偏小
答案:
2 D A(×):复分解反应发生的过程中,有气体或沉淀或水产生,不一定有气体、沉淀和水同时生成。B(×):铵盐如氯化铵、硫酸铵等溶液中含有铵根离子,不含金属阳离子。C(×):盐酸与氢氧化钠溶液发生中和反应后,只有二者恰好完全反应时,所得溶液才呈中性,等质量的稀盐酸和氢氧化钠溶液充分反应,无法确定稀盐酸与氢氧化钠溶液中的溶质质量,所得溶液不一定呈中性。D(√):用湿润的pH试纸测定氢氧化钠溶液的pH,碱溶液相当于加水稀释,碱性减弱,pH会偏小。
3 [2023 嘉兴中考]如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是 ( )
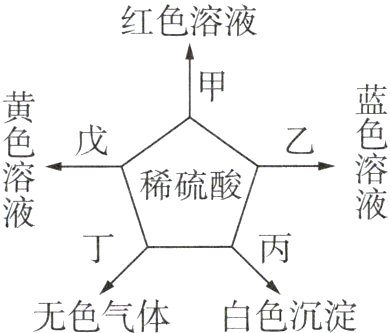
A. 甲可能是无色酚酞溶液
B. 乙、戊一定是金属单质
C. 稀硫酸与丙生成的白色沉淀不可能属于盐
D. 稀硫酸与丁的反应类型可能是置换反应

A. 甲可能是无色酚酞溶液
B. 乙、戊一定是金属单质
C. 稀硫酸与丙生成的白色沉淀不可能属于盐
D. 稀硫酸与丁的反应类型可能是置换反应
答案:
3 D A(×):稀硫酸显酸性,不能使无色酚酞溶液变红。B(×):含有铜离子的溶液呈蓝色,含有铁离子的溶液呈黄色,若乙、戊是金属单质,则分别为Cu、Fe,但稀硫酸与Fe反应生成$FeSO_{4}$溶液,为浅绿色,稀硫酸与Cu不反应,故乙、戊不是金属单质。稀硫酸与氧化铜或氢氧化铜反应生成硫酸铜和水。氧化铁与稀硫酸反应生成硫酸铁和水。C(×):稀硫酸与丙生成的白色沉淀可能属于盐,如硫酸与氯化钡反应生成的硫酸钡白色沉淀属于盐。D(√):稀硫酸能与活泼金属反应生成盐和氢气,该类反应属于置换反应,故稀硫酸与丁的反应类型可能是置换反应。
4 如图所示,分别向四支试管中加入饱和石灰水,使其与试管内溶液充分反应。无论饱和石灰水加入多少,反应后试管内溶液一定呈碱性的是 ( )
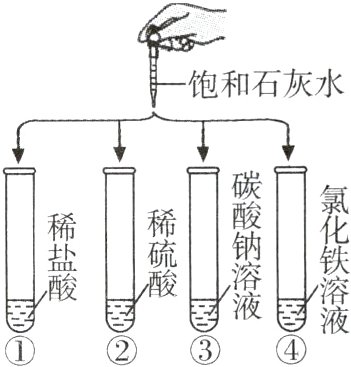
A. ①
B. ②
C. ③
D. ④

A. ①
B. ②
C. ③
D. ④
答案:
4 C A(×):饱和石灰水与稀盐酸反应生成氯化钙和水,氯化钙溶液显中性,只有饱和石灰水过量时溶液才显碱性。B(×):饱和石灰水与稀硫酸反应生成硫酸钙和水,硫酸钙溶液显中性,只有饱和石灰水过量时溶液才显碱性。C(√):饱和石灰水与碳酸钠反应生成碳酸钙沉淀和氢氧化钠,氢氧化钠和碳酸钠溶液均显碱性,则无论饱和石灰水加入多少,反应后试管内溶液一定呈碱性。D(×):饱和石灰水与氯化铁反应生成氢氧化铁沉淀和氯化钙,氯化钙溶液显中性,只有饱和石灰水过量时溶液才显碱性。
5 某同学绘制了如图所示的可以通过一步反应制取 $MgSO_{4}$的思维导图。下列所选用的物质错误的是 ( )
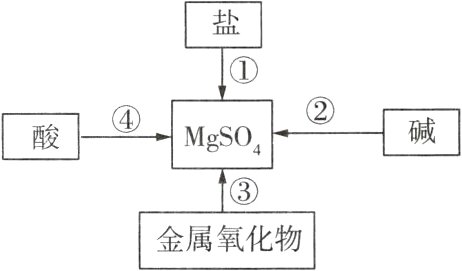
A. ① - Mg
B. ② - $MgCl_{2}$
C. ③ - $H_{2}SO_{4}$
D. ④ - $Mg(OH)_{2}$

A. ① - Mg
B. ② - $MgCl_{2}$
C. ③ - $H_{2}SO_{4}$
D. ④ - $Mg(OH)_{2}$
答案:
5 B A(√):镁和硫酸铜(或其他比镁的金属活动性弱的金属的可溶性硫酸盐)反应生成硫酸镁和铜。B(×):碱和盐反应生成新的碱和新的盐,碱和$MgCl_{2}$反应生成的是氢氧化镁沉淀,得不到硫酸镁。C(√):氧化镁和硫酸反应生成硫酸镁和水。D(√):硫酸和氢氧化镁反应生成硫酸镁和水。
6 [2024 云南中考]某溶液可能含有 HCl、$CuCl_{2}$、$CuSO_{4}$中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系如图所示。下列说法正确的是 ( )
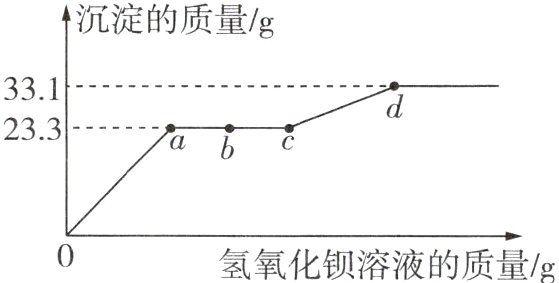
A. d 点后,溶液的 pH 保持不变
B. b 点对应的溶液中有三种溶质
C. c 点到 d 点的过程中,溶液中溶质总质量在减少
D. 原溶液含有 HCl、$CuCl_{2}$和 $CuSO_{4}$

A. d 点后,溶液的 pH 保持不变
B. b 点对应的溶液中有三种溶质
C. c 点到 d 点的过程中,溶液中溶质总质量在减少
D. 原溶液含有 HCl、$CuCl_{2}$和 $CuSO_{4}$
答案:
6 B 根据生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系,可得一开始就有沉淀生成,但$a→c$段无沉淀生成,又根据题意可知,溶液中一定有盐酸,发生的反应为$2HCl + Ba(OH)_{2}=BaCl_{2}+2H_{2}O$,$OH^{-}$可以和$H^{+}$结合,也可以和$Cu^{2+}$结合,但酸碱中和优先发生,又反应一开始就有沉淀生成,$Ba^{2+}$与$SO_{4}^{2-}$结合生成的$BaSO_{4}$沉淀,故溶液中一定有$CuSO_{4}$。图中反应分析如下:
 由图像可知,反应生成$BaSO_{4}$沉淀的质量为23.3 g,生成$Cu(OH)_{2}$沉淀的质量为33.1 g - 23.3 g = 9.8 g,设生成23.3 g $BaSO_{4}$沉淀需要$CuSO_{4}$的质量为x,生成9.8 g $Cu(OH)_{2}$沉淀需要$CuSO_{4}$的质量为y,则有:
由图像可知,反应生成$BaSO_{4}$沉淀的质量为23.3 g,生成$Cu(OH)_{2}$沉淀的质量为33.1 g - 23.3 g = 9.8 g,设生成23.3 g $BaSO_{4}$沉淀需要$CuSO_{4}$的质量为x,生成9.8 g $Cu(OH)_{2}$沉淀需要$CuSO_{4}$的质量为y,则有:
①$CuSO_{4}~BaSO_{4}$ ②$CuSO_{4}~Cu(OH)_{2}$
160 233 160 98
x 23.3 g y 9.8 g
$\frac{160}{233}=\frac{x}{23.3g}$ $\frac{160}{98}=\frac{y}{9.8g}$
解得x = 16 g、y = 16 g,则原溶液中含有$CuSO_{4}$,不含$CuCl_{2}$。
A(×):d点后反应停止,继续滴加氢氧化钡溶液,溶液碱性增强,故溶液的pH逐渐增大。B(√):b点时盐酸过量,此时溶液中存在的溶质有HCl、$BaCl_{2}$和$CuCl_{2}$。C(×):c点到d点的过程中,发生反应:$Ba(OH)_{2}+CuCl_{2}=BaCl_{2}+Cu(OH)_{2}\downarrow$,每135份质量的$CuCl_{2}$参与反应,生成208份质量的$BaCl_{2}$,则反应后溶液的质量增大,即该过程溶液中溶质总质量在增大。D(×):结合以上对图像的分析可知,原溶液中只有HCl和$CuSO_{4}$。
6 B 根据生成沉淀的质量与所加氢氧化钡溶液的质量之间的关系,可得一开始就有沉淀生成,但$a→c$段无沉淀生成,又根据题意可知,溶液中一定有盐酸,发生的反应为$2HCl + Ba(OH)_{2}=BaCl_{2}+2H_{2}O$,$OH^{-}$可以和$H^{+}$结合,也可以和$Cu^{2+}$结合,但酸碱中和优先发生,又反应一开始就有沉淀生成,$Ba^{2+}$与$SO_{4}^{2-}$结合生成的$BaSO_{4}$沉淀,故溶液中一定有$CuSO_{4}$。图中反应分析如下:
 由图像可知,反应生成$BaSO_{4}$沉淀的质量为23.3 g,生成$Cu(OH)_{2}$沉淀的质量为33.1 g - 23.3 g = 9.8 g,设生成23.3 g $BaSO_{4}$沉淀需要$CuSO_{4}$的质量为x,生成9.8 g $Cu(OH)_{2}$沉淀需要$CuSO_{4}$的质量为y,则有:
由图像可知,反应生成$BaSO_{4}$沉淀的质量为23.3 g,生成$Cu(OH)_{2}$沉淀的质量为33.1 g - 23.3 g = 9.8 g,设生成23.3 g $BaSO_{4}$沉淀需要$CuSO_{4}$的质量为x,生成9.8 g $Cu(OH)_{2}$沉淀需要$CuSO_{4}$的质量为y,则有:①$CuSO_{4}~BaSO_{4}$ ②$CuSO_{4}~Cu(OH)_{2}$
160 233 160 98
x 23.3 g y 9.8 g
$\frac{160}{233}=\frac{x}{23.3g}$ $\frac{160}{98}=\frac{y}{9.8g}$
解得x = 16 g、y = 16 g,则原溶液中含有$CuSO_{4}$,不含$CuCl_{2}$。
A(×):d点后反应停止,继续滴加氢氧化钡溶液,溶液碱性增强,故溶液的pH逐渐增大。B(√):b点时盐酸过量,此时溶液中存在的溶质有HCl、$BaCl_{2}$和$CuCl_{2}$。C(×):c点到d点的过程中,发生反应:$Ba(OH)_{2}+CuCl_{2}=BaCl_{2}+Cu(OH)_{2}\downarrow$,每135份质量的$CuCl_{2}$参与反应,生成208份质量的$BaCl_{2}$,则反应后溶液的质量增大,即该过程溶液中溶质总质量在增大。D(×):结合以上对图像的分析可知,原溶液中只有HCl和$CuSO_{4}$。
7 [2024 天津中考]如下图所示,在白色点滴板上进行酸、碱、盐性质的实验。

完成以下实验报告:
|目的|操作|现象|分析或解释|
| ---- | ---- | ---- | ---- |
|探究酸的化学性质|向 A 中滴加盐酸|粉末逐渐溶解,形成黄色溶液|盐酸与氧化铁反应|
| |向 B 中滴加盐酸|产生气泡|(1) B 中发生反应的化学方程式为____|
| |向 C 中滴加稀硫酸|溶液红色褪去|(2) C 中发生反应的化学方程式为____|
|探究碱的化学性质|向 D 中滴加氢氧化钠溶液|(3) D 中的现象为____|可溶性碱与指示剂作用|
| |向 E 中滴加氢氧化钠溶液|产生蓝色沉淀|(4) 蓝色沉淀的化学式为____|
|探究盐的化学性质|向 F 中滴加氯化钙溶液|溶液变浑浊|(5) 两种物质发生反应的反应类型为____|

完成以下实验报告:
|目的|操作|现象|分析或解释|
| ---- | ---- | ---- | ---- |
|探究酸的化学性质|向 A 中滴加盐酸|粉末逐渐溶解,形成黄色溶液|盐酸与氧化铁反应|
| |向 B 中滴加盐酸|产生气泡|(1) B 中发生反应的化学方程式为____|
| |向 C 中滴加稀硫酸|溶液红色褪去|(2) C 中发生反应的化学方程式为____|
|探究碱的化学性质|向 D 中滴加氢氧化钠溶液|(3) D 中的现象为____|可溶性碱与指示剂作用|
| |向 E 中滴加氢氧化钠溶液|产生蓝色沉淀|(4) 蓝色沉淀的化学式为____|
|探究盐的化学性质|向 F 中滴加氯化钙溶液|溶液变浑浊|(5) 两种物质发生反应的反应类型为____|
答案:
(1)$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$
(2)$H_{2}SO_{4}+2NaOH=Na_{2}SO_{4}+2H_{2}O$
(3)溶液由紫色变为蓝色
(4)$Cu(OH)_{2}$
(5)复分解反应
[解析] B:锌和盐酸反应生成氯化锌和氢气,化学方程式为$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$;
C:氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为$H_{2}SO_{4}+2NaOH=Na_{2}SO_{4}+2H_{2}O$;
D:氢氧化钠溶液显碱性,能使紫色石蕊溶液变蓝;
E:氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,蓝色沉淀是氢氧化铜;
F:碳酸钾和氯化钙反应生成碳酸钙沉淀和氯化钾,该反应是两种化合物相互交换成分,生成另外两种化合物的化学反应,属于复分解反应。
(1)$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$
(2)$H_{2}SO_{4}+2NaOH=Na_{2}SO_{4}+2H_{2}O$
(3)溶液由紫色变为蓝色
(4)$Cu(OH)_{2}$
(5)复分解反应
[解析] B:锌和盐酸反应生成氯化锌和氢气,化学方程式为$Zn + 2HCl=ZnCl_{2}+H_{2}\uparrow$;
C:氢氧化钠和硫酸反应生成硫酸钠和水,化学方程式为$H_{2}SO_{4}+2NaOH=Na_{2}SO_{4}+2H_{2}O$;
D:氢氧化钠溶液显碱性,能使紫色石蕊溶液变蓝;
E:氢氧化钠和硫酸铜反应生成氢氧化铜沉淀和硫酸钠,蓝色沉淀是氢氧化铜;
F:碳酸钾和氯化钙反应生成碳酸钙沉淀和氯化钾,该反应是两种化合物相互交换成分,生成另外两种化合物的化学反应,属于复分解反应。
查看更多完整答案,请扫码查看


