第82页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
化学方程式中所有的反应物和生成物都是指纯净物,因此必须用
纯净物
的质量代入计算。若题目中给出的是不纯物质的质量,则必须先将不纯物质
的质量换算成纯净物
的质量,然后代入计算。
答案:
纯净物 不纯物质 纯净物
1. 100 t 含铁 97%的生铁中杂质的质量为(
A.100 t
B.97 t
C.3 t
D.0.03 t
C
)A.100 t
B.97 t
C.3 t
D.0.03 t
答案:
C
2. (2024·长沙)某小苏打包装袋上标注的碳酸氢钠含量为 99%,小丽同学对此产生怀疑。她取 9 g 该小苏打样品于烧杯中,向其中加入 50 g 稀硫酸,恰好完全反应后,称得烧杯中剩余物质的质量为 54.6 g。(已知:$2NaHCO_{3}+H_{2}SO_{4}= Na_{2}SO_{4}+2CO_{2}\uparrow +2H_{2}O$,其他成分不与稀硫酸反应)
(1)计算反应中产生$CO_{2}$的质量为
(2)请计算该小苏打样品中碳酸氢钠的质量分数,并判断包装袋上碳酸氢钠含量的标注是否准确。(写出计算过程,结果精确到 0.1%)
(1)计算反应中产生$CO_{2}$的质量为
4.4
g。(2)请计算该小苏打样品中碳酸氢钠的质量分数,并判断包装袋上碳酸氢钠含量的标注是否准确。(写出计算过程,结果精确到 0.1%)
答案:
(1)4.4 (2)解:设9g该小苏打样品中碳酸氢钠的质量为x。
2NaHCO₃+H₂SO₄=Na₂SO₄+2CO₂↑+2H₂O
168 88
x 4.4g
$\frac{168}{88}=\frac{x}{4.4\,g}$ x=8.4g
则该小苏打样品中碳酸氢钠的质量分数为$\frac{8.4\,g}{9\,g}× 100\%\approx 93.3\%$,93.3%<99%,所以包装袋上碳酸氢钠含量的标注不准确。
答:该小苏打样品中碳酸氢钠的质量分数约为93.3%,包装袋上碳酸氢钠含量的标注不准确。
2NaHCO₃+H₂SO₄=Na₂SO₄+2CO₂↑+2H₂O
168 88
x 4.4g
$\frac{168}{88}=\frac{x}{4.4\,g}$ x=8.4g
则该小苏打样品中碳酸氢钠的质量分数为$\frac{8.4\,g}{9\,g}× 100\%\approx 93.3\%$,93.3%<99%,所以包装袋上碳酸氢钠含量的标注不准确。
答:该小苏打样品中碳酸氢钠的质量分数约为93.3%,包装袋上碳酸氢钠含量的标注不准确。
3. (2024·安徽改编)《天工开物》记载了锡的冶炼方法:入砂(指锡砂)数百斤,丛架木炭亦数百斤,鼓鞴(指鼓入空气)熔化……用铅少许勾引,方始(锡)沛然流注,其反应原理为$C+SnO_{2}\xlongequal {高温}Sn+CO_{2}\uparrow $。现有 151 kg 含$SnO_{2}$20%的锡砂,理论上可以炼出锡的质量是多少?(写出计算过程)
答案:
解:设理论上可以炼出锡的质量为x。
C+SnO₂$\frac{\underline{高温}}{}$Sn+CO₂↑
151 119
151kg×20% x
$\frac{151}{119}=\frac{151\,kg× 20\%}{x}$ x=23.8kg
答:理论上可以炼出锡的质量是23.8kg。
C+SnO₂$\frac{\underline{高温}}{}$Sn+CO₂↑
151 119
151kg×20% x
$\frac{151}{119}=\frac{151\,kg× 20\%}{x}$ x=23.8kg
答:理论上可以炼出锡的质量是23.8kg。
4. (2024·兰州改编)兴趣小组同学得知鸡蛋壳的主要成分是碳酸钙,就用它来测定某瓶标签破损的稀盐酸中 HCl 质量占稀盐酸质量的百分比。称取 5.5 g 干燥的鸡蛋壳(杂质不参加反应)于烧杯中,再将 75 g 该稀盐酸分 3 次加入,充分反应后得到实验数据如表:
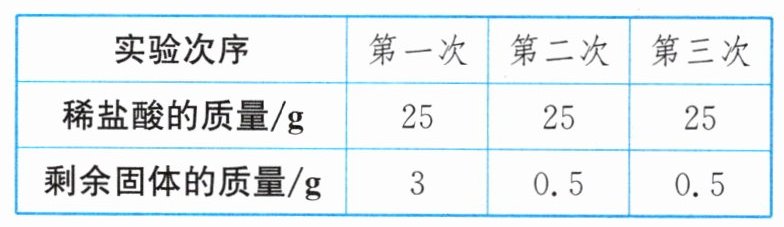
(1)鸡蛋壳中碳酸钙的质量为
(2)该稀盐酸中 HCl 质量占稀盐酸质量的百分比是多少?

(1)鸡蛋壳中碳酸钙的质量为
5.0
g。(2)该稀盐酸中 HCl 质量占稀盐酸质量的百分比是多少?
答案:
(1)5.0 (2)解:分析表中数据,25g稀盐酸能与2.5g碳酸钙恰好完全反应。设25g稀盐酸中HCl的质量为x。
CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
100 73
2.5g x
$\frac{100}{73}=\frac{2.5\,g}{x}$ x=1.825g
稀盐酸中HCl质量占稀盐酸质量的百分比为$\frac{1.825\,g}{25\,g}× 100\%=7.3\%$。
答:该稀盐酸中HCl质量占稀盐酸质量的百分比是7.3%。
CaCO₃+2HCl=CaCl₂+H₂O+CO₂↑
100 73
2.5g x
$\frac{100}{73}=\frac{2.5\,g}{x}$ x=1.825g
稀盐酸中HCl质量占稀盐酸质量的百分比为$\frac{1.825\,g}{25\,g}× 100\%=7.3\%$。
答:该稀盐酸中HCl质量占稀盐酸质量的百分比是7.3%。
查看更多完整答案,请扫码查看


