第62页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
1. 纯净物中元素之间的质量关系
(1)计算化合物中各元素的质量比:化合物中各元素的质量比= 化学式中各元素的相对原子质量与
(2)注意:元素只讲
(1)计算化合物中各元素的质量比:化合物中各元素的质量比= 化学式中各元素的相对原子质量与
各元素的原子个数
的乘积之比。如计算$P_{2}O_{5}$中各元素的质量比:$m(P):m(O)= $(31×2):(16×5)
= 31:40
。(2)注意:元素只讲
种类
,不讲个数
;用元素符号来表示化合物中各元素质量比时,元素符号前或右下角不能写数字
,如(1)中不能写成$2P:5O$(或$P_{2}:O_{5}$);计算式中元素的相对原子质量和原子个数的顺序要一致
;计算结果一般用最简整数比表示。
答案:
(1)各元素的原子个数 (31×2):(16×5) 31:40 (2)种类 个数 数字 一致
2. 计算化合物中某元素的质量分数
(1)质量分数是指组成物质的某种成分的质量在物质总质量中所占的比,可用百分数表示。
注意:这里所指的“成分”可以是
(2)化合物中某元素的质量分数=
(1)质量分数是指组成物质的某种成分的质量在物质总质量中所占的比,可用百分数表示。
注意:这里所指的“成分”可以是
元素
(如人体中钙元素的质量分数约为$1.5\%$),也可以是混合物中的某种组成物质(如人体中水的质量分数约为$70\%$),质量分数用“$\omega$”表示。(2)化合物中某元素的质量分数=
$\frac{该原子的相对原子质量(A_r)×原子个数}{化合物的相对分子质量(M_r)}$
(用计算式表示)$×100\%$,如$Fe_{3}O_{4}中铁元素的质量分数\omega(Fe)= \frac{A_{r}(Fe)×3}{M_{r}(Fe_{3}O_{4})}×100\%= \frac{56×3}{56×3 + 16×4}×100\%\approx72.4\%$,则$\omega(O)= 1 - 72.4\% = 27.6\%$。
答案:
(1)元素 (2)$\frac{该原子的相对原子质量(A_r)×原子个数}{化合物的相对分子质量(M_r)}$
3. 化合物中元素质量与化合物质量的换算
(1)元素的质量= 化合物的质量×
(2)化合物的质量= 元素的质量
(1)元素的质量= 化合物的质量×
化合物中该元素的质量分数
。(2)化合物的质量= 元素的质量
÷化合物中该元素的质量分数
。
答案:
(1)化合物中该元素的质量分数 (2)÷化合物中该元素的质量分数
1. 由化学式难以确定的是(
A.物质中各元素的质量比
B.物质中各元素的质量分数
C.物质体积的大小
D.物质的相对分子质量
C
)A.物质中各元素的质量比
B.物质中各元素的质量分数
C.物质体积的大小
D.物质的相对分子质量
答案:
C
2. (2024·山西改编)早在距今约六千年的半坡文化时期,陶制品上便出现了最早的彩绘。彩绘颜料种类多样,有红彩、黑彩和白彩(主要成分是硫酸钙等),硫酸钙$(CaSO_{4})$中,氧元素与钙元素的质量比为(
A.$5:8$
B.$8:5$
C.$5:6$
D.$6:5$
B
)A.$5:8$
B.$8:5$
C.$5:6$
D.$6:5$
答案:
B
3. (易错易混)蔗糖是食品中常用的甜味剂,其化学式为$C_{12}H_{22}O_{11}$。下列关于蔗糖的说法正确的是(
A.属于氧化物
B.$C$、$H$、$O三种元素的质量比为12:22:11$
C.$1个蔗糖分子中含有11$个水分子
D.氧元素的质量分数约为$51.5\%$
D
)A.属于氧化物
B.$C$、$H$、$O三种元素的质量比为12:22:11$
C.$1个蔗糖分子中含有11$个水分子
D.氧元素的质量分数约为$51.5\%$
答案:
D [易错分析]选错答案的原因主要是将化合物中元素的质量比和化合物中各元素的原子个数比混为一谈,误认为含氧化合物就是氧化物,误认为化合物的分子中还会含有其他物质的分子。
4. (2024·临沂)“临沂炒鸡”是临沂一张靓丽的美食名片,其特色是麻辣鲜香。“麻”的灵魂源于花椒中的花椒酰胺$(C_{16}H_{25}NO)$,下列有关花椒酰胺的说法,错误的是(
A.$1个花椒酰胺分子由43$个原子构成
B.花椒酰胺的相对分子质量为$247$
C.花椒酰胺中碳、氧元素的质量比为$16:1$
D.$247g花椒酰胺中含氮元素的质量为14g$
C
)A.$1个花椒酰胺分子由43$个原子构成
B.花椒酰胺的相对分子质量为$247$
C.花椒酰胺中碳、氧元素的质量比为$16:1$
D.$247g花椒酰胺中含氮元素的质量为14g$
答案:
C 解析:1个花椒酰胺分子是由16个碳原子、25个氢原子、1个氮原子和1个氧原子构成的,则1个花椒酰胺分子由43个原子构成,故A选项的说法正确;花椒酰胺的相对分子质量为12×16+1×25+14+16=247,故B选项的说法正确;花椒酰胺中碳、氧元素的质量比为(12×16):(16×1)=12:1,故C选项的说法错误;247g花椒酰胺中含氮元素的质量为$247g×(\frac{14}{247}×100\%)=14g$,故D选项的说法正确。
5. 茶叶中含有茶氨酸$(C_{7}H_{14}N_{2}O_{3})$,茶氨酸中各元素的质量分数如图所示。其中①表示的元素是(
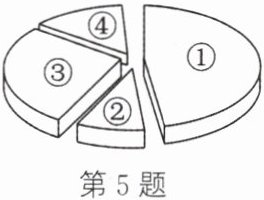
A.碳
B.氢
C.氧
D.氮
A
)
A.碳
B.氢
C.氧
D.氮
答案:
A 解析:因为(12×7)>(16×3)>(14×2)>(1×14),所以茶氨酸中各元素的质量分数由大到小的顺序为碳、氧、氮、氢。
6. (2024·齐齐哈尔)蔗糖(化学式为$C_{12}H_{22}O_{11}$)是红糖、白糖和冰糖的主要成分,是生活中常用的甜味剂。请根据蔗糖的化学式进行计算:
(1)蔗糖的相对分子质量是
(2)蔗糖中氢元素和氧元素的质量比是
(3)$34.2g$蔗糖中含有
(1)蔗糖的相对分子质量是
342
。(2)蔗糖中氢元素和氧元素的质量比是
1:8
(填最简整数比)。(3)$34.2g$蔗糖中含有
14.4
$g$碳元素。
答案:
(1)342 (2)1:8 (3)14.4
查看更多完整答案,请扫码查看


