第31页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
1. 从空气中分离出氧气
(1)氧气的工业制法——分离液态空气法(一般)
① 原理:工业上根据
② 流程:(说明:“蒸发”一词说成蒸馏更准确,“蒸馏”将在本章第4节学习)
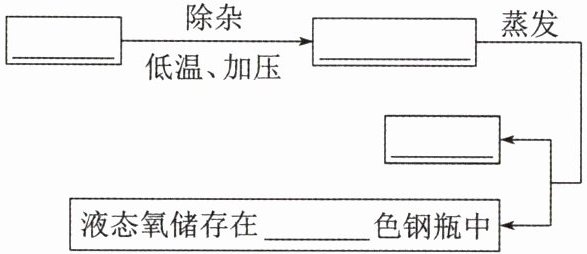
液态氧储存在
(2)在一定压力下,让空气通过特殊薄膜或多孔性材料(如
(1)氧气的工业制法——分离液态空气法(一般)
① 原理:工业上根据
氧气和氮气的沸点
不同分离出氧气,发生的是物理
变化。② 流程:(说明:“蒸发”一词说成蒸馏更准确,“蒸馏”将在本章第4节学习)

液态氧储存在
淡蓝
色钢瓶中(2)在一定压力下,让空气通过特殊薄膜或多孔性材料(如
分子筛
),将氧气和氮气分离,可以得到高纯度的氧气。
答案:
(1)①氧气和氮气的沸点 物理 ②淡蓝 (2)分子筛
2. 氧气的实验室制法(发生
(1)制取原理:实验室常用
(2)实验装置:
① 发生装置:“固液常温型”装置(用双氧水制取氧气)和“固体加热型”装置(用高锰酸钾或氯酸钾制取氧气)。用高锰酸钾制取氧气时,在试管口需放置一小团棉花,其目的是
② 收集装置:收集氧气可用
(3)装置气密性检查:检查教材P54图2 - 26中发生装置的气密性的方法是先将导管另一端插入
(4)氧气的检验和验满:用带火星的木条分别伸入
(5)用排水法收集氧气,在停止实验时,应先将导管移出水面,再熄灭酒精灯,以免因
(6)催化剂:在化学反应中能
(7)由一种物质生成两种或两种以上新物质的化学反应称为
化学
变化)(1)制取原理:实验室常用
过氧化氢溶液
(俗名为双氧水)、高锰酸钾或氯酸钾等含氧元素的物质来制取氧气,发生反应的文字表达式分别为①过氧化氢$\xrightarrow{\mathrm{二}\mathrm{氧}\mathrm{化}\mathrm{锰}}$水+氧气
;②高锰酸钾$\xrightarrow{\mathrm{加}\mathrm{热}}$锰酸钾+二氧化锰+氧气
;③氯酸钾$\xrightarrow[{\mathrm{加}\mathrm{热}}]{\mathrm{二}\mathrm{氧}\mathrm{化}\mathrm{锰}}$氯化钾+氧气
。(2)实验装置:
① 发生装置:“固液常温型”装置(用双氧水制取氧气)和“固体加热型”装置(用高锰酸钾或氯酸钾制取氧气)。用高锰酸钾制取氧气时,在试管口需放置一小团棉花,其目的是
防止高锰酸钾粉末进入导管造成堵塞或污染水槽
。② 收集装置:收集氧气可用
排水
法,也可用向上
排空气法,因为氧气不易
溶于水且不与水反应,氧气在常温下一般不与空气中的其他气体反应,且密度比空气大
。(3)装置气密性检查:检查教材P54图2 - 26中发生装置的气密性的方法是先将导管另一端插入
水中
,后用手握住试管
,观察到导管口有气泡冒出
,移开手后过一段时间,导管中会形成一段稳定的水柱
,则说明装置不漏气
。检查教材P53图2 - 25中发生装置的气密性的方法是关闭分液漏斗的活塞,将导管另一端插入水中,用双手握住锥形瓶外壁,观察到导管口有气泡逸出,移开双手后过一段时间,导管中形成一段稳定的水柱,则装置不漏气
。(4)氧气的检验和验满:用带火星的木条分别伸入
集气瓶中
和置于集气瓶口
,观察是否复燃。用排水法收集氧气时,当集气瓶口有气泡逸出时,则说明氧气已集满。(5)用排水法收集氧气,在停止实验时,应先将导管移出水面,再熄灭酒精灯,以免因
试管内气体压强减小
而产生倒吸现象
,可能造成试管炸裂(或试管破裂)
。(6)催化剂:在化学反应中能
增大(或改变)
化学反应速率,但本身的质量
和化学性质
在化学反应前后都没有发生变化
的物质称为该反应的催化剂。(7)由一种物质生成两种或两种以上新物质的化学反应称为
分解反应
。
答案:
化学 (1)过氧化氢溶液 ①过氧化氢$\xrightarrow{\mathrm{二}\mathrm{氧}\mathrm{化}\mathrm{锰}}$水+氧气 ②高锰酸钾$\xrightarrow{\mathrm{加}\mathrm{热}}$锰酸钾+二氧化锰+氧气 ③氯酸钾$\xrightarrow[{\mathrm{加}\mathrm{热}}]{\mathrm{二}\mathrm{氧}\mathrm{化}\mathrm{锰}}$氯化钾+氧气 (2)①防止高锰酸钾粉末进入导管造成堵塞或污染水槽 ②排水 上 不易 大 (3)水中 试管 气泡冒出 一段稳定的水柱 不漏气 关闭分液漏斗的活塞,将导管另一端插入水中,用双手握住锥形瓶外壁,观察到导管口有气泡逸出,移开双手后过一段时间,导管中形成一段稳定的水柱,则装置不漏气 (4)集气瓶中 集气瓶口 (5)试管内气体压强减小 倒吸现象 试管炸裂(或试管破裂) (6)增大(或改变) 质量 化学性质 没有发生变化 (7)分解反应
1. 下列关于氧气的说法错误的是(
A.工业上可采用分离液态空气法制取氧气
B.氧气支持燃烧,是一种高能清洁燃料
C.铁丝在氧气中燃烧时火星四射,放出大量的热
D.实验室制取氧气发生化学变化
B
)A.工业上可采用分离液态空气法制取氧气
B.氧气支持燃烧,是一种高能清洁燃料
C.铁丝在氧气中燃烧时火星四射,放出大量的热
D.实验室制取氧气发生化学变化
答案:
B
2. 分析氧气的收集方法时,不需要考虑的是(
A.氧气的溶解性
B.氧气能否与水或空气中其他成分反应
C.氧气的密度
D.空气中氧气的体积分数
D
)A.氧气的溶解性
B.氧气能否与水或空气中其他成分反应
C.氧气的密度
D.空气中氧气的体积分数
答案:
D
查看更多完整答案,请扫码查看


