第107页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
- 第94页
- 第95页
- 第96页
- 第97页
- 第98页
- 第99页
- 第100页
- 第101页
- 第102页
- 第103页
- 第104页
- 第105页
- 第106页
- 第107页
- 第108页
- 第109页
- 第110页
- 第111页
- 第112页
- 第113页
- 第114页
7. (教材 P172 练习与实践第 4 题变式)赤铁矿是重要的炼铁原料,其中$ Fe_2O_3 $的含量直接影响到炼铁的效率和成本。兴趣小组用一氧化碳还原 10 g 赤铁矿样品,充分反应后得到 5.6 g 铁单质,计算该赤铁矿样品中$ Fe_2O_3 $的质量分数。
答案:
解:设充分反应后得到5.6g铁单质,需要氧化铁的质量为x。
Fe₂O₃+3CO$\frac{\underline{高温}}{}$2Fe+3CO₂
160 112
x 5.6g
$\frac{160}{112}$=$\frac{x}{5.6\,g}$ x=8g
该赤铁矿样品中Fe₂O₃的质量分数为$\frac{8\,g}{10\,g}$×100%=80%。
答:该赤铁矿样品中Fe₂O₃的质量分数为80%。
Fe₂O₃+3CO$\frac{\underline{高温}}{}$2Fe+3CO₂
160 112
x 5.6g
$\frac{160}{112}$=$\frac{x}{5.6\,g}$ x=8g
该赤铁矿样品中Fe₂O₃的质量分数为$\frac{8\,g}{10\,g}$×100%=80%。
答:该赤铁矿样品中Fe₂O₃的质量分数为80%。
8. 金属是重要的资源。下列说法错误的是(
A.高炉炼铁时加入的石灰石可将二氧化硅等杂质转化为炉渣
B.电解熔融氯化镁可以制备金属镁,属于分解反应
C.用一氧化碳还原氧化铜制备铜,该反应属于化合反应
D.金矿中的金以单质形式存在,用物理方法可以制得
C
)A.高炉炼铁时加入的石灰石可将二氧化硅等杂质转化为炉渣
B.电解熔融氯化镁可以制备金属镁,属于分解反应
C.用一氧化碳还原氧化铜制备铜,该反应属于化合反应
D.金矿中的金以单质形式存在,用物理方法可以制得
答案:
C
9. 利用如图所示的实验装置模拟工业炼铁。下列说法正确的是(
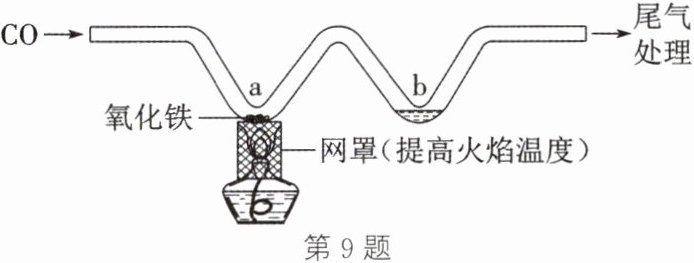
A.反应前后 Fe 元素的化合价由 + 2 变为 0
B.充分加热,a 处固体由黑色变为红棕色
C.b 处可以用澄清石灰水来检验生成的$ CO_2 $气体
D.可用水吸收尾气中的 CO
C
)
A.反应前后 Fe 元素的化合价由 + 2 变为 0
B.充分加热,a 处固体由黑色变为红棕色
C.b 处可以用澄清石灰水来检验生成的$ CO_2 $气体
D.可用水吸收尾气中的 CO
答案:
C
10. (2024·镇江科技新城实验学校段考)用如图装置研究足量木炭和 CuO 的反应。下列说法不正确的是(
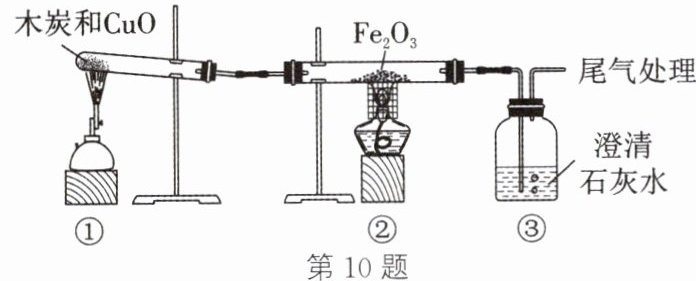
A.装置①中逐渐出现红色固体
B.装置②中固体变黑,说明装置①中生成 CO
C.装置③中变浑浊,说明装置①中生成$ CO_2$
D.向木炭和 CuO 混合物中加入少量$ CaCO_3 $固体,有助于 CuO 转化为 Cu
C
)
A.装置①中逐渐出现红色固体
B.装置②中固体变黑,说明装置①中生成 CO
C.装置③中变浑浊,说明装置①中生成$ CO_2$
D.向木炭和 CuO 混合物中加入少量$ CaCO_3 $固体,有助于 CuO 转化为 Cu
答案:
C 解析:木炭与氧化铜在高温下反应得到铜和二氧化碳(或一氧化碳),氧化铜为黑色固体,铜为红色固体,因此装置①中逐渐出现红色固体,故A的说法正确。一氧化碳具有还原性,可与氧化铁在高温下反应生成铁和二氧化碳,氧化铁为红棕色,铁为黑色,因此装置②中固体变黑,说明装置①中生成CO,故B的说法正确。二氧化碳可与氢氧化钙反应得到碳酸钙沉淀,溶液变浑浊。由于装置②中一氧化碳与氧化铁高温下反应得到铁和二氧化碳,因此装置③中变浑浊,不能说明装置①中生成二氧化碳,故C的说法错误。碳酸钙在高温下分解得到二氧化碳,木炭与二氧化碳在高温下反应得到一氧化碳,一氧化碳的量增多,有助于CuO转化为铜,故D的说法正确。
11. 某工业尾气中可能含有$ H_2、$CO 和$ CO_2 $中的一种或几种,为检验其成分,小明同学按如图装置进行实验,观察到黑色固体变红,澄清石灰水变浑浊。由此实验现象得出该工业尾气的组成情况可能有(
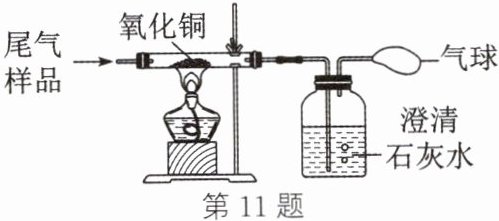
A.2 种
B.3 种
C.4 种
D.5 种
D
)
A.2 种
B.3 种
C.4 种
D.5 种
答案:
D 解析:黑色固体变红说明工业尾气中含有氢气、一氧化碳中的一种或两种,澄清石灰水变浑浊说明有二氧化碳与澄清石灰水反应,这里的二氧化碳可能是反应生成的,可能是原工业尾气中的,也可能既有反应生成的,又有原工业尾气中的。所以尾气的组成有以下5种情况:①CO;②CO和CO₂;③H₂、CO;④H₂和CO₂;⑤H₂、CO和CO₂。
查看更多完整答案,请扫码查看


