第27页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
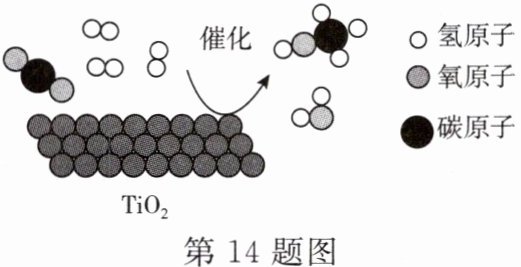
14. 亚运会在杭州成功举行,本届亚运会秉持“绿色、智能、节俭、文明”的办会理念。开幕式主火炬燃料创新使用零碳甲醇燃料,甲醇$(CH_{3}OH)$制取模型如图所示,即在二氧化钛$(TiO_{2})$催化下,将二氧化碳转化为水和甲醇。
(1)请写出制取甲醇的化学方程式:__________________________。该反应________(选填“属于”或“不属于”)四大基本反应类型。
(2)关于该反应,下列说法中正确的是(填字母)。
A. $CO_{2}$和$CH_{3}OH$都属于有机物
B. 本反应在常温下就可进行,可以节约能源
C. 利用该技术,每生成3.2t甲醇,可消耗4.4t二氧化碳
D. 该技术拓宽了人工合成有机物的途径,为人工合成其他有机物提供了参考
(1)请写出制取甲醇的化学方程式:__________________________。该反应________(选填“属于”或“不属于”)四大基本反应类型。
(2)关于该反应,下列说法中正确的是(填字母)。
A. $CO_{2}$和$CH_{3}OH$都属于有机物
B. 本反应在常温下就可进行,可以节约能源
C. 利用该技术,每生成3.2t甲醇,可消耗4.4t二氧化碳
D. 该技术拓宽了人工合成有机物的途径,为人工合成其他有机物提供了参考

答案:
$14.(1)CO₂ + 3H₂ \overset{TiO₂}= CH₃OH + H₂O $不属于
(2)BCD
(2)BCD
15. 室内起火时,如果立即打开门窗,火反而会烧得更旺,原因是__________________________;某气体是家用液化石油气的主要成分之一,该气体燃烧的化学方程式为$2R + 13O_{2}\xlongequal{点燃}8CO_{2} + 10H_{2}O$,则该气体的化学式是________________。
答案:
15.增大了空气的流通速度,补充了氧气使燃烧更旺 C₄H₁₀
16. 2023年2月3日,美国俄亥俄州一列载有危险品的火车脱轨,有毒化学品氯乙烯$(C_{2}H_{3}Cl)$大量泄漏。当地政府采用焚烧方式处理泄漏的氯乙烯,但是该过程会产生致畸、致癌、致突变的“二噁英”$(C_{12}H_{4}O_{2}Cl_{4})$,而且二噁英一旦渗透到环境之中,就很难自然降解。
(1)氯乙烯是一种
(2)氯乙烯分子中,碳、氢、氯原子个数比为
(3)187.5g氯乙烯中所含碳元素质量与
(1)氯乙烯是一种
有机物
(选填“有机物”或“无机物”)。(2)氯乙烯分子中,碳、氢、氯原子个数比为
2:3:1
。(3)187.5g氯乙烯中所含碳元素质量与
161
g二噁英中所含碳元素质量相等。
答案:
16.
(1)有机物
(2)2:3:1
(3)161
(1)有机物
(2)2:3:1
(3)161
17. 有机物是自然界物质中的一个大家族。
(1)下列是生活中常见的物质:①尿素$[CO(NH_{2})_{2}]$;②纯碱$(Na_{2}CO_{3})$;③酒精$(C_{2}H_{5}OH)$;④葡萄糖$(C_{6}H_{12}O_{6})$,其中属于有机物的是
(2)食醋是生活中常用的调味品,其主要成分是乙酸$(CH_{3}COOH)$,在乙酸分子中碳、氢、氧的原子个数比是
(3)一定质量的某有机化合物X与8g氧气恰好完全反应,生成8.8g二氧化碳和1.8g水。请计算化合物X中各元素的质量比。
(1)下列是生活中常见的物质:①尿素$[CO(NH_{2})_{2}]$;②纯碱$(Na_{2}CO_{3})$;③酒精$(C_{2}H_{5}OH)$;④葡萄糖$(C_{6}H_{12}O_{6})$,其中属于有机物的是
①③④
(填序号)。(2)食醋是生活中常用的调味品,其主要成分是乙酸$(CH_{3}COOH)$,在乙酸分子中碳、氢、氧的原子个数比是
1:2:1
。(3)一定质量的某有机化合物X与8g氧气恰好完全反应,生成8.8g二氧化碳和1.8g水。请计算化合物X中各元素的质量比。
答案:
17.
(1)①③④
(2)1:2:1
(3)8.8 g二氧化碳中含有碳元素的质量为$ 8.8 g×\frac{12}{44}×100\% = 2.4 g; 8.8 g$二氧化碳中含有氧元素的质量为 8.8 g - 2.4 g = 6.4 g; 1.8 g水中含有氢元素的质量为$ 1.8 g×\frac{2}{18}×100\% = 0.2 g; 1.8 g$水中含有氧元素的质量为 1.8 g - 0.2 g = 1.6 g; 二氧化碳和水中含有氧元素的质量之和为 8 g,正好等于参加反应的氧气的质量,则该有机物是由碳元素和氢元素组成的。则化合物 X 中碳元素和氢元素质量比为 2.4 g:0.2 g = 12:1。
(1)①③④
(2)1:2:1
(3)8.8 g二氧化碳中含有碳元素的质量为$ 8.8 g×\frac{12}{44}×100\% = 2.4 g; 8.8 g$二氧化碳中含有氧元素的质量为 8.8 g - 2.4 g = 6.4 g; 1.8 g水中含有氢元素的质量为$ 1.8 g×\frac{2}{18}×100\% = 0.2 g; 1.8 g$水中含有氧元素的质量为 1.8 g - 0.2 g = 1.6 g; 二氧化碳和水中含有氧元素的质量之和为 8 g,正好等于参加反应的氧气的质量,则该有机物是由碳元素和氢元素组成的。则化合物 X 中碳元素和氢元素质量比为 2.4 g:0.2 g = 12:1。
18. 一定质量的乙醇在氧气中不完全燃烧,生成一氧化碳、二氧化碳和水,化学方程式可表示为$mC_{2}H_{5}OH + nO_{2}\xlongequal{点燃}xCO + yCO_{2} + zH_{2}O$;则一定质量的乙醇和氧气在密闭容器中燃烧后生成一氧化碳、二氧化碳和水分子的个数比不可能是(
A.$1:1:3$
B.$1:2:5$
C.$1:3:6$
D.$2:4:9$
B
)A.$1:1:3$
B.$1:2:5$
C.$1:3:6$
D.$2:4:9$
答案:
18.B
19. 三聚氰胺$(C_{3}H_{6}N_{6})$是一种白色结晶粉末,无毒,无味,不溶于水。动物长期摄入三聚氰胺会造成生殖、泌尿系统的损害,产生膀胱、肾部结石,并可进一步诱发膀胱癌。请回答下列问题:
(1)三聚氰胺是一种
(2)如图所示是某医院用于抢救的氧气瓶上的一种装置,下列有关这种装置的说法中不正确的是
A. 导管B连接供给氧气的钢瓶
B. 导管B连接病人吸氧气的塑胶管
C. 该装置可用来观察输出氧气的速度
D. 该装置可增加吸入氧气的湿度

(1)三聚氰胺是一种
有机物
(选填“有机物”或“无机物”)。(2)如图所示是某医院用于抢救的氧气瓶上的一种装置,下列有关这种装置的说法中不正确的是
A
(填字母)。A. 导管B连接供给氧气的钢瓶
B. 导管B连接病人吸氧气的塑胶管
C. 该装置可用来观察输出氧气的速度
D. 该装置可增加吸入氧气的湿度

答案:
19.
(1)有机物
(2)A
(1)有机物
(2)A
查看更多完整答案,请扫码查看


