2025年暑假作业黑龙江教育出版社高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假作业黑龙江教育出版社高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
9. 如下图所示的实验进行一段时间后,只取烧杯内的液体进行分析,下列描述合理的是(
A.滴入几滴碘水,溶液变蓝色
B.滴入几滴$AgNO_{3}$溶液,有白色沉淀产生
C.光束通过时可产生丁达尔现象
D.烧杯内半透膜外的液体不导电
B
)A.滴入几滴碘水,溶液变蓝色
B.滴入几滴$AgNO_{3}$溶液,有白色沉淀产生
C.光束通过时可产生丁达尔现象
D.烧杯内半透膜外的液体不导电
答案:
B [烧杯内的液体为 NaCl 溶液,滴入几滴碘水溶液不变蓝,A 错误;烧杯内的液体为 NaCl 溶液,滴入几滴 $ AgNO_3 $溶液生成 AgCl 白色沉淀,B 正确;烧杯内的液体为 NaCl 溶液,不能产生丁达尔现象,C 错误;烧杯内的液体为 NaCl 溶液,具有导电性,D 错误。]
10. 铜器久置于空气中会和空气中的水蒸气、$CO_{2}$、$O_{2}$作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为$Cu_{2}(OH)_{2}CO_{3}$],“铜绿”能跟酸反应生成铜盐、$CO_{2}和H_{2}O$。某同学利用下述系列反应实现了“铜→铜绿→……→铜”的转化。
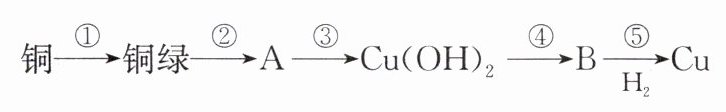
(1)从三种不同分类标准回答,“铜绿”属于哪类物质:______
(2)请写出“铜绿”与盐酸反应的化学方程式:______
(3)写出④⑤的化学方程式:④______
(4)上述转化过程中属于化合反应的是______

(1)从三种不同分类标准回答,“铜绿”属于哪类物质:______
盐、铜盐、碱式盐(或碳酸盐)
。(2)请写出“铜绿”与盐酸反应的化学方程式:______
$ Cu_2(OH)_2CO_3 + 4HCl = 2CuCl_2 + 3H_2O + CO_2↑ $
。(3)写出④⑤的化学方程式:④______
$ Cu(OH)_2 \xlongequal{\triangle} CuO + H_2O $
;⑤______$ CuO + H_2 \xlongequal{\triangle} Cu + H_2O $
。(4)上述转化过程中属于化合反应的是______
①
(填序号,下同),属于复分解反应的是______②③
,属于分解反应的是______④
。
答案:
(1)盐、铜盐、碱式盐(或碳酸盐)
(2)$ Cu_2(OH)_2CO_3 + 4HCl = 2CuCl_2 + 3H_2O + CO_2↑ $
(3)$ Cu(OH)_2 \xlongequal{\triangle} CuO + H_2O $ $ CuO + H_2 \xlongequal{\triangle} Cu + H_2O $
(4)① ②③ ④
(1)盐、铜盐、碱式盐(或碳酸盐)
(2)$ Cu_2(OH)_2CO_3 + 4HCl = 2CuCl_2 + 3H_2O + CO_2↑ $
(3)$ Cu(OH)_2 \xlongequal{\triangle} CuO + H_2O $ $ CuO + H_2 \xlongequal{\triangle} Cu + H_2O $
(4)① ②③ ④
11. 现有铁、氧化铁、稀盐酸、氢氧化钙溶液、碳酸钠溶液五种物质。存在如图所示的相互反应和转化关系。图中“——”表示两端的物质间可以发生化学反应。“→”表示物质间存在相应的转化关系。下列判断合理的是(
A.X一定是碳酸钠溶液
B.Y一定是氧化铁
C.N转化为铁的反应都属于置换反应
D.X、Y、M两两之间都可以发生复分解反应
D
)A.X一定是碳酸钠溶液
B.Y一定是氧化铁
C.N转化为铁的反应都属于置换反应
D.X、Y、M两两之间都可以发生复分解反应
答案:
D [X 可能为氢氧化钙溶液或碳酸钠溶液,故 A 错误;Y 为稀盐酸,故 B 错误;若 $ Fe_2O_3 $转化为 Fe 的反应为 $ 3CO + Fe_2O_3 \xlongequal{高温} 3CO_2 + 2Fe $,则该反应不属于置换反应,故 C 错误;X、Y、M 两两之间都可以发生复分解反应,故 D 正确。]
12. 2023年诺贝尔化学奖颁发给发现和合成量子点的科学家,如图是一种$TiO_{2}$复合氧化铁量子点,该量子点的粒径范围为$40\sim 60nm$,可用于高效率降解有机污染物。有关上述材料的说法错误的是(

A.该量子点属于混合物
B.该量子点中的氧化铁属于金属氧化物
C.该量子点是一种具有特殊功能的金属单质
D.该量子点分散于水中所得的分散系具有丁达尔效应
C
)
A.该量子点属于混合物
B.该量子点中的氧化铁属于金属氧化物
C.该量子点是一种具有特殊功能的金属单质
D.该量子点分散于水中所得的分散系具有丁达尔效应
答案:
C [根据题意可知,该量子点是 $ TiO_2 $复合氧化铁量子点,属于混合物,A 正确、C 错误;该量子点的粒径范围为 40~60 nm,则该量子点分散于水中所得的分散系属于胶体,具有丁达尔效应,D 正确。]
13. 下面是制备$Fe(OH)_{3}$胶体的三种方法。
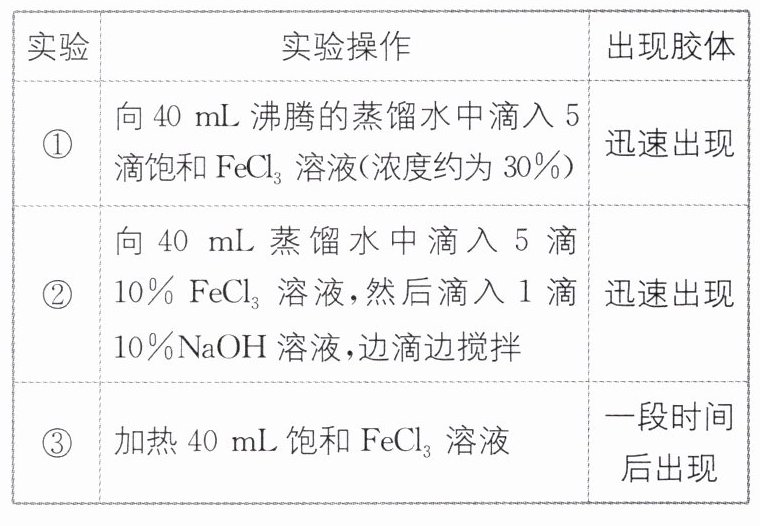
(1)实验②与实验①对比,优点是
(2)综合上述实验可知,制备$Fe(OH)_{3}$胶体提供OH⁻的物质可以是H₂O或
(3)向$Fe(OH)_{3}$胶体中逐滴加入稀硫酸,产生的现象依次是
(4)用化学方程式表示实验②的原理
(5)电解质对胶体的聚沉作用主要是由与胶粒电性相反的离子引起的,这种离子所带电荷越多,聚沉能力越强。下列物质对$Fe(OH)_{3}$胶体聚沉能力最强的是
A.$NaCl$
B.$MgSO_{4}$
C.$K_{2}CO_{3}$
D.$Na_{3}PO_{4}$

(1)实验②与实验①对比,优点是
不需加热
,$FeCl_3$溶液浓度小
。(2)综合上述实验可知,制备$Fe(OH)_{3}$胶体提供OH⁻的物质可以是H₂O或
NaOH
,控制反应条件即可制得。(3)向$Fe(OH)_{3}$胶体中逐滴加入稀硫酸,产生的现象依次是
生成红褐色沉淀
,沉淀逐渐溶解,溶液呈棕黄色
。(4)用化学方程式表示实验②的原理
$FeCl_3 + 3NaOH = Fe(OH)_3(胶体) + 3NaCl$
。(5)电解质对胶体的聚沉作用主要是由与胶粒电性相反的离子引起的,这种离子所带电荷越多,聚沉能力越强。下列物质对$Fe(OH)_{3}$胶体聚沉能力最强的是
D
(填字母)。A.$NaCl$
B.$MgSO_{4}$
C.$K_{2}CO_{3}$
D.$Na_{3}PO_{4}$
答案:
(1)不需加热 $ FeCl_3 $溶液浓度小
(2)NaOH
(3)生成红褐色沉淀 沉淀逐渐溶解,溶液呈棕黄色
(4)$ FeCl_3 + 3NaOH = Fe(OH)_3(胶体) + 3NaCl $
(5)D
解析:对比实验①和实验②可知,实验②不需要加热,且即使不是饱和 $ FeCl_3 $溶液也能生成 $ Fe(OH)_3 $胶体。
(2)根据实验①和③可知,向沸腾的蒸馏水中滴加饱和 $ FeCl_3 $溶液并加热,生成 $ Fe(OH)_3 $胶体的速度大于直接加热饱和 $ FeCl_3 $溶液,说明此时提供 $ OH^- $的物质是$ H_2O $,对比实验①和②可知,加入少量 NaOH 溶液后,即使不用饱和 $ FeCl_3 $溶液,也能生成 $ Fe(OH)_3 $胶体,此时提供 $ OH^- $的物质是 NaOH。
(3)$ Fe(OH)_3 $胶体遇到稀硫酸会先聚沉生成红褐色沉淀,继续加入稀硫酸,$ Fe(OH)_3 $和稀硫酸反应生成硫酸铁,沉淀逐渐溶解,溶液呈棕黄色。
(5)$ Fe(OH)_3 $胶粒带正电,阴离子可中和其电性使其聚沉,$ Cl^- $、$ SO_4^{2-} $、$ PO_4^{3-} $、$ CO_3^{2-} $四种阴离子中,$ PO_4^{3-} $所带负电荷最多,其聚沉能力最强,故选 D。
(1)不需加热 $ FeCl_3 $溶液浓度小
(2)NaOH
(3)生成红褐色沉淀 沉淀逐渐溶解,溶液呈棕黄色
(4)$ FeCl_3 + 3NaOH = Fe(OH)_3(胶体) + 3NaCl $
(5)D
解析:对比实验①和实验②可知,实验②不需要加热,且即使不是饱和 $ FeCl_3 $溶液也能生成 $ Fe(OH)_3 $胶体。
(2)根据实验①和③可知,向沸腾的蒸馏水中滴加饱和 $ FeCl_3 $溶液并加热,生成 $ Fe(OH)_3 $胶体的速度大于直接加热饱和 $ FeCl_3 $溶液,说明此时提供 $ OH^- $的物质是$ H_2O $,对比实验①和②可知,加入少量 NaOH 溶液后,即使不用饱和 $ FeCl_3 $溶液,也能生成 $ Fe(OH)_3 $胶体,此时提供 $ OH^- $的物质是 NaOH。
(3)$ Fe(OH)_3 $胶体遇到稀硫酸会先聚沉生成红褐色沉淀,继续加入稀硫酸,$ Fe(OH)_3 $和稀硫酸反应生成硫酸铁,沉淀逐渐溶解,溶液呈棕黄色。
(5)$ Fe(OH)_3 $胶粒带正电,阴离子可中和其电性使其聚沉,$ Cl^- $、$ SO_4^{2-} $、$ PO_4^{3-} $、$ CO_3^{2-} $四种阴离子中,$ PO_4^{3-} $所带负电荷最多,其聚沉能力最强,故选 D。
查看更多完整答案,请扫码查看


