2025年暑假作业黑龙江教育出版社高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假作业黑龙江教育出版社高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
9. 结合氮及其化合物“价—类”二维图及氧化还原反应的规律,下列分析或预测正确的是 (
A.$N_{2}O_{3}$、$NO_{2}$、$N_{2}O_{5}$均能与水反应生成酸,三者均为酸性氧化物
B.$HNO_{3}$、$HNO_{2}$、$NaNO_{3}$、$NH_{3}$的水溶液均可以导电,四者均属于电解质
C.联氨$(N_{2}H_{4})可能被亚硝酸(HNO_{2})氧化成氢叠氮酸(HN_{3})$
D.硝酸具有较强的氧化性,可用稀硝酸溶解 Au、Pt
C
)A.$N_{2}O_{3}$、$NO_{2}$、$N_{2}O_{5}$均能与水反应生成酸,三者均为酸性氧化物
B.$HNO_{3}$、$HNO_{2}$、$NaNO_{3}$、$NH_{3}$的水溶液均可以导电,四者均属于电解质
C.联氨$(N_{2}H_{4})可能被亚硝酸(HNO_{2})氧化成氢叠氮酸(HN_{3})$
D.硝酸具有较强的氧化性,可用稀硝酸溶解 Au、Pt
答案:
C [A. $ N_{2}O_{3} $、$ N_{2}O_{5} $ 为酸性氧化物,$ NO_{2} $ 溶于水生成硝酸和一氧化氮,$ NO_{2} $ 不是酸性氧化物,A 错误;B. $ NH_{3} $ 溶于水后生成的一水合氨电离出阴阳离子导电,一水合氨为电解质,氨气为非电解质,B 错误;C. 联氨 $ (N_{2}H_{4}) $ 中氮元素为 -2 价,从元素价态规律分析,可能被含有 +3 价氮元素的亚硝酸 $ (HNO_{2}) $ 氧化成氢叠氮酸 $ (HN_{3}) $,C 正确;D. 硝酸具有较强的氧化性,但 Au、Pt 需要硝酸与浓盐酸配成的王水才可以溶解,D 错误。]
10. 为证明稀硝酸与铜反应产物中气体为 NO,设计如图实验(实验过程中分液漏斗顶部玻璃塞上的凹槽与漏斗口颈上的小孔相通),下列说法不正确的是 (
A.关闭活塞,加入稀硝酸至液面 a 处
B.在装置左侧稍加加热可以加快稀硝酸与铜的反应速率
C.通过关闭或开启活塞可以控制反应的进行
D.反应开始后,胶塞下方有无色气体生成,但不能证明该气体为 NO
A
)A.关闭活塞,加入稀硝酸至液面 a 处
B.在装置左侧稍加加热可以加快稀硝酸与铜的反应速率
C.通过关闭或开启活塞可以控制反应的进行
D.反应开始后,胶塞下方有无色气体生成,但不能证明该气体为 NO
答案:
A [关闭活塞,将无法加液体到液面 a 处,A 错误;关闭活塞,生成的 NO 把稀硝酸压向右边,使铜丝与稀硝酸分离,C 正确;想证明该气体为 NO,必须使 NO 与 $ O_{2} $ 接触,生成红棕色的 $ NO_{2} $,D 正确。]
11. 某实验小组用如图装置探究炽热的木炭与浓硝酸发生的反应。
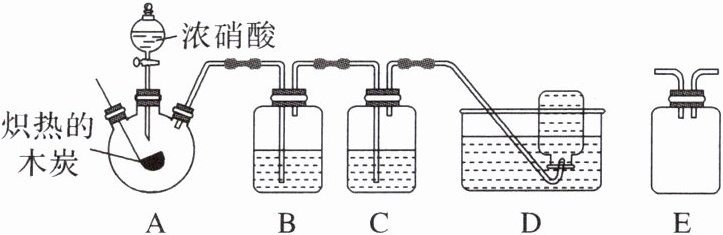
(1)按图示接好装置后,加入药品或试剂前需进行的操作是
(2)浓硝酸与炽热的木炭发生反应的化学方程式为
(3)装置 B 中盛装的是去氧蒸馏水,写出$NO_{2}与H_{2}O$反应的化学方程式:
(4)有同学建议在装置 A、B 间补充装置 E,装置 E 的作用是
(5)装置 D 中收集到某无色气体,同学甲猜想是 NO,同学乙猜想是$O_{2}$。
①若$O_{2}$是由装置 A 中反应生成的,则生成$O_{2}$对应的化学方程式为
②若同学甲的猜想正确,则移开集气瓶口的玻璃片,可观察到的现象是

(1)按图示接好装置后,加入药品或试剂前需进行的操作是
检查装置的气密性
;装置 A 中盛装浓硝酸的仪器的名称为分液漏斗
。(2)浓硝酸与炽热的木炭发生反应的化学方程式为
$ C+4HNO_{3}(浓)\overset{\triangle}{=}CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O $
。(3)装置 B 中盛装的是去氧蒸馏水,写出$NO_{2}与H_{2}O$反应的化学方程式:
$ 3NO_{2}+H_{2}O=2HNO_{3}+NO $
;装置 C 中盛装的是氢氧化钡溶液(足量),观察到的现象是生成白色沉淀
,发生反应的离子方程式为$ Ba^{2+}+2OH^{-}+CO_{2}=BaCO_{3}\downarrow +H_{2}O $
。(4)有同学建议在装置 A、B 间补充装置 E,装置 E 的作用是
作安全瓶,防止倒吸
。(5)装置 D 中收集到某无色气体,同学甲猜想是 NO,同学乙猜想是$O_{2}$。
①若$O_{2}$是由装置 A 中反应生成的,则生成$O_{2}$对应的化学方程式为
$ 4HNO_{3}(浓)\overset{\triangle}{=}4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O $
。②若同学甲的猜想正确,则移开集气瓶口的玻璃片,可观察到的现象是
集气瓶的瓶口处的气体变为红棕色
。
答案:
(1) 检查装置的气密性 分液漏斗
(2) $ C+4HNO_{3}(浓)\overset{\triangle}{=}CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O $
(3) $ 3NO_{2}+H_{2}O=2HNO_{3}+NO $ 生成白色沉淀 $ Ba^{2+}+2OH^{-}+CO_{2}=BaCO_{3}\downarrow +H_{2}O $
(4) 作安全瓶,防止倒吸
(5) ① $ 4HNO_{3}(浓)\overset{\triangle}{=}4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O $ ② 集气瓶的瓶口处的气体变为红棕色 解析
(1) 加入药品或试剂前需进行的操作是检查装置的气密性;由图可知装置 A 中盛装浓硝酸的仪器的名称为分液漏斗;
(2) 浓硝酸与炽热的木炭反应生成二氧化碳、二氧化氮和水,其化学方程式为 $ C+4HNO_{3}(浓)\overset{\triangle}{=}CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O $;
(3) 二氧化氮和水反应生成硝酸和一氧化氮,其对应的化学方程式为 $ 3NO_{2}+H_{2}O=2HNO_{3}+NO $;从 $ B \to C $ 的气体中含有二氧化碳,二氧化碳可以和氢氧化钡反应生成碳酸钡沉淀,故现象为生成白色沉淀;对应的离子方程式为 $ Ba^{2+}+2OH^{-}+CO_{2}=BaCO_{3}\downarrow +H_{2}O $;
(4) 二氧化氮在水中的溶解度较大,容易导致倒吸,故在装置 A、B 间应该有防倒吸装置,其作用是作安全瓶,防止倒吸;
(5) ① 浓硝酸分解可以生成氧气,其对应的化学方程式为 $ 4HNO_{3}(浓)\overset{\triangle}{=}4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O $;② 一氧化氮无色,容易和氧气反应生成二氧化氮,二氧化氮为红棕色气体,故可观察到的现象是集气瓶的瓶口处的气体变为红棕色。
(1) 检查装置的气密性 分液漏斗
(2) $ C+4HNO_{3}(浓)\overset{\triangle}{=}CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O $
(3) $ 3NO_{2}+H_{2}O=2HNO_{3}+NO $ 生成白色沉淀 $ Ba^{2+}+2OH^{-}+CO_{2}=BaCO_{3}\downarrow +H_{2}O $
(4) 作安全瓶,防止倒吸
(5) ① $ 4HNO_{3}(浓)\overset{\triangle}{=}4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O $ ② 集气瓶的瓶口处的气体变为红棕色 解析
(1) 加入药品或试剂前需进行的操作是检查装置的气密性;由图可知装置 A 中盛装浓硝酸的仪器的名称为分液漏斗;
(2) 浓硝酸与炽热的木炭反应生成二氧化碳、二氧化氮和水,其化学方程式为 $ C+4HNO_{3}(浓)\overset{\triangle}{=}CO_{2}\uparrow +4NO_{2}\uparrow +2H_{2}O $;
(3) 二氧化氮和水反应生成硝酸和一氧化氮,其对应的化学方程式为 $ 3NO_{2}+H_{2}O=2HNO_{3}+NO $;从 $ B \to C $ 的气体中含有二氧化碳,二氧化碳可以和氢氧化钡反应生成碳酸钡沉淀,故现象为生成白色沉淀;对应的离子方程式为 $ Ba^{2+}+2OH^{-}+CO_{2}=BaCO_{3}\downarrow +H_{2}O $;
(4) 二氧化氮在水中的溶解度较大,容易导致倒吸,故在装置 A、B 间应该有防倒吸装置,其作用是作安全瓶,防止倒吸;
(5) ① 浓硝酸分解可以生成氧气,其对应的化学方程式为 $ 4HNO_{3}(浓)\overset{\triangle}{=}4NO_{2}\uparrow +O_{2}\uparrow +2H_{2}O $;② 一氧化氮无色,容易和氧气反应生成二氧化氮,二氧化氮为红棕色气体,故可观察到的现象是集气瓶的瓶口处的气体变为红棕色。
查看更多完整答案,请扫码查看


