2025年暑假作业黑龙江教育出版社高一化学
注:目前有些书本章节名称可能整理的还不是很完善,但都是按照顺序排列的,请同学们按照顺序仔细查找。练习册 2025年暑假作业黑龙江教育出版社高一化学 答案主要是用来给同学们做完题方便对答案用的,请勿直接抄袭。
2. 为了探究钠的性质,某化学兴趣小组设计了如图所示装置进行实验,下列说法错误的是(
A.密度:$CuSO_4$溶液 > Na > 煤油
B.溶液中有红色固体生成
C.实验过程中,关闭弹簧夹,一段时间后,长颈漏斗中的液面上升
D.可观察到有气泡生成,钠在煤油和$CuSO_4$溶液交界处上下跳动
B
)A.密度:$CuSO_4$溶液 > Na > 煤油
B.溶液中有红色固体生成
C.实验过程中,关闭弹簧夹,一段时间后,长颈漏斗中的液面上升
D.可观察到有气泡生成,钠在煤油和$CuSO_4$溶液交界处上下跳动
答案:
B [如图装置中由下到上分别为CuSO₄溶液、Na、煤油,所以密度:CuSO₄溶液>Na>煤油,A正确;CuSO₄溶液与Na的反应是钠与水先发生反应生成NaOH,NaOH再与CuSO₄溶液反应生成蓝色沉淀Cu(OH)₂,B错误;实验过程中,关闭弹簧夹,一段时间后,生成的氢气使装置内气压增大,长颈漏斗中的液面上升,C正确;可观察到有气泡生成,将钠推入煤油层中,钠与水的反应停止后又落回水中,再生成氢气,如此往复可以看到钠在煤油和CuSO₄溶液交界处上下跳动,D正确。]
3. 用洁净的铂丝蘸取某无色溶液,放在火焰上灼烧,火焰的颜色呈黄色,下列说法错误的是(
A.该溶液中可能含有钠离子,一定没有钾离子
B.该溶液中一定含有钠离子
C.该溶液中一定没有铜离子
D.该溶液中可能含有钾离子
A
)A.该溶液中可能含有钠离子,一定没有钾离子
B.该溶液中一定含有钠离子
C.该溶液中一定没有铜离子
D.该溶液中可能含有钾离子
答案:
A
4. 已知A是一种金属单质,B显淡黄色,A、B、C、D之间的转化关系如图所示,下列说法错误的是(
A.C是碳酸钠
B.D应密封保存
C.A与$O_2$反应只能生成B
D.反应①、②中生成的气体相同
C
)A.C是碳酸钠
B.D应密封保存
C.A与$O_2$反应只能生成B
D.反应①、②中生成的气体相同
答案:
C [B为A与氧气反应的产物,为氧化物,颜色为淡黄色,应为Na₂O₂,则A为Na,C为Na₂CO₃,D为NaOH,易潮解,故应密封保存,反应①是过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应②是过氧化钠和水反应生成氢氧化钠和氧气。]
5. 下列实验设计,不能达到实验目的的是(
B
)
答案:
B [K元素的焰色试验必须透过蓝色钴玻璃观察,滤去黄光的干扰,故A正确;碳酸氢钠不稳定,受热分解生成Na₂CO₃、CO₂、H₂O,小试管中应该盛放碳酸氢钠,故B错误;过氧化钠和水反应生成氧气,能使带火星的木条复燃,故C正确;Na₂CO₃、NaHCO₃和稀盐酸反应生成气泡的快慢不同,从而可以比较NaHCO₃和Na₂CO₃与盐酸反应的快慢,故D正确。]
6. 下列有关实验操作、现象和解释或结论都正确的是(
B
)
答案:
B [向溶液中加入稀盐酸产生的气体能使澄清石灰水变浑浊,该溶液中也可能含有HCO₃⁻,故A错误;向饱和Na₂CO₃溶液中通入足量CO₂,发生反应:Na₂CO₃ + CO₂ + H₂O = 2NaHCO₃↓,因相同条件下,碳酸氢钠的溶解度小于碳酸钠,则有NaHCO₃晶体析出,故B正确;火焰呈黄色,只能说明溶液中含有Na⁺,观察K⁺的火焰需要透过蓝色钴玻璃,故C错误;向Na₂CO₃粉末中滴加几滴水,少量溶解,没有准确的相对量的关系,不能说明碳酸钠溶解性大小,故D错误。]
7. 以不同类别物质间的转化为线索,认识钠及其化合物。
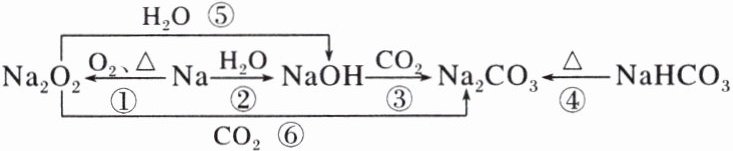
下列分析不正确的是(
A.反应③表明$CO_2$具有酸性氧化物的性质
B.反应④说明$NaHCO_3$的稳定性强于$Na_2CO_3$
C.反应⑤⑥说明$Na_2O_2$可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应等

下列分析不正确的是(
B
)A.反应③表明$CO_2$具有酸性氧化物的性质
B.反应④说明$NaHCO_3$的稳定性强于$Na_2CO_3$
C.反应⑤⑥说明$Na_2O_2$可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应等
答案:
B [反应③的化学方程式为2NaOH + CO₂ = Na₂CO₃ + H₂O,NaOH为碱,Na₂CO₃为盐,因此CO₂具有酸性氧化物的性质,故A正确;反应④是2NaHCO₃ $\xlongequal{\triangle}$ Na₂CO₃ + CO₂↑ + H₂O,说明Na₂CO₃比NaHCO₃稳定,故B错误;反应⑤⑥分别是2Na₂O₂ + 2H₂O = 4NaOH + O₂↑、2Na₂O₂ + 2CO₂ = 2Na₂CO₃ + O₂,因此反应⑤⑥说明Na₂O₂可用于潜水艇中氧气的供给,故C正确;反应④为分解反应,反应①为化合反应,反应②为置换反应,故D正确。]
8. 过量的$NaHCO_3$与$Na_2O_2$混合,在密闭容器中充分加热后,最后排出气体,残留的物质应是(
A.$Na_2O$和$Na_2O_2$
B.$Na_2O_2$和$Na_2CO_3$
C.$Na_2CO_3$
D.$Na_2O$
C
)A.$Na_2O$和$Na_2O_2$
B.$Na_2O_2$和$Na_2CO_3$
C.$Na_2CO_3$
D.$Na_2O$
答案:
C [在题中所给出的两种物质中NaHCO₃是过量的,两种混合物在密闭容器中加热所发生的化学反应为2NaHCO₃ $\xlongequal{\triangle}$ Na₂CO₃ + H₂O + CO₂↑、2Na₂O₂ + 2CO₂ = 2Na₂CO₃ + O₂、2Na₂O₂ + 2H₂O = 4NaOH + O₂↑、2NaOH + CO₂ = Na₂CO₃ + H₂O;因NaHCO₃是过量的,又充分加热,有足够的CO₂使Na₂O₂最终全部转化为Na₂CO₃,过量的NaHCO₃也完全分解成Na₂CO₃,而Na₂CO₃稳定,受热不易分解,故最后排出产生的气体后,残留的固体是Na₂CO₃。]
9. 碳酸钠和碳酸氢钠是生活中常见的物质。请回答下列问题:
(1)碳酸氢钠的化学式是
(2))碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为
(1)碳酸氢钠的化学式是
NaHCO₃
,俗称小苏打
,其水溶液显碱
(填“酸”“碱”或“中”)性。(2))碳酸氢钠可治疗胃酸(0.2%~0.4%的盐酸)过多,反应的离子方程式为
H⁺ + HCO₃⁻ = H₂O + CO₂↑
。等质量的碳酸钠和碳酸氢钠与足量盐酸反应时生成$CO_2$的量:前者<
(填“>”“<”或“=”)后者。(3)除去碳酸钠固体中碳酸氢钠的反应的化学方程式为
2NaHCO₃ $\xlongequal{\triangle}$ Na₂CO₃ + H₂O + CO₂↑
。
答案:
(1)NaHCO₃ 小苏打 碱
(2)H⁺ + HCO₃⁻ = H₂O + CO₂↑ <
(3)2NaHCO₃ $\xlongequal{\triangle}$ Na₂CO₃ + H₂O + CO₂↑
(1)NaHCO₃ 小苏打 碱
(2)H⁺ + HCO₃⁻ = H₂O + CO₂↑ <
(3)2NaHCO₃ $\xlongequal{\triangle}$ Na₂CO₃ + H₂O + CO₂↑
查看更多完整答案,请扫码查看


