第74页
- 第1页
- 第2页
- 第3页
- 第4页
- 第5页
- 第6页
- 第7页
- 第8页
- 第9页
- 第10页
- 第11页
- 第12页
- 第13页
- 第14页
- 第15页
- 第16页
- 第17页
- 第18页
- 第19页
- 第20页
- 第21页
- 第22页
- 第23页
- 第24页
- 第25页
- 第26页
- 第27页
- 第28页
- 第29页
- 第30页
- 第31页
- 第32页
- 第33页
- 第34页
- 第35页
- 第36页
- 第37页
- 第38页
- 第39页
- 第40页
- 第41页
- 第42页
- 第43页
- 第44页
- 第45页
- 第46页
- 第47页
- 第48页
- 第49页
- 第50页
- 第51页
- 第52页
- 第53页
- 第54页
- 第55页
- 第56页
- 第57页
- 第58页
- 第59页
- 第60页
- 第61页
- 第62页
- 第63页
- 第64页
- 第65页
- 第66页
- 第67页
- 第68页
- 第69页
- 第70页
- 第71页
- 第72页
- 第73页
- 第74页
- 第75页
- 第76页
- 第77页
- 第78页
- 第79页
- 第80页
- 第81页
- 第82页
- 第83页
- 第84页
- 第85页
- 第86页
- 第87页
- 第88页
- 第89页
- 第90页
- 第91页
- 第92页
- 第93页
1. 有关中和反应的叙述错误的是 ( )
A. 一定有沉淀生成
B. 一定有水生成
C. 一定是酸和碱反应
D. 一定放热
A. 一定有沉淀生成
B. 一定有水生成
C. 一定是酸和碱反应
D. 一定放热
答案:
A
2.(2024·黑龙江大庆改编)下列化学反应属于中和反应的是 ( )
A. $Al_{2}O_{3}+3H_{2}SO_{4}=Al_{2}(SO_{4})_{3}+3H_{2}O$
B. $Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$
C. $CO_{2}+Ca(OH)_{2}=CaCO_{3}\downarrow +H_{2}O$
D. $H_{2}SO_{4}+2NaOH = 2H_{2}O+Na_{2}SO_{4}$
A. $Al_{2}O_{3}+3H_{2}SO_{4}=Al_{2}(SO_{4})_{3}+3H_{2}O$
B. $Fe + 2HCl=FeCl_{2}+H_{2}\uparrow$
C. $CO_{2}+Ca(OH)_{2}=CaCO_{3}\downarrow +H_{2}O$
D. $H_{2}SO_{4}+2NaOH = 2H_{2}O+Na_{2}SO_{4}$
答案:
D
3. 下列生产、生活中的应用,利用了中和反应原理的是 ( )
A. 生石灰用作食品干燥剂
B. 用熟石灰和硫酸铜配制波尔多液
C. 用盐酸除铁锈
D. 用硼酸处理沾在皮肤上的碱液
A. 生石灰用作食品干燥剂
B. 用熟石灰和硫酸铜配制波尔多液
C. 用盐酸除铁锈
D. 用硼酸处理沾在皮肤上的碱液
答案:
D
4. 中和反应有着广泛的应用。
(1)中和反应应用于医药卫生方面。当人体中胃酸过多时,通常服用________性药物。
一种胃药叫作胃舒平,主要成分是$Al(OH)_{3}$,写出其与人体中胃酸反应的化学方程式:________________________。
(2)中和反应可应用在农业改良土壤方面。改良酸性土壤通常用熟石灰,是因为熟石灰是________性物质。某地土壤呈酸性,是因为土壤中含有少量的硫酸,请写出用熟石灰改良该土壤时所发生反应的化学方程式:______________________________。
(3)据报道,某地一辆载着硫酸的罐车突然翻车,导致大量硫酸泄漏,赶到现场的消防队员用大量的烧碱$(NaOH)$覆盖泄漏现场,此时所发生反应的化学方程式为________________________,消防队员运用的是________反应原理。
(1)中和反应应用于医药卫生方面。当人体中胃酸过多时,通常服用________性药物。
一种胃药叫作胃舒平,主要成分是$Al(OH)_{3}$,写出其与人体中胃酸反应的化学方程式:________________________。
(2)中和反应可应用在农业改良土壤方面。改良酸性土壤通常用熟石灰,是因为熟石灰是________性物质。某地土壤呈酸性,是因为土壤中含有少量的硫酸,请写出用熟石灰改良该土壤时所发生反应的化学方程式:______________________________。
(3)据报道,某地一辆载着硫酸的罐车突然翻车,导致大量硫酸泄漏,赶到现场的消防队员用大量的烧碱$(NaOH)$覆盖泄漏现场,此时所发生反应的化学方程式为________________________,消防队员运用的是________反应原理。
答案:
碱@@$\mathrm{Al(OH)_3 + 3HCl = AlCl_3 + 3H_2O}$@@碱@@$\mathrm{Ca(OH)_2 + H_2SO_4 = CaSO_4 + 2H_2O}$@@$\mathrm{2NaOH + H_2SO_4 = Na_2SO_4 + 2H_2O}$@@中和
5. 新趋势 创新实验 (2024·江苏苏州模拟)电导率是衡量溶液导电能力大小的物理量,在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,盐酸和氢氧化钠反应电导率曲线如右下图所示,以下分析不正确的是 ( )
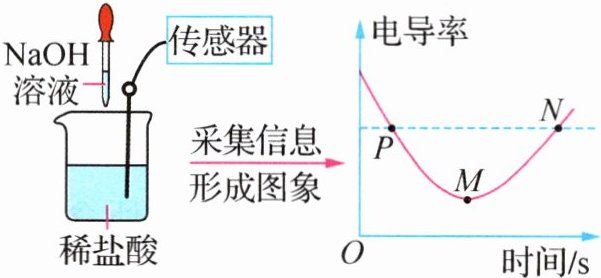
A. 实验开始到$M$点溶液电导率减小可能是由于溶液中离子数量逐渐减小
B. $M$点时$NaOH$溶液与稀盐酸恰好完全反应
C. $N$点时溶液中的离子数量大于$P$点
D. 该实验证明溶液中始终含有带电的粒子

A. 实验开始到$M$点溶液电导率减小可能是由于溶液中离子数量逐渐减小
B. $M$点时$NaOH$溶液与稀盐酸恰好完全反应
C. $N$点时溶液中的离子数量大于$P$点
D. 该实验证明溶液中始终含有带电的粒子
答案:
A@@【解析】在相同条件下,电导率与离子浓度(单位体积内的离子数)成正比,不能只说离子数量,故A错误;M点时溶液的电导率最低,说明此时氢氧化钠与盐酸恰好完全反应,溶液中的离子浓度最小,故B正确;P点和N点的电导率相等,说明溶液中的离子浓度相等,因为实验中是向稀盐酸中加入氢氧化钠溶液,则溶液的体积变大,所以N点时溶液中的离子数量大于P点,故C正确;反应过程中,溶液始终具有导电性,即该实验证明溶液中始终含有带电的粒子,故D正确。
6. 向盛有$50 mL$稀硫酸的烧杯中,缓慢滴加一定溶质质量分数的氢氧化钡溶液至过量[已知$H_{2}SO_{4}+Ba(OH)_{2}=BaSO_{4}\downarrow +2H_{2}O$],随着氢氧化钡溶液的滴加,某些量的变化趋势如下图所示,其中正确的是 ( )
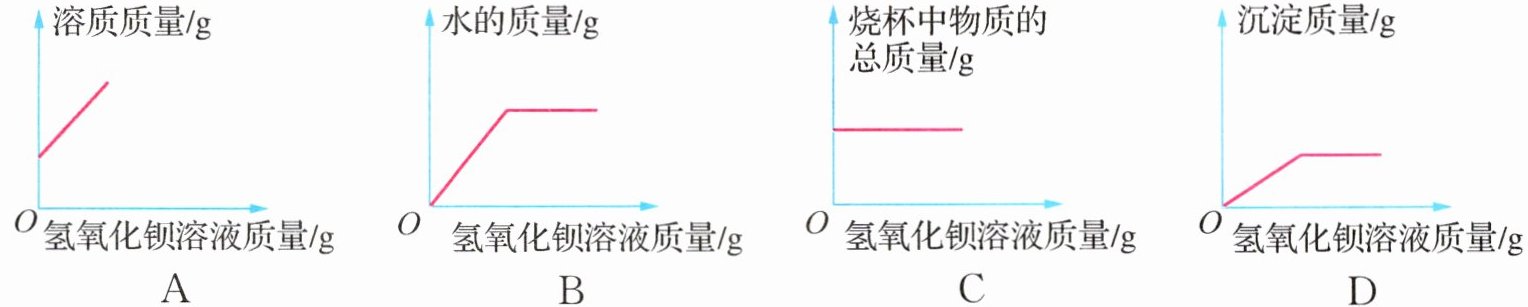

答案:
D@@【解析】在刚开始加入氢氧化钡溶液时,稀硫酸与氢氧化钡反应生成硫酸钡沉淀和水,溶质的质量不断减小,到完全反应后再加入氢氧化钡溶液,溶质的质量才开始慢慢增大,故A错误;稀硫酸中含有水,故曲线不会从原点开始,由于反应有水生成,且稀硫酸和氢氧化钡溶液中都含有水,所以水的质量不断增大,且前期比后期的增幅更大,故B错误;随着氢氧化钡溶液的不断加入,烧杯中物质的总质量在不断增大,故C错误;稀硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,当硫酸反应完后,沉淀的质量不再改变,故D正确。
查看更多完整答案,请扫码查看


